05. halo alkana, alkohol, dan eter.pptx
- 1. DIREKTORAT JENDERAL GURU DAN TENAGA KEPENDIDIKAN KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN 2017 KOMPETENSI PROFESIONAL KELOMPOK KOMPETENSI D KIMIA SMA Halo Alkana, Alkohol, dan Eter
- 2. TUJUAN Setelah belajar dengan modul ini diharapkan Anda dapat: 1. Menjelaskan struktur alkohol, eter dan haloalkana; 2. Menjelaskan tata nama alkohol, eter, dan haloalkana; 3. Memahami sifat alkohol, eter dan haloalkana; 4. Memahami kegunaan alkohol, eter dan haloalkana dalam kehidupan sehari-hari. 2
- 3. INDIKATOR Kompetensi yang diharapkan adalah: 1. Menjelaskan struktur alkohol, eter dan haloalkana; 2. Mengidentifikasi struktur alkohol, eter dan haloalkana; 3. Menentukan tatanama alkohol, eter dan haloalkana; 4. Membedakan sifat alkohol, eter dan haloalkana; 5. Menganalisis sifat senyawa alkohol, eter dan haloalkana; 6. Kegunaan alkohol, eter dan haloalkana dalam kehidupan sehari-hari. 3
- 4. SKENARIO 4 Pendahuluan Review Mengkaji materi modul Melakukan aktivitas pembelajaran ( diskusi/ ekperimen/latihan) Presentasi dan Konfirmasi Latihan Soal Uji Kompetens i
- 5. Tugas dan Lk Setelah mengkaji modul D profesional materi Alkohol, Eter dan Haloalkana, tugas yang dikerjakan adalah : 1. Membuat peta konsep mengenai materi Alkohol, Eter dan Haloalkana 2. Mengerjakan LK 1 mengenai Sifat fisik dan kimia alkohol 3. Presentasi hasil praktikum 5
- 6. Struktur halo alkana, alkohol, dan eter REAKSI PENGENALAN GUGUS FUNGSI B GUGUS FUNGSI A Menu
- 7. A HALO ALKANA GUGUS FUNGSI RUMUS KIMIA Back
- 8. A ALKANOL / ALKOHOL GUGUS FUNGSI RUMUS KIMIA Back Rumus struktur : R-C-OH Rumus molekul : CnH2n+2O Gugus fungsi : -OH
- 9. 9 No. Rumus Molekul Alkil Nama Rumus Struktur 1. CH3OH CH3- Metanol CH3 - OH 2. C2H5OH C2H5- Etanol CH3- CH2 - OH 3. C3H7OH C3H7- Propanol CH3- CH2 – CH2 - OH 4. C4H9OH C4H9- Butanol CH3- CH2 – CH2 - CH2 - OH Beberapa senyawa alkanol Bila kita perhatikan pada tabel di atas, pada deret homolog alkanol terdapat gugus fungsi hidroksil (-OH) yang terikat pada sebuah atom karbon. Alkanol disebut juga turunan alkana dimana sebuah atom H- nya diganti dengan gugus –OH. Rumus umum alkanol atau alkohol adalah R - OH atau CnH2n+2O
- 10. 10 Alkohol Primer Alkohol Sekunder Alkohol Tersier Dimana R adalah gugus alkil, untuk R, R’ dan R’’ bisa sama atau berbeda
- 11. Berdasarkan letak gugus fungsinya, alkohol dibedakan menjadi 3 1. Alkohol primer : gugus –OH terletak pada atom C primer 2. Alkohol sekunder : gugus –OH terletak pada atom C sekunder 3. Alkohol tersier : gugus –OH terletak pada atom C tersier Reaksi pada alkohol 1. Alkohol bereaksi dengan logam Na menghasikan gas H2 R-OH + Na 2 RONa + H2 2. Alkohol bereaksi dengan asam karboksilat membentuk ester (reaksi esterifikasi) R-OH + RCOOH RCOOR’ + H2O
- 12. 3. Reaksi oksidasi a. Alkohol primer dapat dioksidasi oleh kalium dikromat membentuk asetaldehid O || 3RCH2OH + Cr2O7 2- + 8 H+ 3R-C-H + 2Cr3+ + H2O b. Alkohol sekunder dapat dioksidasi oleh K2Cr2O7 atau CrO3 membentuk keton R’ R’ | | R-CH-OH + K2Cr2O7 atau CrO3 R-C=O c. Alkohol tersier tidak dapat teroksidasi Alkohol tersier 4. Reaksi alkohol dengan hidrogen halida CH3OH + HBr CH3Br + H2O 5. Reaksi eliminasi alkohol dengan adanya asam sulfat pada temperatur tinggi membentuk alkena CH3CH2OH 200oC, H2SO4 CH2=CH2 + H2O
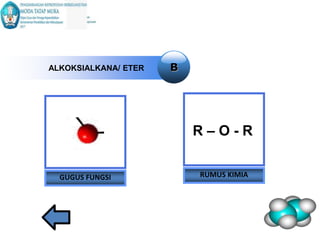
- 13. ALKOKSIALKANA/ ETER GUGUS FUNGSI RUMUS KIMIA B R – O - R
- 14. ETER / ALKOKSI ALKANA 2. TATA NAMA A. TATA NAMA IUPAC R –O – R Alkoksi alkana 1). Gugus alkil besar dianggap rantai induk 2). Gugus alkil kecil dianggap cabang 3). Penomoran dimulai dari dari alkil besar sehingga gugus alkoksi nomor sekecil mungkin 1. CH3 – O – CH3 = Metoksi metana 2. CH3 – O – CH2 – CH3 = Metoksi etana 3. CH3 – O – CH2 – CH2 – CH3 = 1-Metoksi propana 4. CH3 – O – CH –CH3 = 2-Metoksi propana I CH3
- 15. ETER / ALKOKSI ALKANA A. TATA NAMA IUPAC 5. CH3 – O – CH - CH2 – CH3 = 2-Metoksi butana I CH3 6. CH3 – O – CH 2- CH – CH3 = 1-Metoksi – 2- metil propana I CH3 7. CH3 – O – CH 2- CH – CH3 = 1-Metoksi – 2- metil propana I CH3
- 16. ETER / ALKOKSI ALKANA A. TATA NAMA IUPAC 8. CH3 – CH2 - O – CH - CH2 – CH3 = 2-Etoksi - butana I CH3 9. CH3 – CH2 - O – CH 2- CH – CH3 = 1-Metoksi – 2- metil propana I CH3 CH3 I 10. CH3 – CH2 – O – - C – CH3 = 2-etoksi – 2- metil propana I CH3
- 17. ETER / ALKOKSI ALKANA B. TATA NAMA TRIVIAL 1. CH3 – O – CH3 = Dimetil - eter 2. CH3 – O – CH2 – CH3 = Metil – etil - eter 3. CH3 – O – CH2 – CH2 – CH3 = Metil – propil - eter 4. CH3 – O – CH –CH3 = Metil – isopropil - eter I CH3 5. CH3 - CH2– O – CH –CH3 = Etil – isopropil - eter I CH3
- 18. ETER / ALKOKSI ALKANA B. TATA NAMA TRIVIAL 6. CH3 – O – CH –CH2- CH3 = Metil – sek-butil - eter I CH3 CH3 I 7. CH3 - CH2 – O – C –CH3 = Etil – ters- butil - eter I CH3 CH3 I 8. CH3 - CH2 – O – C –CH2- CH3 = Etil – ters- amil - eter I CH3
- 19. ETER / ALKOKSI ALKANA 3. SIFAT – SIFAT ETER A. SIFAT FISIK 1. Zat cair, mudah menguap, titik didih rendah, mudah terbakar dan bersifat anestetis 2. Tidak campur dengan air B. SIFAT KIMIA 1. Tidak bereaksi dengan logam Na 2. Bereaksi dengan asam Iodida 3. Bereaksi dengan PCl5 4. Tidak bereaksi dengan asam karboksilat
- 20. ETER / ALKOKSI ALKANA 4. REAKSI-REAKSI ETER 1. R – O – R + PCl5 ïƒ 2R – Cl + POCl3 2. R – O – R + HI ïƒ R – I + R – OH 3. R – O – R’ + 2 HI ïƒ R – I + R’ – I + H2O 4. R – ONa + R – X ïƒ R – O – R + NaX
- 21. ETER / ALKOKSI ALKANA 5. PEMBUATAN ETER 1. Dehidrasi alkohol ( pada suhu 140 oC ) CH3-CH2-OH + H2SO4 ïƒ CH3 – CH2 – O – CH2 - CH3 + H2O 2. Sintesis Williamsons CH3-CH2-ONa + CH3Cl ïƒ CH3 –CH2 - O – CH3 + NaCl
- 22. ETER / ALKOKSI ALKANA 1. Metil propil eter Digunakan sebagai zat anestesi ( bius ) 2. Dimetil eter Berbentuk gas digunakan untuk gas aerosol 3. Eter Rantai Panjang Zat pelarut cat pernis dan lak karena sifatnya non polar maka digunakan sebagi pelarut lemak atau minyak 4. MTBE ( Metil Tersier Butil Eter ) Digunakan zat anti ketukan pada jenis bensin non premium ( seperti pertamax ) APLIKASI
- 23. ETER / ALKOKSI ALKANA LATIHAN SOAL A. Tuliskan rumus struktur senyawa eter berikut ini ! 1. Metoksi - etana 2. 2-Metoksi - propana 3. 1-etoksi – propana 4. 2-etoksi – butana CH3 – O – CH2 – CH3 Jawab : CH3 – O – CH – CH3 I CH3 Jawab : CH3 – CH2 – O – CH2 – CH2 - CH3 Jawab : CH3–CH2 –O–CH – CH2 - CH3 I CH3 Jawab :
- 24. ETER / ALKOKSI ALKANA B. TATA NAMA TRIVIAL 6. CH3 – O – CH –CH2- CH3 = Metil – sek-butil - eter I CH3 CH3 I 7. CH3 - CH2 – O – C –CH3 = Etil – ters- butil - eter I CH3 CH3 I 8. CH3 - CH2 – O – C –CH2- CH3 = Etil – ters- amil - eter I CH3
- 25. ETER / ALKOKSI ALKANA 3. SIFAT – SIFAT ETER A. SIFAT FISIK 1. Zat cair, mudah menguap, titik didih rendah, mudah terbakar dan bersifat anestetis 2. Tidak campur dengan air B. SIFAT KIMIA 1. Tidak bereaksi dengan logam Na 2. Bereaksi dengan asam Iodida 3. Bereaksi dengan PCl5 4. Tidak bereaksi dengan asam karboksilat
- 26. ETER / ALKOKSI ALKANA 5. PEMBUATAN ETER 1. Dehidrasi alkohol ( pada suhu 140 oC ) CH3-CH2-OH + H2SO4 ïƒ CH3 – CH2 – O – CH2 - CH3 + H2O 2. Sintesis Williamsons CH3-CH2-ONa + CH3Cl ïƒ CH3 –CH2 - O – CH3 + NaCl
- 27. ETER / ALKOKSI ALKANA 1. Metil propil eter Digunakan sebagai zat anestesi ( bius ) 2. Dimetil eter Berbentuk gas digunakan untuk gas aerosol 3. Eter Rantai Panjang Zat pelarut cat pernis dan lak karena sifatnya non polar maka digunakan sebagi pelarut lemak atau minyak 4. MTBE ( Metil Tersier Butil Eter ) Digunakan zat anti ketukan pada jenis bensin non premium ( seperti pertamax ) APLIKASI
- 28. ETER / ALKOKSI ALKANA LATIHAN SOAL A. Tuliskan rumus struktur senyawa eter berikut ini ! 1. Metoksi - etana 2. 2-Metoksi - propana 3. 1-etoksi – propana 4. 2-etoksi – butana CH3 – O – CH2 – CH3 Jawab : CH3 – O – CH – CH3 I CH3 Jawab : CH3 – CH2 – O – CH2 – CH2 - CH3 Jawab : CH3–CH2 –O–CH – CH2 - CH3 I CH3 Jawab :
- 29. ETER / ALKOKSI ALKANA LATIHAN SOAL B. Tuliskan nama dari rumus struktur senyawa eter berikut ini ! 2 – metoksi - butana Jawab : 1. CH3 – O – CH – CH3 I CH2 - CH3 2. CH3 – CH2 - O – CH – CH3 I CH3 – CH – CH3 2 – etoksi – 3 – metil butana Jawab :
- 30. ETER / ALKOKSI ALKANA LATIHAN SOAL B. Tuliskan nama dari rumus struktur senyawa eter berikut ini ! 2 – metoksi – 2- metil propana Jawab : CH3 I 3. CH3 – O – C – CH3 I CH3 2. CH3 – CH2 - O – CH2 I CH3 - CH2 – CH – CH3 1 – etoksi – 2 – metil butana Jawab :
- 31. ETER / ALKOKSI ALKANA LATIHAN SOAL C. Tuliskan hasil reaksi senyawa eter berikut ini ! ïƒ CH3 – OH + CH3 - I Jawab : ïƒ 2 CH3- Cl + POCl3 Jawab : 1. CH3 – O – CH3 + HI ïƒ 2. CH3 – O – CH3 + PCl5 ïƒ 3. CH3 – CH2 - OH + H2SO4 (Suhu 140oC ) ïƒ ïƒ CH3 - CH2 – O – CH2 – CH3 + H2O Jawab : 4. CH3-CH2-ONa + CH3Cl ïƒ ïƒ CH3 – CH2 – O – CH3 + NaCl Jawab :
- 32. Reaksi pada eter 1. Tidak bereaksi dengan logam Na dan PCl3 sehingga dapat digunakan untuk membedakan alkohol dan eter. R-O-R + Na R-O-R + PCl3 2. Bereaksi dengan PCl5 membentuk Alkil klorida tanpa menghasilkan HCl karena itu dapat digunakan untuk membedakan alkohol dan eter. R-O-R’ + PCl5 R-Cl + R’-Cl + POCl3 3. Bereaksi dengan asam halida HX (X= F, Cl, Br, I) membentuk alkohol dan alkil halida. R-O-R + HX R-OH + RX 4. Bereaksi dengan HI berlebih dan pemanasan membentuk alkil iodida (RI) dan H2O. R-O-R’ + HI R-I + R’-I + H2O
- 33. ETER / ALKOKSI ALKANA EVALUASI A. Etoksi propana 2. Senyawa CH3 - CH2 – O – CH2 – CH(CH3) – CH3 mempunyai nama …. BENAR ! B. 1- etoksi - isobutana C. 2 – etoksi - butana D. Etoksi - isopropana E. Etoksi - etana
- 34. ETER / ALKOKSI ALKANA EVALUASI A. CH3 – O – (CH2)3 – CH3 3. Senyawa MTBE ( metil tersier butil eter ) mempunyai rumus struktur …. B. CH3 - CH2- O - C(CH3)3 C. CH3 – O – CH2 – CH(CH3)2 D. CH3 – O – CH(CH3) - CH3 BENAR ! E. CH3 – O – C(CH3)3
- 35. ETER / ALKOKSI ALKANA EVALUASI BENAR ! A. 2- etoksi – ters - butana 4. Senyawa CH3 - CH2 – O – C(CH3)2 – CH3 mempunyai nama …. B. 2- etoksi - isobutana C. 2 – etoksi – sek - butana D. 2- etoksi - butana E. 2- etoksi - pentana
- 36. ETER / ALKOKSI ALKANA EVALUASI BENAR ! A. isopropiL– ters – butil - eter 5. Senyawa CH3 – CH(CH3) – O – C(CH3)3 mempunyai nama …. B. isopropoksi – isobutil - eter C. isopropoksi–sek–butil-eter D. propil – butil - eter E. propil – isobutil - eter
- 37. ETER / ALKOKSI ALKANA EVALUASI BENAR ! A. dietil - eter 6. Reaksi antara etanol dengan asam sulfat pada suhu 140oC akan menghasilkan senyawa air dan …. B. dimetil – eter C. etanal D. asam etanoat E. etil etanoat
- 38. ETER / ALKOKSI ALKANA EVALUASI 7. Berikut ini merupakan sifat – sifat dari eter …. A. Mempunyai TD tinggi BENAR ! B. Mudah terbakar C. Bereaksi dengan logam Na D. Campur dengan air E. Sukar menguap
- 39. ETER / ALKOKSI ALKANA EVALUASI BENAR ! A. Metil – ters - butil - eter 8. Senyawa berikut ini yang digunakan untuk mengurangi ketukan pada jenis bensin non premium adalah …. B. 2- Etoksi - isobutana C. 2- Etoksi – sek - butana D. 2- etoksi - butana E. 2- etoksi - pentana
- 40. ETER / ALKOKSI ALKANA EVALUASI 9. Pembuatan eter dengan sintesis Wiliamsons dari senyawa : CH3-CH2-ONa + CH3Cl ïƒ â€¦ + NaCl A. CH3 - CH2 - CHO BENAR ! B. CH3 –CH2 - O – CH3 C. CH3 - CH2 - COOH D. CH3 – CO – CH3 E. CH3 – COO – CH3
- 41. EVALUASI 10. Reaksi antara CH3 - CH2 – O – CH3 dengan HI akan menghasilkan CH3 – I dan …. A. CH3 - CHO BENAR ! B. CH3 – CH2 - OH C. CH3 – COOH D. CH3- COO – CH3 E. CH3- CO –CH3