[123doc.vn] tong-hop-cach-nhan-biet-mot-so-cation-anion-khi-va-bai-tap-trac-nghiem-nhan-biet-pps
- 1.  HOÙA HOÏC 12- Chöông trình chuaån vaø naâng cao Naêm Hoïc 2008 – 2009 (Hoïc Kyø II) TỔNG HỢP CÁCH NHẬN BIẾT MỘT SỐ CATION- ANION- KHÍ VÀ BÀI TẬP TRẮC NGHIỆM NHẬN BIẾT I. PHÂN BIỆT một số ion trong dung dịch : Nguyên Tắc : Người ta thêm vào dung dịch một thuốc thử tạo với ion đó một sản phẩm đặc trưng như : một chất kết tủa, một hợp chất có màu hoặc một chất khí khó tan sủi bọt, bay khỏi dung dịch. NHẬN BIẾT ION DƯƠNG (CATION) CATION Thuốc thử Hiện tượng Giải thích Li+ Đốt cháy hợp chất trên ngọn lửa vô sắc Ngọn lửa màu đỏ thẫm Na+ Ngọn lửa màu vàng tươi K+ Ngọn lửa màu tím hồng Ca2+ Ngọn lửa màu đỏ da cam Ba2+ Ngọn lửa màu lục (hơi vàng) NH+ 4 Dung dịch kiềm (OH- ) Có khí mùi khai thoát ra làm xanh quì tím NH4 + + OH- → NH3 ↑ + H2O. Ba2+ dd H2SO4 loãng Tạo kết tủa trắng không tan trong thuốc thử dư. Ba2+ + SO4 2- → BaSO4 ↓ dd K2CrO4 hoặc K2Cr2O7 - Tạo kết tủa màu vàng tươi. Ba2+ + CrO4 2- → BaCrO4 ↓ Ba2+ + Cr2O7 2- + H2O → BaCrO4 ↓ + 2H+ Al3+ Cr3+ Dung dịch kiềm (OH- ) tạo kết tủa sau đó kết tan trong kiềm dư Al3+ + 3 OH- → Al(OH)3 ↓ trắng Al(OH)3 + OH- → [Al(OH)4] trong suốt Cr3+ + 3 OH- → Cr(OH)3 ↓ xanh Cr(OH)3 + OH- → [Cr(OH)4] xanh Fe3+ 1. dd chứa ion thioxianat SCN- tạo ion phức có màu đỏ máu Fe3+ + SCN- → Fe(SCN)3 (màu đỏ máu) 2. dung dịch kiềm tạo kết tủa màu nâu đỏ tạo kết tủa màu nâu đỏ Fe2+ 1.dung dịch kiềm tạo kết tủa trắng xanh, kết tủa chuyễn sang màu nâu đỏ khi tiếp xúc với không khí Fe2+ + 2OH- →Fe(OH)2 ↓ trắng 4Fe(OH)2 +2H2O+ O2 → 4 Fe(OH)3 ↓ nâu đỏ 2. Dung dịch thuốc tím làm mất màu dung dịch thuốc tím trong H+ 5Fe2+ + MnO4 - + 8H+ → Mn2+ + 5Fe3+ + 4H2O Ag+ HCl, HBr, HI AgCl ↓ trắng AgBr ↓ vàng nhạt AgI ↓ vàng đậm Ag+ + Cl− → AgCl ↓ Ag+ + Br− → AgBr ↓ Ag+ + I− → AgI ↓ Pb2+ dd KI PbI2 ↓ vàng Pb2+ + 2I− → PbI2 ↓ GV. Thaân Troïng Tuaán Taøi lieäu oân thi Toát Nghieäp THPT vaø Ñaïi Hoïc Trang 1
- 2.  HOÙA HOÏC 12- Chöông trình chuaån vaø naâng cao Naêm Hoïc 2008 – 2009 (Hoïc Kyø II) Hg2+ HgI2 ↓ đỏ Hg2+ + 2I− → HgI2 ↓ Pb2+ Na2S, H2S PbS ↓ đen Pb2+ + S2− → PbS ↓ Hg2+ HgS ↓ đỏ Hg2+ + S2− → HgS ↓ Cd2+ CdS ↓ vàng Cd2+ + S2− → CdS ↓ Zn2+ dd NH3 ↓ xanh, tan trong dd NH3 dư Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2 Ag+ ↓ trắng, tan trong dd NH3 dư AgOH + 2NH3 → [Cu(NH3)2]OH Mg2+ dd Kiềm( NaOH) ↓ trắng Mg2+ + 2OH− → Mn(OH)2 ↓ Zn2+ ↓ trắng tan trong kiềm dư Zn2+ + 2OH− → Zn(OH)2 ↓ Zn(OH)2 + 2OH− → 2 2 ZnO − + 2H2O Be2+ Be2+ + 2OH− → Be(OH)2 ↓ Be(OH)2 + 2OH− → 2 2 BeO − + 2H2O Pb2+ Pb2+ + 2OH− → Pb(OH)2 ↓ Pb(OH)2 + 2OH− → 2 2 PbO − + 2H2O NHẬN BIẾT ION ÂM (ANION) ANION Thuốc thử Hiện tượng Giải Thích NO3 - Cu, H2SO4 l tạo dd màu xanh, có khí không màu (NO) dễ hóa nâu trong không khí (NO2). 3Cu + 8H+ +2NO3 - → 3Cu2+ + 2NO+4H2O 2NO + O2 → 2NO2 màu nâu đỏ SO4 2- dd BaCl2 trong môi trường axit loãng dư tạo kết tủa trắng không tan trong axit Ba2+ + SO4 2- → BaSO4 ↓ trắng Cl- dd AgCl trong môi trường HNO3loãngdư tạo kết tủa trắng không tan trong axit Ag+ + Cl- → AgCl ↓ trắng CO3 2- Dung dịch axit và nước vôi trong tạo ra khí làm đục nước vôi trong CO3 2- + 2H+ → CO2 + H2O CO2 + Ca(OH)2 → CaCO3 ↓trắng + H2O. OH - Quì tím Hóa xanh Br - AgNO3 ↓ vàng nhạt Br− + Ag+ → AgBr↓ (hóa đen ngoài ánh sáng) I - ↓ vàng đậm I− + Ag+ → AgI↓ (hóa đen ngoài ánh sáng) PO4 3- ↓ vàng 3 4 PO − + 3Ag+ → Ag3PO4↓ S 2- ↓ đen S2− + 2Ag+ → Ag2S↓ CO3 2- BaCl2 ↓ trắng 2 3 CO − + Ba2+ → BaCO3↓ (tan trong HCl) SO3 2- ↓ trắng 2 3 SO − + Ba2+ → BaSO3↓ (tan trong HCl) 2 4 CrO − ↓ vàng 2 4 CrO − + Ba2+ → BaCrO4↓ S2− Pb(NO3)2 ↓ đen S2− + Pb2+ → PbS↓ GV. Thaân Troïng Tuaán Taøi lieäu oân thi Toát Nghieäp THPT vaø Ñaïi Hoïc Trang 2
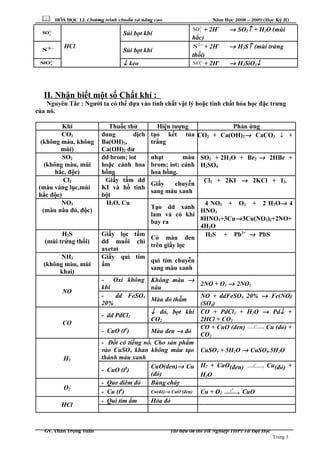
- 3.  HOÙA HOÏC 12- Chöông trình chuaån vaø naâng cao Naêm Hoïc 2008 – 2009 (Hoïc Kyø II) 2 3 SO − HCl Sủi bọt khí 2 3 SO − + 2H+ → SO2↑ + H2O (mùi hắc) S2− Sủi bọt khí 2 S − + 2H+ → H2S↑ (mùi trứng thối) 2 3 SiO − ↓ keo 2 3 SiO − + 2H+ → H2SiO3↓ II. Nhận biết một số Chất khí : Nguyên Tắc : Người ta có thể dựa vào tính chất vật lý hoặc tính chất hóa học đặc trưng của nó. Khí Thuốc thử Hiện tượng Phản ứng CO2 (không màu, không mùi) dung dịch Ba(OH)2, Ca(OH)2 dư tạo kết tủa trắng CO2 + Ca(OH)2→ CaCO3 ↓ + SO2 (không màu, mùi hắc, độc) dd brom; iot hoặc cánh hoa hồng nhạt màu brom; iot; cánh hoa hồng. SO2 + 2H2O + Br2 → 2HBr + H2SO4 Cl2 (màu vàng lục,mùi hắc độc) Giấy tẩm dd KI và hồ tinh bột Giấy chuyễn sang màu xanh Cl2 + 2KI → 2KCl + I2. NO2 (màu nâu đỏ, độc) H2O, Cu Tạo dd xanh lam và có khí bay ra 4 NO2 + O2 + 2 H2O→ 4 HNO3 8HNO3+3Cu→3Cu(NO3)2+2NO+ 4H2O H2S (mùi trứng thối) Giấy lọc tẩm dd muối chì axetat Có màu đen trên giấy lọc H2S + Pb2+ → PbS NH3 (không màu, mùi khai) Giấy quì tím ẩm quì tím chuyễn sang màu xanh NO - Oxi không khí Không màu → nâu 2NO + O2 → 2NO2 - dd FeSO4 20% Màu đỏ thẫm NO + ddFeSO4 20% → Fe(NO) (SO4) CO - dd PdCl2 ↓ đỏ, bọt khí CO2 CO + PdCl2 + H2O → Pd↓ + 2HCl + CO2 - CuO (t0 ) Màu đen → đỏ CO + CuO (đen) 0 t →Cu (đỏ) + CO2 H2 - Đốt có tiếng nổ. Cho sản phẩm vào CuSO4 khan không màu tạo thành màu xanh CuSO4 + 5H2O → CuSO4.5H2O - CuO (t0 ) CuO(đen)→ Cu (đỏ) H2 + CuO(đen) 0 t → Cu(đỏ) + H2O O2 - Que diêm đỏ Bùng cháy - Cu (t0 ) Cu(đỏ)→ CuO (đen) Cu + O2 0 t → CuO HCl - Quì tím ẩm Hóa đỏ GV. Thaân Troïng Tuaán Taøi lieäu oân thi Toát Nghieäp THPT vaø Ñaïi Hoïc Trang 3
- 4.  HOÙA HOÏC 12- Chöông trình chuaån vaø naâng cao Naêm Hoïc 2008 – 2009 (Hoïc Kyø II) BÀI TẬP TỰ LUẬN PHÂN BIỆT CÁC CHẤT VÔ CƠ 1. Có 3 dung dịch , mỗi dung dịch chứa 1 Cation : Ba2+ , NH4 + , Al3+ . Trình bày cách nhận biết chúng. 2. Có 3 dung dịch , mỗi dung dịch chứa 1 Cation : Ba2+ , Fe3+ , Cu2+ . Trình bày cách nhận biết chúng. 3. Có 2 dung dịch riêng rẽ chứa các anion : NO3 2- , SO4 2- . Hãy nêu cách nhận biết từng ion trong dung dịch đó. 4. Dung dịch A chứa đồng thời các Cation Fe2+ , Al3+ , Cu2+ . Trình bày cách tách và nhận biết mỗi ion từ dd A. 5. Một dung dịch chứa đồng thời các Cation Ba2+ , NH4 + , Cr3+ . Trình bày cách nhận biết sự có mặt của từng Cation trongdung dịch. 6. Một dung dịch chứa đồng thời các Cation Ca2+ , Al3+ , Fe3+ . Trình bày cách nhận biết sự có mặt của từng Cation trongdung dịch. 7. Một dung dịch chứa đồng thời các Cation Ni2+ , Al3+ , Fe3+ . Trình bày cách nhận biết sự có mặt của từng Cation trongdung dịch 8. Dung dịch chứa Na+ , NH4 + , HCO3 - , CO3 2- và SO4 2- . Chỉ dùng HCl, BaCl2 với các ống nghiệm, đèn cồn phểu lọc thì có thể nhận ra được những ion nào? 9.Dung dÞch A chøa c¸c ion Na+ , SO4 2- , SO3 2- , CO3 2- , NO3 - . B»ng nh÷ng ph¶n øng ho¸ häc nµo cã thÓ nhËn biÕt tõng lo¹i anion cã trong dungdÞch.' 10 Cã 4 dung dÞch trong suèt. Mçi dung dÞch chøa mét lo¹i ion ©m vµ mét lo¹i ion d¬ng trong c¸c ion sau:Ba2+ , Mg2+ , Pb2+ , Na+ , SO4 2- , Cl- , CO3 2- , NO3 - . a. T×m c¸c dung dÞch. b. NhËn biÕt tõng dung dÞch b»ng ph¬ng ph¸p ho¸ häc. 11. Chỉ dùng một thuốc thử, hãy phân biệt các khí đựng trong các lọ bị mất nhãn: a) CO2 và SO2 b) Cl2 và SO2 c) H2S và NH3 12. Có hỗn hợp khí gồm : CO2, SO2, H2 . Hãy chứng minh trong hỗn hợp có mặt từng khí 13. Bằng phương pháp hóa học nhận biết các khí trong các lọ mất nhãn sau: a. N2, Cl2, SO2, CO2. b. CO, CO2, SO2, SO3, H2 BÀI TẬP TRẮC NGHIỆM KHÁCH QUAN Câu 1: Nguyên tắc nhận biết một ion trong dung dịch là dùng A. phương pháp đốt nóng thử màu ngọn lửa. B. phương pháp nhiệt phân để tạo kết tủa. C. thuốc thử để tạo với ion một sản phẩm kết tủa, bay hơi hoặc có sự thay đổi màu. D. phương pháp thích hợp để tạo ra sự biến đổi về trạng thái, màu sắc từ các ion trong dung dịch. Câu 2: Để nhận biết ion Fe2+ không dùng ion A. OH- /không khí . B. NH3/không khí. C. SCN- . D. MnO4 - . Câu 3: Để nhận biết ion Ba2+ không dùng ion A. SO4 2- . B. S2- . C. CrO4 2- . D. Cr2O7 2- . Câu 4: Để phận biệt Fe2+ và Fe3+ không dùng thuốc thử A. NH3. B. NaSCN. C. KMnO4/H2SO4. D. H2SO4 (loãng). GV. Thaân Troïng Tuaán Taøi lieäu oân thi Toát Nghieäp THPT vaø Ñaïi Hoïc Trang 4
- 5.  HOÙA HOÏC 12- Chöông trình chuaån vaø naâng cao Naêm Hoïc 2008 – 2009 (Hoïc Kyø II) Câu 5: Để phận biệt Al3+ và Zn2+ không dùng thuốc thử A. NH3. B. NaOH. C. Na2CO3. D. Na2S. Câu 6: Để nhận biết sự có mặt của các ion Al3+ , Cu2+ , Fe3+ , Zn2+ trong dung dịch bằng phương pháp hóa học, cần dùng ít nhất mấy phản ứng? A. 6 B. 5 C. 4 D. 3 Câu 7: Cho các ion Na+ , K+ , NH4 + , Ba2+ , Al3+ , Ca2+ . Số ion có thể nhận biết bằng thử màu ngọn lửa là A. 2 B. 3 C. 4 D. 5 Câu 8: Có 5 mẫu kim loại: Ba, Mg, Al, Fe, Ag. Để nhận ra kim loại Fe, số hiện tượng tối thiểu quan sát được là A. 2. B. 3. C. 4. D. 5. Câu 9: Cho các chất bột Al, Mg, Fe, Cu. Để phân biệt các chất bột trên chỉ cần dùng ít nhất mấy thuốc thử? A. 3 B. 2 C. 4 D. 5 Câu 10: Có 5 mẫu kim loại: Ba, Mg, Al, Fe, Ag. Chỉ dùng thêm dd H2SO4 loãng thì số kim loại có thể nhận ra là A. 2. B. 3. C. 4. D. 5. Câu 11: Chỉ dùng thêm chất nào sau đây có thể phân biệt được các oxit: Na2O, ZnO, CaO, MgO? A. C2H5OH. B. H2O. C. dung dịch HCl. D. dung dịch CH3COOH. Câu 12: Có 6 gói bột: CuO, FeO, Fe3O4, MnO2, Ag2O và Fe + FeO. Chỉ dùng thêm dung dịch HCl, có thể nhận ra được số gói đựng từng chất là A. 6. B. 5. C. 4. D. 3. Câu13:Có 6 gói bột:CuO,FeO,Fe3O4,MnO2,Ag2Ovà Fe+FeO.Để nhận ra từng gói bột, cần quan sát các hiện tượng A. sự tạo khí. B. sự tạo kết tủa. C. màu của sản phẩm. D. cả A, B, C. Câu 14: Có 2 dung dịch AlCl3 và NaOH. Cách nào sau đây không nhận ra được từng dung dịch ? A. Đổ từ từ dung dịch AlCl3 vào dung dịch NaOH. B. Cho từ từ dung dịch tác dụng với NH3. C. Cho từng dung dịch tác dụng với dung dịch Na2CO3. D. Cho từng dung dịch tác dụng với H2SO4. Câu 15: Cho các dung dịch axit HCl, HNO3, H2SO4 và H3PO4 có thể dùng A. bột Cu. B. dung dịch AgNO3. C. bột Cu và dd AgNO3. D. Cu và CaCl2. Câu 20: Để phân biệt 3 dung dịch riêng biệt KCl, (NH4)2SO4, NH4Cl có thể dùng A. dung dịch AgNO3.B. dung dịch NaOH. C. dung dịch Ca(OH)2. D. dung dịch Ca(OH)2. Câu 21: Có các dd AlCl3, ZnSO4, FeSO4. Chỉ cần dùng thuốc thử nào sau đây có thể phân biệt được các dd trên? A. Quì tím. B. Dung dịch NH3. C. Dung dịch NaOH.D. Dung dịch BaCl2. GV. Thaân Troïng Tuaán Taøi lieäu oân thi Toát Nghieäp THPT vaø Ñaïi Hoïc Trang 5
- 6.  HOÙA HOÏC 12- Chöông trình chuaån vaø naâng cao Naêm Hoïc 2008 – 2009 (Hoïc Kyø II) Câu 22: Dùng thuốc thử nào sau đây có thể phân biệt được dd Fe2(SO4)3 và dd Fe2(SO4)3 có lẫn FeSO4? A. Dung dịch KMnO4/H2SO4. B. Dung dịch NaOH. C. Dung dịch NH3. D. Dung dịch Ba(OH)2. Câu 23: Có 2 dung dịch HCl và Na2CO3. Cách nào sau đây không xác định được từng dung dịch ? A. Đổ từ từ dung dịch này vào dung dịch kia. B. Cho từng dung dịch tác dụng với dung dịch CaCl2. C. Cho từng dung dịch tác dụng với dung dịch FeCl3. D. Cho từng dung dịch tác dụng với dung dịch AgNO3 Câu 24: (trang 233-SGK– Nâng cao) Có 5 dd riêng rẽ, mỗi dd chứa một cation sau đây: NH4 + , Mg2+ , Fe2+ , Fe3+ , Al3+ (nồng độ khoảng 0,1M). Dùng dd NaOH cho lần lượt vào từng dd trên, có thể nhận biết tối đa được mấy dd? A. 2 dung dịch B. 3 dung dịch C. 1 dung dịch D. 5 dung dịch Câu 25: (trang 233 –SGK– Nâng cao). Có 5 lọ chứa hoá chất mất nhãn, mỗi lọ đựng một trong các dd chứa cation sau (nồng độ mỗi dd khoảng 0,01M): Fe2+ , Cu2+ , Ag+ , Al3+ , Fe3+ . Chỉ dùng một dd thuốc thử KOH có thể nhận biết được tối đa mấy dung dịch? A. 2 dung dịch B. 3 dung dịch C. 1 dung dịch D. 5 dung dịch Câu 26: (trang 236 –SGK– Nâng cao) Có 5 dung dịch hoá chất không nhãn, mỗi dung dịch nồng độ khoảng 0,1M của một trong các muối sau: KCl, Ba(HCO3)2, K2CO3, K2S, K2SO3. Chỉ dùng một dung dịch thuốc thử là dung dịch H2SO4 loãng nhỏ trực tiếp vào mỗi dung dịch thì có thể phân biệt tối đa mấy dung dịch? A. 1 dung dịch. B. 2 dung dịch. C. 3 dung dịch. D. 5 dung dịch. Câu 27: Cho các dung dịch mất nhãn: Al(NO3)3, Zn(NO3)2, NaCl, MgCl2. Có các thuốc thử sau : dd NaOH (1); dd NH3 (2); dd Na2CO3 (3); dd AgNO3 (4). Để nhận ra từng dd, có thể sử dụng các thuốc thử trên theo thứ tự A. (1) (lấy dư). B. (2) (lấy dư), (1). C. (3), (1). D. (4), (3). Câu 28: Có 4 dung dịch riêng biệt AlCl3, KNO3, Na2CO3, NH4Cl. Thuốc thử có thể dùng để phân biệt 4 dd trên là A. dung dịch Ba(OH)2. B. dung dịch NaOH. C. dung dịch H2SO4. D. dung dịch Ca(OH)2. Câu 29:Có 5 lọ mất nhãn đựng các dd: NaNO3, CuCl2, FeCl2, AlCl3, NH4Cl. dùng dd nào để nhận biết các dd trên A. Dung dịch NaOH.B. Dung dịch AgNO3. C. Dung dịch H2SO4. D. Dung dịch Na2CO3. Câu30:Có 5 lọ đựng từng dd NaHSO4, KHCO3, Na2SO3, Ba(HCO3)2, NaCl.Bằng cách đun nóng có thể nhận ra dd A. KHCO3. B. NaHSO4. C. Na2SO3. D. Ba(HCO3)2. Câu 31: Có 5 ống nghiệm đựng riêng rẽ từng dung dịch NaHSO4, KHCO3, Na2SO3, Ba(HCO3)2, NaCl. Bằng dung dịch Ba(HCO3)2 có thể nhận ra được dung dịch A. NaHSO4. B. Na2SO3. C. KHCO3. D. NaHSO4 và Na2SO3. Câu 32: Để nhận biết các dung dịch riêng biệt NH4HSO4, Ba(OH)2, BaCl2, HCl, NaCl, H2SO4 . có thể dùng thêm A. dung dịch HNO3. B. dung dịch Ca(OH)2. C. dung dịch AgNO3.D. giấy quì tím. GV. Thaân Troïng Tuaán Taøi lieäu oân thi Toát Nghieäp THPT vaø Ñaïi Hoïc Trang 6
- 7.  HOÙA HOÏC 12- Chöông trình chuaån vaø naâng cao Naêm Hoïc 2008 – 2009 (Hoïc Kyø II) Câu 33: Có 5 dung dịch chứa từng chất riêng rẽ sau: BaCl2, Ba(HCO3)2, K2SO3, K2S, KCl. Người ta cho từng dung dịch tác dụng với thuốc thử H2SO4 loãng thì có các hiện tượng sau : - không có hiện tượng gì. - tạo kết tủa. - tạo khí không màu. - tạo khí làm mất màu dung dịch brom. - tạo khí, khí tạo kết tủa với dung dịch CuCl2. Hiện tượng xác định Ba(HCO3)2 là A. tạo kết tủa B. tạo khí không màu C. tạo khí, tạo kết tủa với dd CuCl2 D. tạo kết tủa và khí không màu Câu 34: Có 5 dung dịch chứa từng chất riêng rẽ sau: BaCl2, Ba(HCO3)2, K2SO3, K2S, KCl. Người ta cho từng dung dịch tác dụng với thuốc thử H2SO4 loãng thì có các hiện tượng sau - không có hiện tượng gì. - tạo kết tủa. - tạo khí không màu. - tạo khí làm mất màu dung dịch brom. - tạo khí, khí tạo kết tủa với dung dịch CuCl2. Số chất tối đa có thể phân biệt được là A. 2. B. 3. C. 4. D. 5. Câu 35: Cho 5 dung dịch riêng rẽ, mỗi dung dịch chứa 1 cation trong số: Al3 , Fe3+ , Zn2+ , Cu2+ . Có thể nhận ra cation Zn2+ bằng 1 dung dịch với hiện tượng quan sát được là A. tạo kết tủa, sau đó kết tủa tan trong thuốc thử dư. B. tạo kết tủa màu trắng. C. tạo kết tủa, kết tủa tan trong thuốc thử dư thành dung dịch không màu. D. tạo kết tủa, kết tủa tan trong thuốc thử dư thành dung dịch không màu. Câu 36: Cho 5 dung dịch riêng rẽ, mỗi dung dịch chứa 1 cation trong số: NH4 + , Mg2+ , Fe2+ , Fe3+ , Zn2+ . Có thể nhận ra từng cation bằng 1 dung dịch (trong điều kiện không có không khí), hiện tượng là A. tạo khí và tạo kết tủa. B. tạo các kết tủa có màu khcá nhau. C. tạo kết tủa có màu khác nhau trong không khí và khả năng tan trong thuốc thử dư khác nhau. D. tạo khí, tạo kết tủa có màu khác nhau và khả năng tan trong thuốc thử dư khác nhau. Câu 37: Để phận biệt CO2 và SO2 không dùng thuốc thử A. Dung dịch Br2. B. Dung dịch I2 C. Dung dịch nước vôi. D. Dung dịch H2S. Câu 38: Để phân biệt các khí riêng biệt NH3, CO2, O2, H2S có thể dùng A. nước và giấy quì tím. B. dung dịch Ca(OH)2 và giấy quì tím. C. giấy quì tím ẩm và tàn đóm cháy dở. D. giấy quì tím và giấy tẩm dung dịch Pb(NO3)2. Câu 39: Có 4 dd chứa riêng rẽ từng chất: AlCl3, CrCl3, ZnCl2, MgCl2. Để nhận ra từng dd làm các thí nghiệm : (1) Cho tác dụng với dung dịch nước brom. (2) Cho tác dụng với dung dịch NaOH tới dư. (3) Cho tác dụng với dung dịch NH3 từ từ đến dư. GV. Thaân Troïng Tuaán Taøi lieäu oân thi Toát Nghieäp THPT vaø Ñaïi Hoïc Trang 7
- 8.  HOÙA HOÏC 12- Chöông trình chuaån vaø naâng cao Naêm Hoïc 2008 – 2009 (Hoïc Kyø II) Thứ tự thí nghiệm để xác định được dung dịch CrCl3 là A. 1, 2. 3. B. 2, 1. C. 2, 3, 1. D. 3, 2, 1. Câu 40 (trang 239 – SGK– Nâng cao ) Khí CO2 có lẫn tạp chất là khí HCl. Để loại trừ tạp chất HCl đó nên cho khí CO2 đi qua dung dịch nào sau đây là tốt nhất? A. Dung dịch NaOH dư. B. Dung dịch NaHCO3 bão hoà dư. C. Dung dịch Na2CO3 dư. D. Dung dịch AgNO3 dư. GV. Thaân Troïng Tuaán Taøi lieäu oân thi Toát Nghieäp THPT vaø Ñaïi Hoïc Trang 8
![ HOÙA HOÏC 12- Chöông trình chuaån vaø naâng cao Naêm Hoïc 2008 – 2009 (Hoïc Kyø II)
TỔNG HỢP CÁCH NHẬN BIẾT MỘT SỐ CATION- ANION- KHÍ
VÀ BÀI TẬP TRẮC NGHIỆM NHẬN BIẾT
I. PHÂN BIỆT một số ion trong dung dịch :
Nguyên Tắc : Người ta thêm vào dung dịch một thuốc thử tạo với ion đó một sản phẩm
đặc trưng như : một chất kết tủa, một hợp chất có màu hoặc một chất khí khó tan sủi bọt, bay
khỏi dung dịch.
NHẬN BIẾT ION DƯƠNG (CATION)
CATION Thuốc thử Hiện tượng Giải thích
Li+
Đốt cháy hợp
chất trên ngọn
lửa vô sắc
Ngọn lửa màu đỏ thẫm
Na+ Ngọn lửa màu vàng
t∆∞∆°i
K+ Ngọn lửa màu tím
hồng
Ca2+ Ngọn lửa màu đỏ da
cam
Ba2+ Ngọn lửa màu lục (hơi
vàng)
NH+
4
Dung dịch
kiềm (OH-
)
Có khí mùi khai thoát
ra làm xanh quì tím
NH4
+
+ OH-
‚Üí NH3 ‚Üë +
H2O.
Ba2+
dd H2SO4
lo√£ng
Tạo kết tủa trắng
không tan trong thuốc
thử dư.
Ba2+
+ SO4
2-
‚Üí BaSO4 ‚Üì
dd K2CrO4
ho·∫∑c K2Cr2O7
- Tạo kết tủa màu
vàng tươi.
Ba2+
+ CrO4
2-
‚Üí BaCrO4 ‚Üì
Ba2+
+ Cr2O7
2-
+ H2O ‚Üí BaCrO4 ‚Üì
+ 2H+
Al3+
Cr3+
Dung dịch
kiềm (OH-
)
tạo kết tủa sau đó kết
tan trong kiềm dư
Al3+
+ 3 OH-
‚Üí Al(OH)3 ‚Üì
trắng
Al(OH)3 + OH-
‚Üí [Al(OH)4] trong
suốt
Cr3+
+ 3 OH-
‚Üí Cr(OH)3 ‚Üì
xanh
Cr(OH)3 + OH-
‚Üí [Cr(OH)4]
xanh
Fe3+
1. dd chứa
ion thioxianat
SCN-
tạo ion phức có màu
đỏ máu
Fe3+
+ SCN-
‚Üí Fe(SCN)3
(màu đỏ
m√°u)
2. dung dịch
kiềm
tạo kết tủa màu nâu đỏ tạo kết tủa màu nâu đỏ
Fe2+
1.dung dịch
kiềm
tạo kết tủa trắng xanh,
kết tủa chuyễn sang
màu nâu đỏ khi tiếp
xúc với không khí
Fe2+
+ 2OH-
→Fe(OH)2 ↓ trắng
4Fe(OH)2 +2H2O+ O2 ‚Üí 4 Fe(OH)3
↓ nâu đỏ
2. Dung dịch
thuốc tím
làm mất màu dung
dịch thuốc tím trong
H+
5Fe2+
+ MnO4
-
+ 8H+
‚Üí Mn2+
+ 5Fe3+
+ 4H2O
Ag+ HCl, HBr, HI
AgCl ↓ trắng
AgBr ↓ vàng nhạt
AgI ↓ vàng đậm
Ag+
+ Cl‚àí
‚Üí AgCl ‚Üì
Ag+
+ Br‚àí
‚Üí AgBr ‚Üì
Ag+
+ I‚àí
‚Üí AgI ‚Üì
Pb2+
dd KI PbI2 ↓ vàng Pb2+
+ 2I‚àí
‚Üí PbI2 ‚Üì
GV. Thaân Troïng Tuaán Taøi lieäu oân thi Toát Nghieäp THPT vaø Ñaïi Hoïc
Trang 1](https://image.slidesharecdn.com/123doc-190815094752/85/123doc-vn-tong-hop-cach-nhan-biet-mot-so-cation-anion-khi-va-bai-tap-trac-nghiem-nhan-biet-pps-1-320.jpg)
2
Ag+ ↓ trắng, tan trong dd
NH3 d∆∞
AgOH + 2NH3 ‚Üí
[Cu(NH3)2]OH
Mg2+
dd
Kiềm( NaOH)
↓ trắng
Mg2+
+ 2OH‚àí
‚Üí
Mn(OH)2 ‚Üì
Zn2+
↓ trắng
tan trong kiềm dư
Zn2+
+ 2OH‚àí
‚Üí Zn(OH)2
‚Üì
Zn(OH)2 + 2OH‚àí
‚Üí 2
2
ZnO ‚àí
+ 2H2O
Be2+
Be2+
+ 2OH‚àí
‚Üí Be(OH)2
‚Üì
Be(OH)2 + 2OH‚àí
‚Üí 2
2
BeO ‚àí
+ 2H2O
Pb2+
Pb2+
+ 2OH‚àí
‚Üí Pb(OH)2
‚Üì
Pb(OH)2 + 2OH‚àí
‚Üí 2
2
PbO ‚àí
+ 2H2O
NHẬN BIẾT ION ÂM (ANION)
ANION Thuốc thử Hiện tượng Giải Thích
NO3
-
Cu, H2SO4 l
tạo dd màu xanh, có
khí không màu (NO)
dễ hóa nâu trong
không khí (NO2).
3Cu + 8H+
+2NO3
-
‚Üí 3Cu2+
+
2NO+4H2O
2NO + O2 → 2NO2 màu nâu đỏ
SO4
2- dd BaCl2 trong
môi trường axit
lo√£ng d∆∞
tạo kết tủa trắng
không tan trong axit
Ba2+
+ SO4
2-
‚Üí BaSO4 ‚Üì
trắng
Cl- dd AgCl trong
môi trường
HNO3lo√£ngd∆∞
tạo kết tủa trắng
không tan trong axit
Ag+
+ Cl-
→ AgCl ↓ trắng
CO3
2- Dung dịch axit và
nước vôi trong
tạo ra khí làm đục
nước vôi trong
CO3
2-
+ 2H+
‚Üí CO2 + H2O
CO2 + Ca(OH)2 → CaCO3 ↓trắng +
H2O.
OH -
Quì tím Hóa xanh
Br -
AgNO3
↓ vàng nhạt
Br‚àí
+ Ag+
→ AgBr↓ (hóa đen ngoài
√°nh s√°ng)
I -
↓ vàng đậm
I‚àí
+ Ag+
→ AgI↓ (hóa đen ngoài ánh
s√°ng)
PO4
3-
↓ vàng 3
4
PO ‚àí
+ 3Ag+
‚Üí Ag3PO4‚Üì
S 2-
↓ đen S2−
+ 2Ag+
‚Üí Ag2S‚Üì
CO3
2-
BaCl2
↓ trắng
2
3
CO ‚àí
+ Ba2+
‚Üí BaCO3‚Üì (tan trong
HCl)
SO3
2-
↓ trắng
2
3
SO ‚àí
+ Ba2+
‚Üí BaSO3‚Üì (tan trong
HCl)
2
4
CrO ‚àí
↓ vàng 2
4
CrO ‚àí
+ Ba2+
‚Üí BaCrO4‚Üì
S2‚àí
Pb(NO3)2 ↓ đen S2−
+ Pb2+
‚Üí PbS‚Üì
GV. Thaân Troïng Tuaán Taøi lieäu oân thi Toát Nghieäp THPT vaø Ñaïi Hoïc
Trang 2](https://image.slidesharecdn.com/123doc-190815094752/85/123doc-vn-tong-hop-cach-nhan-biet-mot-so-cation-anion-khi-va-bai-tap-trac-nghiem-nhan-biet-pps-2-320.jpg)