5 C 2009 Aldeidi E Chetoni
- 2. Struttura e propriet├Ā IL GRUPPO CARBONILICO ALDEIDI E CHETONI CONTENGONO C O
- 3. Il gruppo carbonilico Carbonio ed Ossigeno hanno ibridizzazione sp 2 ed il gruppo carbonilico ├© planare con angoli di 120┬░ R RŌĆÖ R e RŌĆÖ possono essere due differenti gruppi e danno origine a vari gruppi funzionali contenenti il gruppo carbonilico EŌĆÖ il pi├╣ importante gruppo funzionale della chimica organica Nel doppio legame tra C ed O troviamo un legame sigma ( Žā ) ed uno pigreco ( ’ü░ ) C O 120┬░ 120┬░ 120┬░
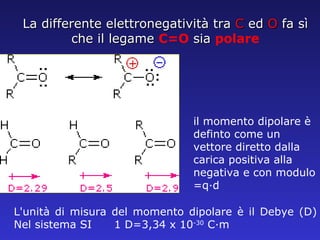
- 4. La differente elettronegativit├Ā tra C ed O fa s├¼ che il legame C=O sia polare il momento dipolare ├© definto come un vettore diretto dalla carica positiva alla negativa e con modulo =q┬Ęd L'unit├Ā di misura del momento dipolare ├© il Debye (D) Nel sistema SI 1 D=3,34 x 10 -30 C┬Ęm
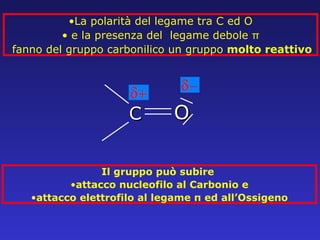
- 5. La polarit├Ā del legame tra C ed O e la presenza del legame debole ŽĆ fanno del gruppo carbonilico un gruppo molto reattivo Il gruppo pu├▓ subire attacco nucleofilo al Carbonio e attacco elettrofilo al legame ŽĆ ed allŌĆÖOssigeno C O
- 6. Struttura di un carbonile
- 7. Composti contenenti il carbonile formula famiglia Aldeide Chetone Acido Carbossilico formula famiglia Estere Ammide Cloruro Acilico C O R H C O R RŌĆÖ C O R OH C O R NH 2 C O R Cl C O R O RŌĆÖ
- 8. Aldeidi e Chetoni La nomenclatura IUPAC assegna alle aldeidi il suffisso ŌĆō ALE (es. CH 2 O metan ale ) ALDEIDE CHETONE Le aldeidi ed i chetoni sono sostanze organiche contenenti il gruppo funzionale CARBONILE il gruppo carbonilico lega un gruppo R ed un H (lŌĆÖaldeide pi├╣ piccola lega da entrambi i lati gruppi H: CH 2 O) il gruppo carbonilico ├© legato da entrambi i lati a gruppi R e presenta quindi da entrambi i lati legami c-c La nomenclatura IUPAC assegna ai chetoni il suffisso ŌĆō ONE ( es. CH 3 COCH 3 propan one ). C O R H C O R RŌĆÖ
- 9. Propriet├Ā Basso rispetto a quella degli alcoli corrispondenti per lŌĆÖincapacit├Ā (ad ecc. del metanale) di formare legami ad idrogeno. Alto rispetto a quella degli eteri corrispondenti e agli alcani a causa della maggiore polarit├Ā . MODERATA POLARIT├Ć Dovuta al gruppo C=O PUNTO DI EBOLLIZIONE SOLUBILIT├Ć La solubilit├Ā in acqua dei termini a pi├╣ basso peso molecolare, riflette il carattere polare del gruppo funzionale. Essa decresce con lŌĆÖaumentare della catena di R e RŌĆÖ
- 10. Nome Formula mM Butano 58 Etile 60 metil etere Propanale 58 Acetone 58 1-Propanolo 60 Propriet├Ā Insol. Sol. Sol. Sol. Solubilit├Ā in acqua Sol.
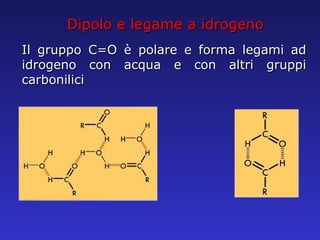
- 11. Dipolo e legame a idrogeno Il gruppo C=O ├© polare e forma legami ad idrogeno con acqua e con altri gruppi carbonilici
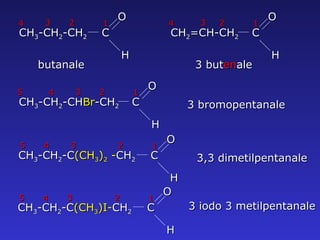
- 12. NOMENCLATURA IUPAC DELLE ALDEIDI Si considera la catena pi├╣ lunga di atomi di carbonio che contiene il gruppo aldeidico Il nome sistematico si ottiene per rimozione della -O finale del corrispondente alcano ed aggiunta del suffisso -ALE Tutti gli altri rami e gruppi sono nominati usando il sistema di nomenclatura standard IUPAC
- 13. butanale 3 bromopentanale 3,3 dimetilpentanale 3 iodo 3 metilpentanale 3 but en ale C O H CH 3 -CH 2 -CH 2 1 2 3 4 C O H CH 3 -CH 2 -CH Br -CH 2 1 2 3 4 5 C O H CH 3 -CH 2 -C (CH 3 ) 2 - CH 2 1 2 3 4 5 C O H CH 3 -CH 2 -C (CH 3 )I- CH 2 1 2 3 4 5 C O H CH 2 =CH-CH 2 1 2 3 4
- 14. Un carbonile. Un Etere. Un fenolo . Questo composto ├© lŌĆÖaroma della vaniglia. Aldeidi ŌĆō esempi dalla vita reale Descrivi i gruppi funzionali:
- 15. Aldeidi ŌĆō esempi dalla vita reale Formaldeide conservazione delle mummie C O H CH 3 Etanale ci├▓ che causa i postumi di una sbornia Benzaldeide lŌĆÖaroma delle mandorle C O H H C H O
- 16. NOMENCLATURA DEI CHETONI Si considera la catena pi├╣ lunga di atomi di carbonio che contiene il C=O chetonico Il nome sistematico si ottiene per rimozione della -o finale del corrispondente alcano ed aggiunta del suffisso ŌĆōone ed un prefisso numerico, pi├╣ piccolo possibile, che indica la posizione del gruppo carbonile Il nome e il numero degli altri sostituenti vengono elencati prima del nome sistematico seguendo lŌĆÖordine alfabetico
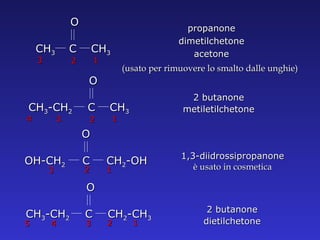
- 17. 2 butanone metiletilchetone propanone dimetilchetone acetone (usato per rimuovere lo smalto dalle unghie) 2 butanone dietilchetone 1,3-diidrossipropanone ├© usato in cosmetica C O CH 3 -CH 2 1 3 4 CH 3 2 C O CH 3 1 3 CH 3 2 C O CH 3 -CH 2 1 3 4 CH 2 -CH 3 2 5 C O OH-CH 2 1 3 CH 2 -OH 2
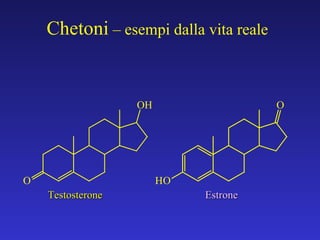
- 18. Testosterone Estrone Chetoni ŌĆō esempi dalla vita reale
- 19. compiti Pag. 226 n┬░ 9.1, 9.2 Pag. 223 n┬░ 8.29
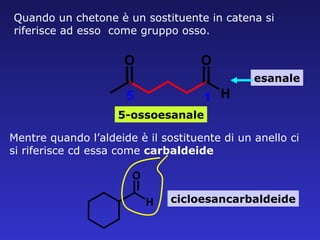
- 20. Quando un chetone ├© un sostituente in catena si riferisce ad esso come gruppo osso. esanale 5-ossoesanale Mentre quando lŌĆÖaldeide ├© il sostituente di un anello ci si riferisce cd essa come carbaldeide cicloesancarbaldeide
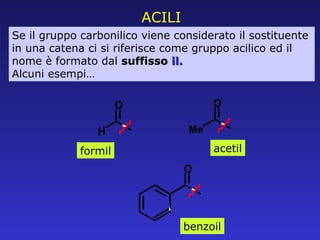
- 21. Se il gruppo carbonilico viene considerato il sostituente in una catena ci si riferisce come gruppo acilico ed il nome ├© formato dal suffisso il. Alcuni esempiŌĆ” formil acetil benzoil ACILI
- 22. Preparazione aldeidi e chetoni Ossidazione degli alcoli R-OH [O] ALDEIDE O CHETONE Il tipo di alcool determina il prodotto
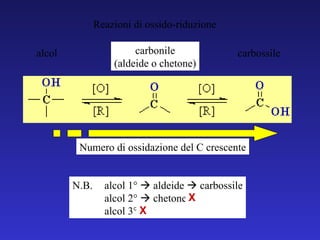
- 23. Reazioni di ossido-riduzione alcol carbonile (aldeide o chetone) carbossile Numero di ossidazione del C crescente N.B. alcol 1┬░ ’āĀ aldeide ’āĀ carbossile alcol 2┬░ ’āĀ chetone ’āĀ alcol 3┬░ ’āĀ X X
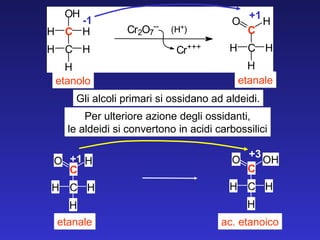
- 24. etanolo etanale Gli alcoli primari si ossidano ad aldeidi. etanale ac. etanoico -1 +1 +1 +3 Per ulteriore azione degli ossidanti, le aldeidi si convertono in acidi carbossilici C O H H H C H H H C C H H H H O C r 2 O 7 - - ( H + ) C r + + + C C H H H OH O C C H H H H O
- 25. Reattivo di Jones LŌĆÖossidazione di con CrO 3 in acido solforico e acetone ├© conosciuta come meto do di Jones. CrO 3 ├© un acido di Lewis (acquista elettroni) e pu├▓ complessare basi come la piridina. Si deve aggiungere CrO 3 alla piridina e non viceversa poich├® il reattivo ├© pericoloso da preparare. si pu├▓ fermare lŌĆÖossidazione degli alcoli 1┬░ ad aldeidi usando come ossidante il clorocromato di piridinio PCC
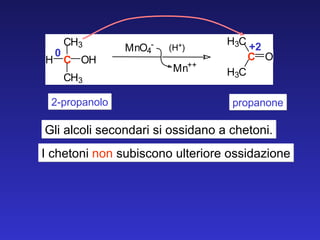
- 26. 2-propanolo propanone Gli alcoli secondari si ossidano a chetoni. 0 +2 I chetoni non subiscono ulteriore ossidazione M n O 4 - ( H + ) M n + + C H 3 C C H 3 H O H C O H 3 C H 3 C
- 27. primario aldeide secondario chetone terziario Nessuna reazione ossidazione degli alcoli [O] [O] [O]
- 28. Alcol secondario Aldeide Alcol primario chetone Le aldeidi a differenza dei chetoni subiscono facilmente unŌĆÖaltra reazione di ossidazione almeno fino allŌĆÖacido corrispondente o in extremis a CO 2 Esempi di ossidazione degli alcoli CH 2 OH [ O ] C H O C CH 3 O CH CH 3 OH [ O ]
- 29. Reazioni delle aldeidi Test di TollenŌĆÖs Ossidazione Conversione delle aldeidi ad acidi carbossilici LŌĆÖargento precipita formando uno specchio
- 30. Riduzione Aldeidi vengono ridotte ad alcoli primari In un processo opposto alla ossidazione, aldeidi e chetoni si riducono ai rispettivi alcoli La reazione pu├▓ avvenire con idrogenazione catalitica o mediante attacco nucleofilo da parte di idruri metallici (es. NaBH 4 ed il pi├╣ efficace LiAlH 4 ) Reazioni delle aldeidi & chetoni Chetoni vengono ridotti ad alcoli secondari La riduzione aggiunge essenzialmente una molecola di idrogeno al doppio legame C=O [H 2 ] [H 2 ]
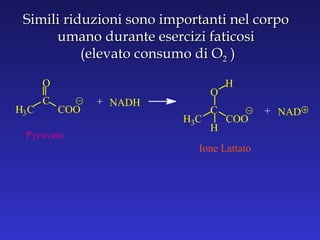
- 31. Simili riduzioni sono importanti nel corpo umano durante esercizi faticosi (elevato consumo di O 2 ) + H 3 C C O COO NADH Ione Lattato + H 3 C C O COO H H NAD Pyruvato
- 32. Addizione nucleofila Le reazioni di addizione nucleofila hanno un ruolo importante in questa classe di composti. EŌĆÖ opportuna una buona comprensione del meccanismo generele di tali reazioni. EŌĆÖ ancora una volta la polarizzazione del legame C=O a controllare la reattivit├Ā.
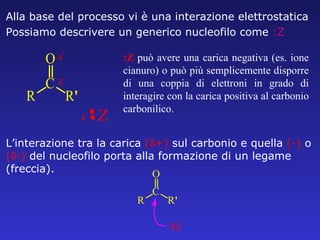
- 33. :Z pu├▓ avere una carica negativa (es. ione cianuro) o pu├▓ pi├╣ semplicemente disporre di una coppia di elettroni in grado di interagire con la carica positiva al carbonio carbonilico. Alla base del processo vi ├© una interazione elettrostatica Possiamo descrivere un generico nucleofilo come :Z LŌĆÖinterazione tra la carica ( ’üż +) sul carbonio e quella (-) o ( ’üż -) del nucleofilo porta alla formazione di un legame (freccia).
- 34. Il carbonio pu├▓ fare solo quattro legami pertanto la formazione del nuovo legame deve corrispondere alla dismissione di uno dei precedenti LŌĆÖossigeno che ├© lŌĆÖelemento pi├╣ elettro-negativo attira gli elettroni di uno dei due legami col carbonio e prende quindi una carica negativa mentre Z che ha fornito gli elettroni per il legame Z-C cede la carica negativa o prende una carica positiva se disponeva solo di una coppia di elettroni
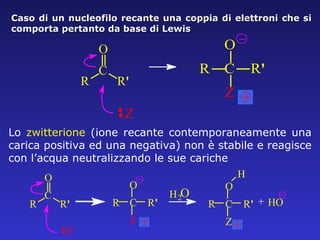
- 35. Lo zwitterione (ione recante contemporaneamente una carica positiva ed una negativa) non ├© stabile e reagisce con lŌĆÖacqua neutralizzando le sue cariche Caso di un nucleofilo recante una coppia di elettroni che si comporta pertanto da base di Lewis R C O Z R ' H 2 O R C O Z R ' H + HO
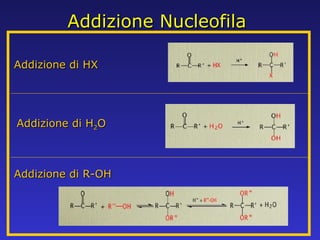
- 36. Addizione Nucleofila Addizione di HX Addizione di H 2 O Addizione di R-OH
- 37. gli ALCOLI sono nucleofili (a causa delle coppie di elettroni allŌĆÖossigeno ) e pertanto reagiscono con le aldeidi. Ricorda: il carbonio del carbonile ha una parziale carica positiva. In particolare R C O R '
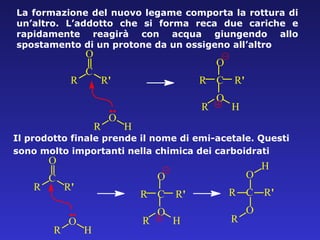
- 38. La formazione del nuovo legame comporta la rottura di unŌĆÖaltro. LŌĆÖaddotto che si forma reca due cariche e rapidamente reagir├Ā con acqua giungendo allo spostamento di un protone da un ossigeno allŌĆÖaltro Il prodotto finale prende il nome di emi-acetale. Questi sono molto importanti nella chimica dei carboidrati R C O R ' O R H R C O R ' O R H
- 39. Il glucosio ├© un aldo esoso (contiene un gruppo aldeidico e diversi gruppi alcolici: Esso esiste nella forma aperta solo in piccolissima quantit├Ā Invece, con lŌĆÖ-OH in posizione 5 si ha reazione di emiacetalizzazione con formazione di un anello a sei atomi. Emiacetali nei carboidrati
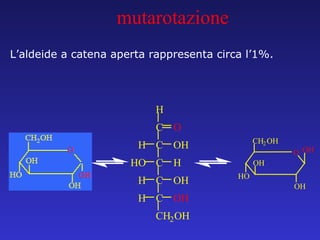
- 40. LŌĆÖaldeide a catena aperta rappresenta circa lŌĆÖ1%. mutarotazione C C O H OH H C C C CH 2 OH H HO H H OH OH O CH 2 OH OH HO OH OH
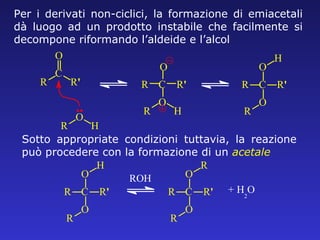
- 41. Per i derivati non-ciclici, la formazione di emiacetali d├Ā luogo ad un prodotto instabile che facilmente si decompone riformando lŌĆÖaldeide e lŌĆÖalcol Sotto appropriate condizioni tuttavia, la reazione pu├▓ procedere con la formazione di un acetale R C O R ' O R H
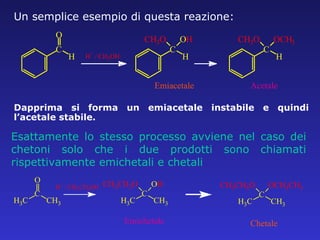
- 42. Dapprima si forma un emiacetale instabile e quindi lŌĆÖacetale stabile. Un semplice esempio di questa reazione: Esattamente lo stesso processo avviene nel caso dei chetoni solo che i due prodotti sono chiamati rispettivamente emichetali e chetali Emiacetale Acetale C O H H + / CH 3 OH C H CH 3 O OCH 3 C H CH 3 O O H Emichetale Chetale
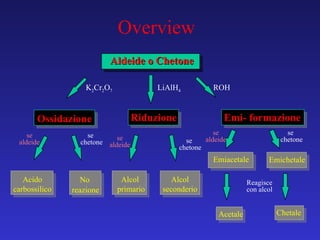
- 43. Aldeide o Chetone Ossidazione Riduzione Emi- formazione Acido carbossilico No reazione Alcol primario Alcol seconderio Emiacetale Emichetale Acetale Chetale ROH LiAlH 4 K 2 Cr 2 O 7 se aldeide se chetone Reagisce con alcol se chetone se chetone se aldeide se aldeide Overview












![Preparazione aldeidi e chetoni Ossidazione degli alcoli R-OH [O] ALDEIDE O CHETONE Il tipo di alcool determina il prodotto](https://image.slidesharecdn.com/5c2009aldeidiechetoni-091219031455-phpapp02/85/5-C-2009-Aldeidi-E-Chetoni-22-320.jpg)

![primario aldeide secondario chetone terziario Nessuna reazione ossidazione degli alcoli [O] [O] [O]](https://image.slidesharecdn.com/5c2009aldeidiechetoni-091219031455-phpapp02/85/5-C-2009-Aldeidi-E-Chetoni-27-320.jpg)
![Alcol secondario Aldeide Alcol primario chetone Le aldeidi a differenza dei chetoni subiscono facilmente unŌĆÖaltra reazione di ossidazione almeno fino allŌĆÖacido corrispondente o in extremis a CO 2 Esempi di ossidazione degli alcoli CH 2 OH [ O ] C H O C CH 3 O CH CH 3 OH [ O ]](https://image.slidesharecdn.com/5c2009aldeidiechetoni-091219031455-phpapp02/85/5-C-2009-Aldeidi-E-Chetoni-28-320.jpg)

![Riduzione Aldeidi vengono ridotte ad alcoli primari In un processo opposto alla ossidazione, aldeidi e chetoni si riducono ai rispettivi alcoli La reazione pu├▓ avvenire con idrogenazione catalitica o mediante attacco nucleofilo da parte di idruri metallici (es. NaBH 4 ed il pi├╣ efficace LiAlH 4 ) Reazioni delle aldeidi & chetoni Chetoni vengono ridotti ad alcoli secondari La riduzione aggiunge essenzialmente una molecola di idrogeno al doppio legame C=O [H 2 ] [H 2 ]](https://image.slidesharecdn.com/5c2009aldeidiechetoni-091219031455-phpapp02/85/5-C-2009-Aldeidi-E-Chetoni-30-320.jpg)