Dwi eni (a1 f011029) lipid
- 1. LIPID Di susun oleh : DWI ENI MULIATI (A1F011029)
- 2. DEFINISI LIPID • Lipid didefinisikan sebagai senyawa organik yang berada di alam semesta dan tidak larut dalam air yang diekstraksi dari makhuk hidup dengan menggunakan pelarut non polar.
- 3. SIFAT LIPID Lipida mempunyai sifat umum sebagai berikut: • Tidak larut dalam air • Larut dalam pelarut organik seperti benzena, eter, aseton, kloroform, dan karbontetraklorida • Mengandung unsur-unsur karbon, hidrogen, dan oksigen, kadang- kadang juga mengandung nitrogen dan fosfor • Bila dihidrolisis akan menghasilkan asam lemak
- 4. 1. Lipid adalah sebagai sumber energi metabolik yang sangat penting dalam pembentukkan ATP. Lipid adalah kelompok nutrien yang sangat kaya energi. Perbandingan nilai energi lipid dengan zat- zat. FUNGSI LIPID 2. Lipid adalah komponen esensial dalam membran sel dan membran sub sel.
- 5. 3. Lipid dapat berguna sebagai penyerap dan pembawa vitamin A, D, E dan K. FUNGSI LIPID 4. Lipid adalah sebagai sumber asam lemak esensial, yang bersifat sebagai pemelihara dan integritas membran sel, mengoptimalkan transpor lipid (karena keterbatasan fosfolipid sebagai agen pengemulsi). 5. Sebagai prekursor hormon-hormon sex seperti prostagtandin hormon endrogen, estrogen. 6. Lipid berfungsi sebagai pelindung organ tubuh yang vital.
- 6. 7. Lipid sebagai sumber steroid, yang sifatnya meningkatkan fungsi-fungsi biologis yang penting. FUNGSI LIPID 8. Dari aspek teknologi makanan, lipid bertindak sebagai pelicin makanan yang berbentuk pellet, sebagai zat yang mereduksi kotoran dalam makanan dan berperan dalam kelezatan makanan.
- 7. Senyawa-senyawa yang termasuk lipid dapat dibagi dalam beberapa golongan. Ada beberapa cara penggolongan yang dikenal. Bloor membagi lipid dalam tiga golongan besar, yaitu: KLASIFIKASI LIPID • yaitu ester asam lemak dengan berbagai alkohol, contohnya lemak atau gliserida dan lilin (waxes). Lipid sederhana • yaitu ester asam lemak yang mempunyai gugus tambahan, contohnya fosfolipid, cerebrosida. Lipid gabungan • yaitu ester asam lemak yang mempunyai gugus tambahan, contohnya fosfolipid, cerebrosida. Derivate lipid
- 8. Lipid memiliki reaksi kimia yang khas, antara lain: REAKSI KIMIA LIPID Hidrolisis • Hidrolisis lipid seperti triasilgliserol dapat dilakukan secara enzimatik dengan bantuan lipase, menghasilkan asam-asam lemak dan gliserol. Sifat lipase pancreas dapat dimanfaatkan yang lebih suka memecahkan ikatan ester pada posisi 1 dan 3 daripada posisi 2 dari triasilgliserol. Penyabunan • Hidrolisis lemak oleh alkali disebut penyabunan. yang dihasilkan adalah gliserol dan garam alkali asam lemak yang disebut sabun.
- 9. Penguraian (kerusakan, ketengikan) lipid • Ketengikan adalah perubahan kimia yang menimbulkan bau dan rasa tidak enak pada lemak. Penyebabnya antara lain auto oksidasi, hidrolisis dan kegiatan bakteri. REAKSI KIMIA LIPID
- 10. LEMAK DAN MINYAK Struktur lemak Struktur minyak
- 11. Lemak merupakan ester2 asam lemak asam lemak yang berasal dari alkohol tunggal, gliserol, HOCH2CHOHCH2OH, dan dikenal sebagai trigliserida. LEMAK DAN MINYAK H2C HC H2C OH OH OH + 3 HOCR -3H2O H2C HC H2C O O O C C C O O O R R R Trigliserida O
- 12. • Minyak dan lemak adalah senyawa ester yang terbentuk dari gliserol dan berbagai asam karboksilat. Ester-ester gliserol ini menurut tatanama lama disebut gliseride. Bila jumlah gugus –OH dalam rumus struktur gliserol yang diesterkan satu, digunakan nama monogliseride, sedangkan bila yang diesterkan dua atau tiga gugus –OH maka berturut-turut dinamakan digliserida atau trigliserida. Kini senyawa trigliserida kebih sering dinamakan triasilgliserol. KOMPOSISI LEMAK
- 13. • Sumber energi • Menghemat Protein • Memberi Rasa Kenyang dan Kelezatan • Sebagai Pelumas • Memelihara Suhu Tubuh • Pelindung Organ Tubuh Fungsi lemak secara pesifik adalah sebagai berikut :
- 14. • Lemak atau minyak dapat menimbulkan racun bila dipanaskan berulang-ulang selain itu pemanasan juga dapat menurunkan nilai gizi dari bahan yang digoreng. • Adanya karsinogenik dalam lemak yang dipanaskan pada suhu 300 - 350 dapat dibuktikan dari bahan pangan berlemak teroksidasi yang dapat mengakibatkan pertumbuhan kanker dalam hati. • Keracunan akibat asam hidroksil dalam lemak telah banyak diteliti. • Senyawa peroksida umumnya mengalami dekomposisi oleh panas, sehingga lemak yang dipanaskan hanya mengandung sejumlah kecil peroksida. • Proses polimerisasi lemak terjadi pada suhu sekitar 250 dan dalam suasana tanpa oksigen. Akibat yang ditimbulkan lemak dan minyak :
- 15. Sifat minyak dibedakan menjadi sifat fisikawi dan kimiawi. a. Melting point(Titik leleh) b. Softening pont(Titik lunak) c. Slipping point d. Berat jenis e. Indeks refraksi f. Smoke,flash,fire pont g. Turbidity point Sifat Lemak dan Minyak
- 16. 2. Sifat kimia a. Hidrolisa Dalam reaksi hidrolisa, minyak dan lemak akan dirubah menjadi asam lemak bebas dan gliserol. reaksi hidrolisa : b. Oksidasi Proses oksidasi dapat berlangsung apabila terjadi kontak antara sejumlah oksigen dengan minyak/lemak. Sifat Lemak dan Minyak
- 17. c. Hidrogenasi Proses hidrogenasi merupakan proses industry untuk menjenuhkan ikatan rangkap dari rantai karbon asam lemak pada lemak/minyak. d. Esterifikasi Proses esterikasi bertujuan untuk mengubah asam- asam lemak dari trigliserida dalam bentuk ester. reaksi esterifikasi : Sifat Lemak dan Minyak
- 18. e. pembentukan keton Keton dapat dihasilkan melalui penguraian dengan cara hidrolisa eter. Berikut adalah rekasinya reaski pembentukan keton : f. Penyabunan reaksi ini dilakukan dengan menambahkan larutan bas apada trilgiserida. • reaksi penyabunan : Sifat Lemak dan Minyak
- 19. Asam lemak mempunyai atom C genap dan di alam bentuk bebas atau ester dengan gliserol. Rumus kimia asam lemak adalah CH3(CH2)nCOOH Asam lemak dibagi menjadi 2 , yaitu 1. Asam lemak jenuh adalah asam lemak yang tidak memiliki ikatan rangkap, hanya memiliki ikatan tunggal saja pada rantai. 2. asam lemak tidak jenuh adalah asam lemak yang memiliki ikatan rangkap, dibagi lagi menjadi MUFA(Mono Unsaturated fatty acid ) yang memiliki satu ikatan rangkap dan PUFA(Poly Unsaturated fatty acid) yang memiliki 2 atau lebih ikatan rangkap. PUFA dan MUFA merupakan EFA (Essensial fatty acid). ASAMLEMAK
- 20. CONTOH ASAMLEMAK
- 21. Asam lemak tidak jenuh mengandung 1 atau lebih ikatan rangkap CH3 – (CH2)7 – CH = CH – (CH2)7 – COOH asam oleat HC – (CH2)7 – COOH HC – (CH2)7 – COOH HC – (CH2)7 – CH3 CH3 – (CH2)7 – CH asam oleat (sis) asam oleat (trans) Asam lemak tidak jenuh di alam adalah isomer sis CH3 – (CH2)4 – CH = CH – CH2 – CH = CH – (CH2)7 – COOH asam linoleat CH3 – CH2 – CH = CH – CH2 – CH = CH – CH2 – CH = CH – (CH2)7 – COOH asam linolenat (α) CH3 – (CH2)4 – CH = CH – CH2 – CH = CH – CH2 – CH = CH – (CH2) – COOH asam linolenat (γ) ASAMLEMAK
- 22. Sifat Fisika • Asam lemak jenuh, makin panjang rantai C, makin tinggi titik leburnya • Asam lemak tidak jenuh, makin banyak ikatan rangkap, makin rendah titik leburnya • Kelarutan asam lemak dalam air berkurang dengan bertambah panjangnya rantai C (exp. asam kaproat larut sedikit dalam air, sedang asam palmitat, stearat, oleat & linoleat tidak larut dalam air) • Umumnya, asam lemak larut dalam eter / alkohol panas Sifat Kimia Asam lemak adalah asam lemah, bila larut dalam air maka molekul asam lemak terionisasi sebagian & melepaskan ion H+ Rumus pH u/ asam lemah (Henderson-Hasselbach) HA H+ + A- maka Ka = [H+] [A-] atau [H+] = Ka [HA] [HA] [ A-] Bila di logaritma : log [H+] = log [Ka] + log [HA] [A-] Bila dikalikan dengan -1 maka : -log [H+] = -log [Ka] - log [HA] [A-] ASAMLEMAK
- 23. Ester asam lemak dengan gliserol OH – CH2 R1 – COO – CH2 HO – CH2 R1 – COO – CH2 HO – CH HO – CH R2 – COO – CH R2 – COO – CH HO – CH2 HO – CH2 R3 – COO – CH2 R3 – COO – CH2 Gliserol monogliserida digliserida trigliserida LEMAK
- 24. SIFAT - Lemak hewan berupa zat padat (suhu ruangan), lemak tumbuhan berupa zat cair - Lemak bertitik lebur tinggi adalah asam lemak jenuh, sedang lemak cair / minyak adalah asam lemak tidak jenuh - Bilangan Iodium : banyaknya gram iodium yg dpt bereaksi dg 100 gr lemak (Makin besar bilangan iodium, makin banyak ikatan rangkap) - Lemak/gliserida asam lemak pendek larut dalam air Lemak/gliserida asam lemak panjang tidak larut dalam air - Ester, kloroform, benzena, alkohol panas adalah pelarut lemak - Lemak hidrolisis asam lemak + gliserol • Bilangan penyabunan : jumlah mg KOH yg diperlukan u/ menyabunkan 1 gr lemak, dimana tgt panjang/pendeknya rantai C asam lemak/berat molekul lemak • Makin kecil berat molekul lemak, makin besar bilangan penyabunannya • Penggaraman (salting out) : penambahan garam NaCl pada larutan gliserol dalam air u/ mendapatkan sabun LEMAK
- 25. • Perbedaan lemak dan minyak adalah pada sifat fisiknya • Pada temperatur kamar lemak lemak bersifat padat sedangkan minyak bersifat cair • Contoh lemak: lard, lemak daging, mentega • Contoh minyak: Minyak jagung, minyak kedelai, minyak kelapa, minyak biji kapuk, dll • Lemak dan minyak sama2 mrpk trigliserida PERBEDAAN LEMAK DAN MINYAK
- 26. STRUKTUR SABUN DAN DETERGEN
- 27. • Merupakan reaksi sintesis kimia dalam pembuatan sabun. • Disebut juga reaksi hidrolisis alkali (reaksi trigliserida dg NaOH) menghasilkan gliserol dan sabun (garam asam karboksilat). • Sabun yang digunakan sehari-hari mrpk campuran garam-garam natrium dari asam lemak rantai panjang. Reaksi Safonifikasi Lemak
- 28. • Sabun dapat dibuat dg berbagai cara demikian pula komposisinya. Sebagai contoh dlm pembuatan sabun, dapat ditambah dg bahan pewangi, zat warna, dan germisida. • Jika basa yg digunakan adalah KOH maka sabun yg diperoleh disebut sebagai sabun lunak. H2C HC H2C OH OH OH + H2C HC H2C O O O C C C O O O R R R Trigliserida NaOH 3 RCOO- Na+ gliserol Sabun Reaksi Safonifikasi Lemak
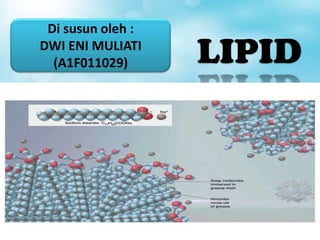
- 29. • Molekul sabun memp satu ujung yg polar, COO- Na+, dan satu ujung yg lain bersifat nonpolar yg berupa rantai hidrokarbon panjang, 12 hingga 18 atom C • Ujung yg polar larut dlm air disebut bersifat hidrofilik, sedangkan ujung nonpolar yg tdk larut dlm air bersifat hidrofobik atau lipofilik dan larut dlm pelarut non polar. Sabun yg memp 2 gugus (ujung) baik polar maupun nonpolar dlm satu molekul disebut sebagai Molekul Ampifatik Reaksi Safonifikasi Lemak
- 30. Ujung non polar dari sabun akan mengikat dan mengangkat minyak dan kotoran lainnya yg bersifat nonpolar sementara ujung yg polar akan berikatan dg air. Kotoran dan minyak akan terangkat dan hilang bersama dengan guyuran air. Cara kerja Sabun dan Deterjen
- 31. Seperti sabun, deterjen memiliki rantai molekul hidrofobik atau rantai molekul yg tidak suka air dan komponen hidrofilik atau rantai molekul suka-air. Hidrokarbon hidrofobik yang ditolak oleh air, tapi ditarik oleh minyak dan lemak. Dengan kata lain berarti bahwa salah satu ujung molekul akan tertarik ke air, sementara sisi lain mengikat minyak. Air bersabun yang mengelilinginya (kotoran) memungkinkan sabun atau deterjen untuk menarik kotoran dari pakaian atau piring dan masuk ke dalam air bilasan untuk selanjutnya dapat dipisahkan. Cara kerja Sabun dan Deterjen
- 32. SIFAT-SIFAT SABUN DAN DETERGEN SABUN • Sabun adalah garam alkali dari asam lemak suku tinggi sehingga akan dihidrolisis parsial oleh air yang menyebabkan larutan sabun dalam air bersifat basa. SABUN • Jika larutan sabun dalam air diaduk maka akan menghasilkan buih, peristiwa ini tidak akan terjadi pada air sadah. Sabun dapat menghasilkan buih setelah garam-garam Mg atau Ca dalam air mengendap. DETERJEN • Dapat melarutkan lemak. • Tak dipengaruhi kesadahan air.
- 33. sabun Sabun adalah garam alkali karboksilat. Molekul lebih mudah terdegradasi oleh bakteri pengurai. Tidak bisa dipakai untuk mencuci dalam air sadah Detergen Detergen adalah garam alkali alkil sulfat atau sulfoniat Molekul detergen harganya lebih murah dan sukar terdegradasi oleh bakteri pengurai. Molekul detergen tidak bereaksi dengan ion Ca2+ dan ion Mg2+ PERBEDAAN SABUN DAN DETERJEN
- 34. sabun Sabun adalah hasil proses penetralan asam lemak dengan menggunakan alkali Sabun biasanya digunakan untuk membersihkan suatu product yang berhubungan langsung dengan kulit manusia Detergen Deterjen adalah campuran zat kimia dari sintetik ataupun alam yang memiliki sifat yang dapat menarik zat pengotor dari media. Deterjen digunakan sebagai sabun cuci pakaian PERBEDAAN SABUN DAN DETERJEN




















![Sifat Fisika
• Asam lemak jenuh, makin panjang rantai C, makin tinggi titik leburnya
• Asam lemak tidak jenuh, makin banyak ikatan rangkap, makin rendah titik
leburnya
• Kelarutan asam lemak dalam air berkurang dengan bertambah panjangnya rantai
C (exp. asam kaproat larut sedikit dalam air, sedang asam palmitat, stearat, oleat &
linoleat tidak larut dalam air)
• Umumnya, asam lemak larut dalam eter / alkohol panas
Sifat Kimia
Asam lemak adalah asam lemah, bila larut dalam air maka molekul asam lemak
terionisasi sebagian & melepaskan ion H+
Rumus pH u/ asam lemah (Henderson-Hasselbach)
HA H+ + A- maka Ka = [H+] [A-] atau [H+] = Ka [HA]
[HA] [ A-]
Bila di logaritma : log [H+] = log [Ka] + log [HA]
[A-]
Bila dikalikan dengan -1 maka : -log [H+] = -log [Ka] - log [HA]
[A-]
ASAMLEMAK](https://image.slidesharecdn.com/dwienia1f011029lipid-130512202711-phpapp02/85/Dwi-eni-a1-f011029-lipid-22-320.jpg)












