Enzima
- 2. MetabolismeConjunt de processosquĂmics que es produeixen a la cèl·lula, catalitzats per enzims i que tenencom a objectiul’obtenciĂł de materials i energia per a les diferensfuncionsvitals.
- 3. Vies del metabolismeEl metabolismepotdescompondre’s en dos sèries de reaccions:Anabolisme: té com a finalitatl’obtenció de substà nciesorgà niquescomplexes a partir de substà nciesmés simples ambconsumd’energia. Ex: fotosintesis, sintesis de proteïnesCatabolisme:conjunt de processos per els que les molèculescomplexessóndegradades a molèculesmés simples. Es tracta de processosdestructiusgeneradorsd’energia.Ex: glucolisis, respiraciócel·lular, fermentacions
- 5. Tipus de metabolismePer la forma d’obtenirelsmaterials:autòtrof: aquellsorganismes que sintetitzenelsseuscompostosorgĂ nicsfent servir com a font de materialssubstĂ nciesinorgĂ niques. (CO2) ex: vegetalsverds i moltesbacteries.Heteròtrof: aquellsorganismes que sintetitzenelsseuscompostosorgĂ nicsfent servir com a font de materialsaltressubstĂ nciesorgĂ niques. ex: animals, fongs i moltesbacteries.Per la forma d’obtenirl’energia:Fotosintèitcs: fan servir la llumcom a fontd’energia. ex: vegetalsverds i moltesbacteries.Quimiosintètics: obtenenl’energia de reaccionsquĂmiques ex: moltesbacteries.
- 6. Concepted’enzimElsenzimssĂłn, generalment, proteĂŻnes o associacions de proteĂŻnes i d’altresmolèculesorgĂ niques o inorgĂ niques que actuencatalitzantelsprocessosquĂmics que es donen en elsèssersvius.Quèéscatalitzar?Accelerar les reaccions
- 7. Disminuir l’energiad’activacióElsenzimses recuperen intactes al final del procés. Degut a això es necessiten en moltpoquesquantitats.
- 8. CaracterĂstiquesNo es consumeixen.MoltespecĂfics.Absoluta: sols actĂşa sobre un substrat. (p.e.:ureasa per a urea)De grup: reconeix un grup de molèculesdeterminat. (p.e.: glucosidasa sobre glucòsids)De classe: depèn del tipusd’enllaç, no del tipus de molècula. (pe: fosfatases sobre grupfosfat)ActĂşen a Temperatura ambient(TÂş Ă©sserviu).Moltactius.Pes molecular moltelevat.
- 9. En les reaccionsquĂmiquescatalitzades per enzims que poden discorrertant en sentitdelsproductescomdelssubstractes, Ă©s el mateixenzim el que actĂşa en ambdossentits.En tota reacciĂłcatalitzada per un enzimdistingirem: A i B Substractes C i D Productes de la reacciĂł E Enzim E A + B C + D E
- 10. Reaccionsexergòniques: desprendimentd’energia calorĂfica per part de substĂ nciesquĂmiques en reaccionar.Això fa augmentar la Temperatura medi.Energialliure de:ReactiusProductes(subst.reaccionants) (subst. ProduĂŻdes)* Energia que tĂ© un sistema per poder realitzar un treball i depèn de l’energiacontinguda en elsenllaçosinterns de les molècules.E
- 11. Energiad’activacióPerò la reacció NO es fa ESPONTÀNIAMENT. Cal donar Energia per debilitar elsenllaços. (pà g.11)
- 12. Modelcomparatiude la disminucióde l’energiad’activació per a l’accióde l’enzim.2) L’enzimdisminueixo elimina l’energiad’activaciónecessà ria i la reacciótranscorreespontà niament.1) La reaccióno es produeixja que fa falta una energiad’activació per a que transcorreixiespontà niament.EnzimSubstracteProducte
- 13. Mecanismede l’accióenzimà ticaExplicacióde la curva de Michaelis-Menten
- 14. Grà ficade Michaelis-MentenVariacióde l’activitatenzimà ticaambla concentracióde substracte: Aquestagrà ficademostrala formaciód’uncomplexeenzim-substracteNivellde saturacióde l’enzimActivitatenzimà ticaConcentracióde substracte
- 15. Per a poder explicar la grà ficade Michaelis-Mentenfemla següentanalogia: Suposemque la cèl·lulaésuna fà bricade rellotges. En aquestafà bricahi ha 40 obrers i cada un potfabricar un rellotgea la hora (R/h). El departamentde subministres proporciona una determinada quantitatde peces per a ferun rellotge(S/h) i elsobrers fabriquen elsrellotges. En aquestaanalogia, comhaurà spogutdeduir, elsobrerssónelsenzims, les pecessubministradeselssubstractes i elsrellotgeselsproductes.Subministre per a fer4 rellotgesa la hora.
- 16. Suposem ara que la direcciĂłdesitgiaugmentarla producciĂł i augmentaprogressivamentel subministre de peces per a ferrellotges(S/h) segonsindica ala grĂ fica.Taula de dades605040302010GrĂ ficarealRellotgesfabricatsper hora (R/h)0 10 20 30 40 50 60 70 80 90 100Subministre de peces per hora (S/h)
- 17. Tipologiaenzims- enzimsestrictamentproteĂŻcs.1 o + cadenespolipeptĂdiques.- holoenzims.1 fracciĂłpolipeptĂdica (apoenzim)1 fracciĂł no polipeptĂdica (cofactor)InorgĂ nic: IĂłmetĂ l·lic: Mg2+, Zn2+,K+,..OrgĂ nic: Coenzim: ATP, NAD+, NADP+,CoA…
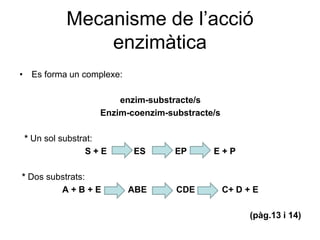
- 18. Mecanisme de l’accióenzimà ticaEs forma un complexe: enzim-substracte/sEnzim-coenzim-substracte/s * Un sol substrat:S + E ES EP E + P * Dos substrats:A + B + E ABE CDE C+ D + E (pà g.13 i 14)
- 19. Mecanismed’actuaciĂłenzimĂ tica:1) Es forma un complexe: enzim-substracteo substractes.2) S’uneixelcoenzima aquestcomplexe.3) Les restes delsaminoĂ cidsque configuran el centre actiucatalitzenel procĂ©s. Per a això debiliten elsenllaçosnecessaris per a que la reacciĂłquĂmica es facia baixatemperatura i no es necessitiuna elevada energiad’activaciĂł.4) Elsproductesde la reacciĂłse separen del centre actiu i l’enzim es recupera intacte per a noves catĂ lisis.5) Elscoenzimscol·laborenen el procĂ©s; beaportantenergia(ATP), electrons(NADH/NADPH) o en d’altresfuncionsrelacionadesambla catĂ lisisenzimĂ ticaproductessubstracteEnzimEnzima inactivaCentre actiuCoenzim
- 21. Coenzims:Sónsubstà nciesnecessaries en el procés de catalisisenzimà tica. Maisónproteïnes:Transportadorsd’electrons (o d’oxidació-reducció):NAD+/NADHNADP+/NADPHFAD+/FADH2Transportadorsd’energia (o de transferència):ADP/ATPGDP/GTP
- 22. El NAD+ /NADH i el NADP+/NADPHintervenenen elsprocessosde transferènciad’electronsentre una substà nciaque s’oxida: O, a una que es redueix, G.e-e-
- 23. L’ ADP/ATP és un coenzimque intervéen les transferènciesd’energiadelsprocessosexergònicsalsendergònics.EE
- 24. Factors que condicionen l’activitatenzimà ticaTemperaturaCompte: desnaturalització(pèrdua estructura tercià ria)pHInhibidorsIrreversible: enverinadorsReversible:CompetitivaNo competitivaActivadors(pà g.18)
- 25. enverinadorssubstracteenvenenadorEnzimElsenverinadorssónsubstà nciesque s’uneixenal centre actiumitjançantenllaçosfortsen un procésirreversible, amb el que impedeixende manera definitiva la catà lisi.
- 26. InhibiciĂłcompetitivasubstracteinhibidorEnzimEnzimaSenseinhibidorambinhibidorElsinhibidorscompetitiussĂłnsubstĂ ncies, moltesvegadessimilarsquĂmicamentalssubstractes, que s’uneixenal centre actiuimpedintambaixòque s’uneixel substracte. El procĂ©sĂ©sreversible i depĂ©nde la quantitatde substracte i d’inhibidor, doncsambdoscompeteixen per l’enzim.
- 27. Inhibicióno competitivasubstracteNo es produeixla catà lisiEnzimEnzimAmbinhibidorSenseinhibidorinhibidorElsinhibidorsno competitiussónsubstà nciesque s’uneixena l’enzimen llocsdiferentsal centre actiualterantla conformacióde la molècul·lade tal manera que, encara es formiun complexeenzim-substracte, no es produeixla catà lisi. Aquesttipusd’inhibiciódepènsolsamentde la concentraciód’inhibidor.
- 29. InhibicióalostèricasubstracteEnzimactivaCentre actiuSenseinhibidorEnzima inactivaElsinhibidorsalostèricss’uneixena una zona de l’enzima i canvienla configuraciódel centre actiude tal manera que impedeixenque el substracte es puguiunir a ell.ambinhibidorCentre reguladorInhibidor (lligand)
- 31. activadorsproductessubstracteEnzima inactivaEnzimactivaactivadorElsactivadorss’uneixenal centre regulador, canvienla configuraciódel centre actiu, que fins a aquestmomentestavainactiu i desencadenen la catà lisienzimà tica.