hukum dasar kimia
Download as pptx, pdf3 likes1,614 views
Dokumen ini menjelaskan hukum-hukum dasar dalam kimia, termasuk hukum kekekalan massa Lavoisier dan hukum perbandingan tetap Proust. Contoh reaksi serta konsep-volume gas juga diuraikan, termasuk hukum Gay Lussac dan Avogadro. Hukum-hukum ini membentuk dasar bagi pemahaman tentang interaksi unsur dan senyawa dalam reaksi kimia.
1 of 13
Downloaded 115 times










Ad
Recommended
C 2
C 2Jenni Nainggolan
╠²
Dokumen ini membahas hukum kelipatan berganda yang dicetuskan oleh John Dalton, yang menyatakan bahwa jika dua unsur membentuk lebih dari satu senyawa, perbandingan massa unsur tersebut akan menjadi bilangan bulat sederhana. Juga dijelaskan tentang hukum perbandingan volume yang dirumuskan oleh Gay Lussac dan hukum Avogadro yang menunjukkan hubungan antara volume gas yang bereaksi dan hasil reaksi dalam kondisi yang sama. Contoh percobaan dituliskan untuk memperkuat penjelasan tentang hukum-hukum ini.Hukum dasar kimia
Hukum dasar kimiaEKO SUPRIYADI
╠²
Dokumen ini membahas hukum-hukum dasar kimia dan aplikasinya dalam perhitungan kimia, termasuk hukum Lavoisier, Proust, Dalton, Gay-Lussac, dan Avogadro. Selain itu, juga dijelaskan tentang hubungan perbandingan massa unsur dalam senyawa dan perbandingan volume gas dalam reaksi kimia. Contoh percobaan dan perhitungan disertakan untuk mendemonstrasikan penerapan hukum-hukum ini dalam konteks praktis.Handout interaktif hukum hukum dasar kimia
Handout interaktif hukum hukum dasar kimiaAdi Prihandono
╠²
Dokumen tersebut membahas lima hukum dasar kimia yaitu hukum Lavoisier tentang kekekalan massa, hukum Proust tentang perbandingan tetap unsur dalam senyawa, hukum Dalton tentang perbandingan berganda, hukum Gay-Lussac tentang perbandingan volum gas, dan hukum Avogadro tentang jumlah partikel dalam volum yang sama. Terdapat pula contoh soal latihan untuk menerapkan lima hukum dasar kimia terseHukum Hukum Dasar Kimia PPT
Hukum Hukum Dasar Kimia PPTPuswita Septia Usman
╠²
Dokumen ini menjelaskan hukum dasar kimia, termasuk hukum kekekalan massa yang dikemukakan oleh Lavoisier, hukum perbandingan tetap oleh Proust, dan hukum perbandingan berganda oleh Dalton. Hukum kekekalan massa menyatakan bahwa massa zat sebelum dan sesudah reaksi tetap, sedangkan hukum perbandingan tetap menunjukkan bahwa rasio massa elemen dalam senyawa adalah konstan. Hukum perbandingan berganda menggambarkan variasi rasio massa antara senyawa yang berbeda yang dibentuk dari elemen yang sama.Hukum dasar kimia
Hukum dasar kimiaYeni Rahayu
╠²
1. Dokumen tersebut membahas biografi dan kontribusi ilmuwan kimia seperti Lavoisier, Proust, Dalton, Gay-Lussac, dan Avogadro dalam menemukan hukum-hukum dasar kimia seperti hukum kekekalan massa, hukum perbandingan tetap, hukum kelipatan perbandingan, hukum Gay-Lussac, dan hipotesis Avogadro.
2. Hukum-hukum tersebut menjelaskan hubungan antara massa, volumeKimia dasar
Kimia dasarKomunitas Teknik Sipil & Arsitek
╠²
Dokumen ini membahas perbedaan antara unsur, senyawa, dan campuran dalam kimia, dengan menjelaskan karakteristik serta cara pemisahannya. Unsur tidak dapat dipecah lebih lanjut, senyawa memiliki komposisi tetap dan memerlukan reaksi kimia untuk pemisahan, sedangkan campuran memiliki komponen yang dapat dipisahkan secara fisika dan tidak mengubah sifat masing-masing. Selain itu, dokumen juga menjelaskan hukum-hukum dasar kimia yang meliputi hukum kekekalan massa, perbandingan tetap, kelipatan berganda, perbandingan volume, dan hipotesis Avogadro.Hukum dasar kimia dan stoikiometri
Hukum dasar kimia dan stoikiometri pierse
╠²
Ringkasan dari dokumen tersebut adalah:
Hukum-hukum dasar kimia seperti hukum kekekalan massa, hukum perbandingan tetap, hukum perbandingan berganda, dan hukum perbandingan volume yang menjelaskan tentang komposisi dan perbandingan zat dalam reaksi kimia. Konsep stoikiometri menerapkan hukum-hukum ini dalam menghitung kadar unsur, rumus kimia, dan perhitungan berdasarkan persHukum Dalton
Hukum DaltonMuhammad Amal
╠²
Dokumen ini menjelaskan hukum kelipatan perbandingan yang dirumuskan oleh John Dalton pada tahun 1803 berdasarkan pengamatan perbandingan massa unsur. Dalton menyatakan bahwa jika dua unsur membentuk lebih dari satu senyawa, perbandingan massa unsur dalam senyawa tersebut adalah bilangan bulat sederhana. Contoh perhitungan perbandingan massa antara nitrogen dan oksigen dalam senyawa NO dan NO2 menunjukkan bahwa rumus ini memenuhi hukum yang diajukan.Hukum Dalton beserta Contoh dan Latihan soal
Hukum Dalton beserta Contoh dan Latihan soalKinantiPutriU
╠²
Dokumen tersebut membahas tentang John Dalton dan hukum Dalton mengenai teori atom. Hukum Dalton menyatakan bahwa dalam suatu senyawa, unsur-unsur akan bergabung secara proporsional sesuai dengan berat atomnya untuk membentuk senyawa tertentu. Diberikan contoh senyawa air yang terbentuk dari hidrogen dan oksigen, serta senyawa belerang dan oksigen.Modul kimia 2 finish
Modul kimia 2 finishHERI_HASAN
╠²
Modul kimia ini membahas perhitungan kimia untuk kelas 10 yang mencakup hukum dasar kimia seperti hukum Lavoisier, Proust, Dalton, Gay Lussac, dan Avogadro. Tujuan modul adalah untuk mengajarkan siswa menghitung volume gas, menentukan mol, dan rumus empiris serta molekul. Selain itu, modul ini menyertakan latihan terkait perhitungan massa dan volume dalam reaksi kimia.Hukum Hukum Dasar Kimia
Hukum Hukum Dasar KimiaPuswita Septia Usman
╠²
Dokumen ini merupakan modul pembelajaran tentang hukum dasar kimia dan perhitungan kimia yang ditujukan untuk siswa kelas X. Modul ini membahas berbagai hukum kimia seperti hukum kekekalan massa, hukum perbandingan tetap, dan hukum perbandingan volume, serta penerapannya dalam perhitungan kimia. Terdapat juga berbagai latihan dan contoh soal untuk membantu siswa memahami konsep-konsep yang diajarkan.Hukum dasar kimia dan perhitungan kimia
Hukum dasar kimia dan perhitungan kimiaEKO SUPRIYADI
╠²
Modul ini membahas hukum dasar kimia dan perhitungan kimia, termasuk hukum kekekalan massa, hukum perbandingan tetap, hukum perbandingan berganda, dan hukum perbandingan volum. Terdapat dua kegiatan belajar yang menjelaskan teori-teori tersebut serta memberikan tugas dan percobaan untuk membuktikannya. Pemahaman materi ini sangat penting sebagai dasar untuk perhitungan kimia di modul-modul selanjutnya.Soal Pilihan Ganda Hukum Dasar Kimia
Soal Pilihan Ganda Hukum Dasar Kimiatiatika11
╠²
Dokumen tersebut membahas tentang konsep-konsep dasar kimia seperti perhitungan massa molekul relatif senyawa, hukum Gay-Lussac tentang volume gas, perbandingan massa unsur dalam senyawa, dan hukum kekekalan massa Lavoisier. Dokumen tersebut berisi 10 pertanyaan uraian singkat tentang konsep-konsep kimia dasar tersebut.Latihan soal stoikiometri
Latihan soal stoikiometriMian Maria Stephanie Gultom
╠²
Dokumen berisi soal latihan stoikiometri yang meliputi perhitungan jumlah zat, volume gas, massa zat, dan kemolaran larutan kimia. Terdapat 12 soal yang mencakup konsep-konsep dasar stoikiometri seperti perhitungan mol, atom, molekul, volume gas, dan massa zat berdasarkan informasi yang diberikan.RPP Hukum kekekalan massa
RPP Hukum kekekalan massaYuliana Karina
╠²
Rencana Pelaksanaan Pembelajaran (RPP) ini membahas hukum kekekalan massa Lavoisier dengan menggunakan model pembelajaran kooperatif Number Head Together (NHT). Guru akan menjelaskan hukum kekekalan massa dan membagi siswa dalam kelompok untuk mengerjakan soal-soal diskusi mengenai hukum tersebut. Penilaian dilakukan berdasarkan hasil diskusi dan pengetahuan siswa tentang hukum kekekalan massa.Stoikiometri
Stoikiometri Jaenal Mutakin
╠²
Dokumen tersebut membahas tentang stoikiometri dan hukum-hukum dasar kimia seperti hukum kekekalan massa, hukum perbandingan tetap, dan hukum Avogadro. Juga membahas konsep mol, massa atom relatif, dan volume satu mol gas.Mr Herina Yuni Utami
Mr Herina Yuni Utamiguest2ef754c
╠²
Dokumen ini membahas massa atom relatif dan massa molekul relatif, serta kompetensi dasar dalam menjelaskan konsep tersebut. Terdapat penjelasan tentang perbandingan massa unsur, latihan soal, dan cara menentukan massa molekul relatif serta kelimpahan isotop tembaga. Massa atom relatif tembaga adalah 63,5, yang dihitung berdasarkan isotop cu-63 dan cu-65.Stoikiometri
StoikiometriAhmad Nurjaman
╠²
Dokumen ini membahas berbagai hukum dasar kimia, seperti hukum Boyle, Lavoisier, Proust, Gay Lussac, Dalton, dan Avogadro, beserta contoh penerapannya. Selain itu, dijelaskan sifat-sifat gas dan definisi tekanan, serta rumus gas ideal. Dokumen juga mencakup contoh soal yang melibatkan perhitungan massa, volume, dan reaksi kimia terkait gas dan senyawa.Materi
MateriNanda Yuliantoro
╠²
Teori kinetika gas menjelaskan perilaku makroskopis gas melalui pendekatan statistik perilaku mikroskopis molekul gas. Gas dianggap ideal jika molekulnya bergerak acak, tidak saling tarik menarik, dan tumbukan elastis. Tekanan gas diakibatkan perubahan momentum molekul saat tumbuk dinding. Teori ini berhasil menjelaskan tekanan, suhu, dan kapasitas kalor gas.STOIKIOMETRI KIMIA
STOIKIOMETRI KIMIAPanggita Inoprasetyo
╠²
Dokumen ini menjelaskan dasar-dasar stoikiometri dalam kimia, termasuk hukum Lavoisier tentang kekekalan massa, hukum Gay-Lussac tentang perbandingan volume gas, dan konsep mol serta perhitungan massa, jumlah partikel, dan konsentrasi. Selain itu, dokumen ini juga membahas rumus empiris dan rumus molekul, serta pentingnya penyetarakan persamaan reaksi dalam analisis kimia. Contoh-contoh konkret disertakan untuk menjelaskan penerapan hukum-hukum ini dalam reaksi kimia.Stoikiometri
StoikiometriArda
╠²
Dokumen ini membahas konsep stoikiometri, termasuk ikatan ion antara unsur logam dan non logam, serta perhitungan terkait larutan asam sulfat dan senyawa nabr. Terdapat pertanyaan mengenai konfigurasi elektron, massa unsur, dan persentase dalam larutan. Contoh perhitungan disertakan untuk memperjelas konsep yang dijelaskan.STOIKIOMETRI
STOIKIOMETRIMei Wina
╠²
Dokumen ini membahas konsep stoikiometri dalam kimia, termasuk hukum dasar seperti hukum Lavoisier, Proust, Dalton, dan Gay Lussac, serta pentingnya perhitungan kuantitas reaktan dan produk dalam reaksi kimia. Stoikiometri memainkan peran krusial dalam kehidupan sehari-hari dan aplikasi praktis seperti produksi energi dan pertanian. Selain itu, dokumen ini menjelaskan rumus empiris, rumus molekul, massa molar, dan persamaan reaksi untuk memahami hubungan antara berbagai unsur dan senyawa.Hukum dasar kimia
Hukum dasar kimiaDina Amalina
╠²
Dokumen tersebut membahas beberapa hukum dasar kimia seperti hukum penyatuan volume Gay-Lussac, hukum Avogadro, dan hukum perbandingan timbal balik Richter. Hukum-hukum tersebut menjelaskan hubungan antara volume, jumlah molekul, dan berat unsur-unsur yang bereaksi dalam suatu persamaan kimia.Tugas kimia hk. gay lussac & avogadro
Tugas kimia hk. gay lussac & avogadrohallotugas
╠²
Hukum Gay Lussac dan hipotesis Avogadro membentuk dasar stoikiometri reaksi gas, di mana perbandingan volum gas yang bereaksi sama dengan koefisien reaksi jika diukur pada suhu dan tekanan yang sama, memungkinkan perhitungan volum gas lain berdasarkan volum yang diketahui.Bab 5 kd 2.2 (hk kim & hit kim)
Bab 5 kd 2.2 (hk kim & hit kim) Resma Puspitasari
╠²
Dokumen ini membahas hukum dasar kimia, termasuk hukum kekekalan massa, perbandingan tetap, perbandingan berganda, dan perbandingan volume. Selain itu, dijelaskan tentang massa atom relatif, massa molekul relatif, serta hubungan mol dengan jumlah partikel dan massa molar. Dokumen ini juga menguraikan hitungan kimia dan aplikasi stoikiometri dalam reaksi kimia.Teori Kinetik Gas
Teori Kinetik GasShofiah Saffanah
╠²
* Suhu oksigen (O2) pada 0┬░C = 273 K
* Massa atom O = 16 x 1.66x10^-27 kg = 2.56x10^-26 kg
* Massa molekul O2 = 2 x 2.56x10^-26 = 5.12x10^-26 kg
* R = 8.314 J/mol.K
* Mengubah ke m/s^2: 9.8 m/s^2
* Persamaan: vrms = ŌłÜ(3RT/M)
* Maka kecepatan rata-rata molekul O2 = ŌłÜ(3x8.314xH4240 2e2e2a3an 0assa
H4240 2e2e2a3an 0assaToga Siahaan
╠²
Hukum kekekalan massa yang dikemukakan oleh Antoine Lavoisier menyatakan bahwa massa zat sebelum dan sesudah reaksi kimia adalah sama, yang berarti massa tidak dapat diciptakan atau dimusnahkan. Lavoisier menggunakan percobaan dengan merkuri dan oksigen untuk membuktikan hukum ini, yang luas digunakan dalam berbagai bidang ilmiah. Contoh penerapannya termasuk reaksi pembakaran yang menunjukkan bahwa jumlah massa total reaktan sama dengan massa total produk.Stoikiometri
StoikiometriAvidia Sarasvati
╠²
1. Kelompok 5 melakukan percobaan untuk menguji hukum kekekalan massa dan hubungan antara unsur-unsur dalam senyawa kimia. Mereka mengukur massa sebelum dan sesudah reaksi serta mengamati hasil reaksi berbagai larutan.
2. Dari hasilnya, ditemukan bahwa massa zat sebelum dan sesudah reaksi tetap, membuktikan kebenaran hukum kekekalan massa. Jumlah mol zat yang bereak502679681-PPT-HUKUM-HUKUM-DASAR-KIMIA.pptx
502679681-PPT-HUKUM-HUKUM-DASAR-KIMIA.pptxAnnisasylvia3
╠²
Dokumen ini membahas hukum dasar kimia, termasuk hukum kekekalan massa, hukum perbandingan tetap, hukum perbandingan berganda, hukum perbandingan volume, dan hipotesis Avogadro, yang kesemuanya berperan penting dalam stoikiometri. Hukum-hukum ini menjelaskan prinsip-prinsip dasar mengenai interaksi massa dan volume dalam reaksi kimia. Selain itu, dokumen ini menyediakan contoh soal untuk menggambarkan penerapan hukum-hukum tersebut dalam perhitungan kimia.cupdf.com_hukum-dasar-kimia-56a0d2c36af34.ppt
cupdf.com_hukum-dasar-kimia-56a0d2c36af34.pptJunesturalely
╠²
Dokumen tersebut merangkum hukum-hukum dasar kimia yang meliputi hukum Lavoisier (hukum kekekalan massa), hukum Proust (hukum perbandingan tetap), hukum Dalton (hukum perbandingan berganda), hukum Gay-Lussac (hukum perbandingan volume), dan hipotesis Avogadro (hukum perbandingan jumlah molekul). Dokumen tersebut juga menjelaskan tokoh-tokoh penemunya dan contoh penerapMore Related Content
What's hot (20)
Hukum Dalton beserta Contoh dan Latihan soal
Hukum Dalton beserta Contoh dan Latihan soalKinantiPutriU
╠²
Dokumen tersebut membahas tentang John Dalton dan hukum Dalton mengenai teori atom. Hukum Dalton menyatakan bahwa dalam suatu senyawa, unsur-unsur akan bergabung secara proporsional sesuai dengan berat atomnya untuk membentuk senyawa tertentu. Diberikan contoh senyawa air yang terbentuk dari hidrogen dan oksigen, serta senyawa belerang dan oksigen.Modul kimia 2 finish
Modul kimia 2 finishHERI_HASAN
╠²
Modul kimia ini membahas perhitungan kimia untuk kelas 10 yang mencakup hukum dasar kimia seperti hukum Lavoisier, Proust, Dalton, Gay Lussac, dan Avogadro. Tujuan modul adalah untuk mengajarkan siswa menghitung volume gas, menentukan mol, dan rumus empiris serta molekul. Selain itu, modul ini menyertakan latihan terkait perhitungan massa dan volume dalam reaksi kimia.Hukum Hukum Dasar Kimia
Hukum Hukum Dasar KimiaPuswita Septia Usman
╠²
Dokumen ini merupakan modul pembelajaran tentang hukum dasar kimia dan perhitungan kimia yang ditujukan untuk siswa kelas X. Modul ini membahas berbagai hukum kimia seperti hukum kekekalan massa, hukum perbandingan tetap, dan hukum perbandingan volume, serta penerapannya dalam perhitungan kimia. Terdapat juga berbagai latihan dan contoh soal untuk membantu siswa memahami konsep-konsep yang diajarkan.Hukum dasar kimia dan perhitungan kimia
Hukum dasar kimia dan perhitungan kimiaEKO SUPRIYADI
╠²
Modul ini membahas hukum dasar kimia dan perhitungan kimia, termasuk hukum kekekalan massa, hukum perbandingan tetap, hukum perbandingan berganda, dan hukum perbandingan volum. Terdapat dua kegiatan belajar yang menjelaskan teori-teori tersebut serta memberikan tugas dan percobaan untuk membuktikannya. Pemahaman materi ini sangat penting sebagai dasar untuk perhitungan kimia di modul-modul selanjutnya.Soal Pilihan Ganda Hukum Dasar Kimia
Soal Pilihan Ganda Hukum Dasar Kimiatiatika11
╠²
Dokumen tersebut membahas tentang konsep-konsep dasar kimia seperti perhitungan massa molekul relatif senyawa, hukum Gay-Lussac tentang volume gas, perbandingan massa unsur dalam senyawa, dan hukum kekekalan massa Lavoisier. Dokumen tersebut berisi 10 pertanyaan uraian singkat tentang konsep-konsep kimia dasar tersebut.Latihan soal stoikiometri
Latihan soal stoikiometriMian Maria Stephanie Gultom
╠²
Dokumen berisi soal latihan stoikiometri yang meliputi perhitungan jumlah zat, volume gas, massa zat, dan kemolaran larutan kimia. Terdapat 12 soal yang mencakup konsep-konsep dasar stoikiometri seperti perhitungan mol, atom, molekul, volume gas, dan massa zat berdasarkan informasi yang diberikan.RPP Hukum kekekalan massa
RPP Hukum kekekalan massaYuliana Karina
╠²
Rencana Pelaksanaan Pembelajaran (RPP) ini membahas hukum kekekalan massa Lavoisier dengan menggunakan model pembelajaran kooperatif Number Head Together (NHT). Guru akan menjelaskan hukum kekekalan massa dan membagi siswa dalam kelompok untuk mengerjakan soal-soal diskusi mengenai hukum tersebut. Penilaian dilakukan berdasarkan hasil diskusi dan pengetahuan siswa tentang hukum kekekalan massa.Stoikiometri
Stoikiometri Jaenal Mutakin
╠²
Dokumen tersebut membahas tentang stoikiometri dan hukum-hukum dasar kimia seperti hukum kekekalan massa, hukum perbandingan tetap, dan hukum Avogadro. Juga membahas konsep mol, massa atom relatif, dan volume satu mol gas.Mr Herina Yuni Utami
Mr Herina Yuni Utamiguest2ef754c
╠²
Dokumen ini membahas massa atom relatif dan massa molekul relatif, serta kompetensi dasar dalam menjelaskan konsep tersebut. Terdapat penjelasan tentang perbandingan massa unsur, latihan soal, dan cara menentukan massa molekul relatif serta kelimpahan isotop tembaga. Massa atom relatif tembaga adalah 63,5, yang dihitung berdasarkan isotop cu-63 dan cu-65.Stoikiometri
StoikiometriAhmad Nurjaman
╠²
Dokumen ini membahas berbagai hukum dasar kimia, seperti hukum Boyle, Lavoisier, Proust, Gay Lussac, Dalton, dan Avogadro, beserta contoh penerapannya. Selain itu, dijelaskan sifat-sifat gas dan definisi tekanan, serta rumus gas ideal. Dokumen juga mencakup contoh soal yang melibatkan perhitungan massa, volume, dan reaksi kimia terkait gas dan senyawa.Materi
MateriNanda Yuliantoro
╠²
Teori kinetika gas menjelaskan perilaku makroskopis gas melalui pendekatan statistik perilaku mikroskopis molekul gas. Gas dianggap ideal jika molekulnya bergerak acak, tidak saling tarik menarik, dan tumbukan elastis. Tekanan gas diakibatkan perubahan momentum molekul saat tumbuk dinding. Teori ini berhasil menjelaskan tekanan, suhu, dan kapasitas kalor gas.STOIKIOMETRI KIMIA
STOIKIOMETRI KIMIAPanggita Inoprasetyo
╠²
Dokumen ini menjelaskan dasar-dasar stoikiometri dalam kimia, termasuk hukum Lavoisier tentang kekekalan massa, hukum Gay-Lussac tentang perbandingan volume gas, dan konsep mol serta perhitungan massa, jumlah partikel, dan konsentrasi. Selain itu, dokumen ini juga membahas rumus empiris dan rumus molekul, serta pentingnya penyetarakan persamaan reaksi dalam analisis kimia. Contoh-contoh konkret disertakan untuk menjelaskan penerapan hukum-hukum ini dalam reaksi kimia.Stoikiometri
StoikiometriArda
╠²
Dokumen ini membahas konsep stoikiometri, termasuk ikatan ion antara unsur logam dan non logam, serta perhitungan terkait larutan asam sulfat dan senyawa nabr. Terdapat pertanyaan mengenai konfigurasi elektron, massa unsur, dan persentase dalam larutan. Contoh perhitungan disertakan untuk memperjelas konsep yang dijelaskan.STOIKIOMETRI
STOIKIOMETRIMei Wina
╠²
Dokumen ini membahas konsep stoikiometri dalam kimia, termasuk hukum dasar seperti hukum Lavoisier, Proust, Dalton, dan Gay Lussac, serta pentingnya perhitungan kuantitas reaktan dan produk dalam reaksi kimia. Stoikiometri memainkan peran krusial dalam kehidupan sehari-hari dan aplikasi praktis seperti produksi energi dan pertanian. Selain itu, dokumen ini menjelaskan rumus empiris, rumus molekul, massa molar, dan persamaan reaksi untuk memahami hubungan antara berbagai unsur dan senyawa.Hukum dasar kimia
Hukum dasar kimiaDina Amalina
╠²
Dokumen tersebut membahas beberapa hukum dasar kimia seperti hukum penyatuan volume Gay-Lussac, hukum Avogadro, dan hukum perbandingan timbal balik Richter. Hukum-hukum tersebut menjelaskan hubungan antara volume, jumlah molekul, dan berat unsur-unsur yang bereaksi dalam suatu persamaan kimia.Tugas kimia hk. gay lussac & avogadro
Tugas kimia hk. gay lussac & avogadrohallotugas
╠²
Hukum Gay Lussac dan hipotesis Avogadro membentuk dasar stoikiometri reaksi gas, di mana perbandingan volum gas yang bereaksi sama dengan koefisien reaksi jika diukur pada suhu dan tekanan yang sama, memungkinkan perhitungan volum gas lain berdasarkan volum yang diketahui.Bab 5 kd 2.2 (hk kim & hit kim)
Bab 5 kd 2.2 (hk kim & hit kim) Resma Puspitasari
╠²
Dokumen ini membahas hukum dasar kimia, termasuk hukum kekekalan massa, perbandingan tetap, perbandingan berganda, dan perbandingan volume. Selain itu, dijelaskan tentang massa atom relatif, massa molekul relatif, serta hubungan mol dengan jumlah partikel dan massa molar. Dokumen ini juga menguraikan hitungan kimia dan aplikasi stoikiometri dalam reaksi kimia.Teori Kinetik Gas
Teori Kinetik GasShofiah Saffanah
╠²
* Suhu oksigen (O2) pada 0┬░C = 273 K
* Massa atom O = 16 x 1.66x10^-27 kg = 2.56x10^-26 kg
* Massa molekul O2 = 2 x 2.56x10^-26 = 5.12x10^-26 kg
* R = 8.314 J/mol.K
* Mengubah ke m/s^2: 9.8 m/s^2
* Persamaan: vrms = ŌłÜ(3RT/M)
* Maka kecepatan rata-rata molekul O2 = ŌłÜ(3x8.314xH4240 2e2e2a3an 0assa
H4240 2e2e2a3an 0assaToga Siahaan
╠²
Hukum kekekalan massa yang dikemukakan oleh Antoine Lavoisier menyatakan bahwa massa zat sebelum dan sesudah reaksi kimia adalah sama, yang berarti massa tidak dapat diciptakan atau dimusnahkan. Lavoisier menggunakan percobaan dengan merkuri dan oksigen untuk membuktikan hukum ini, yang luas digunakan dalam berbagai bidang ilmiah. Contoh penerapannya termasuk reaksi pembakaran yang menunjukkan bahwa jumlah massa total reaktan sama dengan massa total produk.Stoikiometri
StoikiometriAvidia Sarasvati
╠²
1. Kelompok 5 melakukan percobaan untuk menguji hukum kekekalan massa dan hubungan antara unsur-unsur dalam senyawa kimia. Mereka mengukur massa sebelum dan sesudah reaksi serta mengamati hasil reaksi berbagai larutan.
2. Dari hasilnya, ditemukan bahwa massa zat sebelum dan sesudah reaksi tetap, membuktikan kebenaran hukum kekekalan massa. Jumlah mol zat yang bereakSimilar to hukum dasar kimia (20)
502679681-PPT-HUKUM-HUKUM-DASAR-KIMIA.pptx
502679681-PPT-HUKUM-HUKUM-DASAR-KIMIA.pptxAnnisasylvia3
╠²
Dokumen ini membahas hukum dasar kimia, termasuk hukum kekekalan massa, hukum perbandingan tetap, hukum perbandingan berganda, hukum perbandingan volume, dan hipotesis Avogadro, yang kesemuanya berperan penting dalam stoikiometri. Hukum-hukum ini menjelaskan prinsip-prinsip dasar mengenai interaksi massa dan volume dalam reaksi kimia. Selain itu, dokumen ini menyediakan contoh soal untuk menggambarkan penerapan hukum-hukum tersebut dalam perhitungan kimia.cupdf.com_hukum-dasar-kimia-56a0d2c36af34.ppt
cupdf.com_hukum-dasar-kimia-56a0d2c36af34.pptJunesturalely
╠²
Dokumen tersebut merangkum hukum-hukum dasar kimia yang meliputi hukum Lavoisier (hukum kekekalan massa), hukum Proust (hukum perbandingan tetap), hukum Dalton (hukum perbandingan berganda), hukum Gay-Lussac (hukum perbandingan volume), dan hipotesis Avogadro (hukum perbandingan jumlah molekul). Dokumen tersebut juga menjelaskan tokoh-tokoh penemunya dan contoh penerapSTOIKIOMETRI.ppt
STOIKIOMETRI.pptSamudraMutiara
╠²
Dokumen ini membahas hukum stoikiometri, termasuk hukum Lavoisier (kekekalan massa), hukum Proust (perbandingan tetap), hukum Dalton (perbandingan berganda), dan hukum Gay-Lussac (perbandingan volume), dengan memberikan contoh percobaan untuk setiap hukum. Hasil percobaan menunjukkan bahwa massa zat sebelum dan sesudah reaksi tetap, perbandingan massa unsur dalam senyawa adalah tetap, dan perbandingan massa unsur yang terlibat dalam reaksi kimia memenuhi aturan yang ditentukan. Keseluruhan, dokumen ini menjelaskan hubungan antara massa dan volume pada reaksi kimia serta menunjukkan aplikasi dari hukum-hukum tersebut.HUKUM-HUKUM_DASAR_KIMIA.pdf
HUKUM-HUKUM_DASAR_KIMIA.pdf119LennyOctaviany
╠²
Dokumen tersebut membahas empat hukum dasar kimia, yaitu:
1. Hukum kekekalan massa
2. Hukum perbandingan tetap
3. Hukum perbandingan berganda
4. Hukum perbandingan volumeHUKUM DASAR KIMIA.pptx
HUKUM DASAR KIMIA.pptxDianUmniyatulMardiya
╠²
Dokumen ini menjelaskan hukum dasar kimia, termasuk hukum kekekalan massa, hukum perbandingan tetap, dan hukum kelipatan berganda. Berbagai contoh memperlihatkan bahwa massa zat sebelum dan sesudah reaksi tetap sama, serta perbandingan massa unsur dalam senyawa tertentu dan tetap. Selain itu, volume gas yang bereaksi berbanding langsung sesuai jumlah molekul yang terlibat dalam reaksi.Hukum Dasar Kimia.docx
Hukum Dasar Kimia.docxAbuYusuf33
╠²
Dokumen tersebut membahas lima hukum dasar kimia, yaitu hukum kekekalan massa, hukum perbandingan tetap, hukum kelipatan perbandingan, hukum perbandingan volume, dan hukum Avogadro. Hukum-hukum ini menjelaskan sifat-sifat reaksi kimia dan komposisi senyawa kimia."MATKUL KIMDAS MINGGU KE 2 TENTANG Hukum dasar kimia.pdf
MATKUL KIMDAS MINGGU KE 2 TENTANG Hukum dasar kimia.pdfhayati440625
╠²
Dokumen ini membahas dasar-dasar teori atom dan hukum-hukum dasar kimia, termasuk hukum kekekalan massa, hukum perbandingan tetap, dan reaksi kimia. Konsep-konsep tersebut dijelaskan melalui kontribusi ilmuwan seperti Democritus dan John Dalton, serta pengaruhnya terhadap pemahaman unsur dan senyawa. Selain itu, berbagai jenis reaksi kimia, termasuk reaksi pembentukan, penguraian, dan redoks, juga dijelaskan.Hukum hukum dasar kimia
Hukum hukum dasar kimiaPutri Aisyah
╠²
Hukum-hukum dasar kimia meliputi hukum Lavoisier tentang kekekalan massa, hukum Proust tentang perbandingan tetap unsur dalam senyawa, hukum Dalton tentang atom dan molekul, hukum Gay-Lussac tentang perbandingan volume gas, serta hukum Avogadro tentang jumlah partikel dalam volume gas yang sama.PPT Hukum Dasar Kimia; Hukum Kekekalan Massa
PPT Hukum Dasar Kimia; Hukum Kekekalan Massappgyunitagartina99
╠²
Dokumen ini membahas hukum dasar kimia, termasuk hukum kekekalan massa Lavoisier, hukum perbandingan tetap, berganda, dan volume dari Proust, Dalton, dan Gay-Lussac. Contoh penerapan hukum-hukum ini dalam perhitungan dan analisis data percobaan juga disertakan. Selain itu, terdapat penjelasan mengenai reaksi kimia dan perbandingan massa unsur dalam senyawa.hukm hukum dasar kimia fase Eijhjshfbshf.pptx
hukm hukum dasar kimia fase Eijhjshfbshf.pptxsumastikadharma
╠²
Dokumen ini membahas hukum dasar kimia yang penting dalam perhitungan kuantitatif reaksi kimia, termasuk hukum kekekalan massa, hukum perbandingan tetap, hukum perbandingan berganda, dan hukum perbandingan volume. Contoh-contoh diberikan untuk mengilustrasikan penerapan hukum-hukum ini dalam reaksi antara berbagai unsur. Pemahaman hukum-hukum ini esensial untuk memahami interaksi reaktan dan produk dalam kimia.hukm hukum dasar kimia.pptx
hukm hukum dasar kimia.pptxsumastikadharma
╠²
Dokumen ini membahas hukum dasar kimia, termasuk hukum kekekalan massa, hukum perbandingan tetap, hukum perbandingan berganda, dan hukum perbandingan volume. Setiap hukum diilustrasikan dengan contoh reaksi kimia yang menunjukkan hubungan kuantitatif antara reaktan dan produk. Penekanan pada hukum-hukum ini penting untuk memahami perhitungan dalam kimia.X.4 hukum dasar kimia
X.4 hukum dasar kimiaAzizah Alya
╠²
Dokumen ini menjelaskan hukum kekekalan massa dan perbandingan massa unsur dalam reaksi kimia, termasuk hukum perbandingan tetap dan hukum perbandingan berganda. Contoh eksperimen menunjukkan hasil reaksi antara hidrogen dan oksigen serta perbandingan gas dalam reaksi. Penjelasan juga mencakup hubungan antara koefisien reaksi dan volume gas yang terlibat pada kondisi temperatur dan tekanan yang sama.Hukum-hukum dasar kimia Hukum Lavoisier.pptx
Hukum-hukum dasar kimia Hukum Lavoisier.pptxDianRahmawati79
╠²
Dokumen ini menjelaskan hukum dasar kimia, khususnya hukum kekekalan massa yang dikemukakan oleh Antoine Lavoisier. Hukum ini menyatakan bahwa massa total zat sebelum reaksi sama dengan massa total setelah reaksi. Contoh dan soal diberikan untuk mendemonstrasikan penerapan hukum ini dalam reaksi kimia.Hukum dasar lavo proust
Hukum dasar lavo proustolanascorepta
╠²
Dokumen ini membahas hukum dasar kimia dan biografi beberapa ilmuwan penting seperti Lavoisier dan Proust, yang menjelaskan prinsip kekekalan massa dan hukum perbandingan tetap. Lavoisier mengemukakan bahwa massa zat sebelum dan sesudah reaksi adalah sama, sedangkan Proust menyatakan bahwa perbandingan massa unsur dalam senyawa adalah tetap. Terdapat juga contoh percobaan untuk menerapkan hukum-hukum tersebut dalam reaksi kimia.HK KIMIA 1.ppt
HK KIMIA 1.pptErbinPindoRejekiOs
╠²
Dokumen ini membahas hukum-hukum dasar dalam kimia, termasuk hukum Lavoisier (kekekalan massa), Proust (perbandingan tetap), Dalton (perbandingan berganda), Gay-Lussac (perbandingan volume), dan hipotesis Avogadro. Contoh-contoh konkret diberikan untuk setiap hukum, seperti reaksi antara hidrogen dan oksigen serta perbandingan massa unsur dalam senyawa. Latihan disediakan untuk membangun pemahaman tentang penerapan hukum-hukum tersebut dalam perhitungan kimia.dasar dasar kima
dasar dasar kimaSiti Khoiriah
╠²
Dokumen ini membahas lima hukum dasar kimia yaitu hukum Lavoisier (kekekalan massa), hukum Proust (perbandingan tetap), hukum Dalton (kelipatan berganda), hukum Gay-Lussac (perbandingan volume), dan hipotesis Avogadro. Hukum-hukum ini menjelaskan tentang kekekalan massa dan perbandingan massa, volume, dan jumlah molekul dalam reaksi kimia.BAB 4_HUKUM DASAR DAN PERHITUNGAN KIMIA (IPA KIMIA X KurMer).pptx
BAB 4_HUKUM DASAR DAN PERHITUNGAN KIMIA (IPA KIMIA X KurMer).pptxssuser2d50731
╠²
Dokumen ini membahas hukum dasar dan perhitungan kimia untuk siswa SMA/MA Kelas X IPA, termasuk hukum Lavoisier, Proust, Dalton, dan Gay-Lussac, serta konsep mol dan perhitungan terkait. Terdapat contoh penerapan hukum-hukum tersebut dalam kehidupan sehari-hari dan perhitungan kadar logam dalam bijih. Selain itu, dijelaskan juga dampak kebijakan ekspor nikel Indonesia dan pentingnya ekonomi atom dalam prinsip kimia hijau.Tugas Makalah Kimia Richard Amar Heng.pdf
Tugas Makalah Kimia Richard Amar Heng.pdfMariusRikiOlasesa
╠²
Hukum Dalton menyatakan bahwa perbandingan massa unsur-unsur yang membentuk lebih dari satu senyawa adalah bilangan bulat sederhana. Hukum ini membuktikan bahwa atom merupakan unit terkecil yang berperan dalam reaksi kimia.BAB 4_HUKUM DASAR DAN PERHITUNGAN KIMIA (IPA KIMIA X KurMer).pptx
BAB 4_HUKUM DASAR DAN PERHITUNGAN KIMIA (IPA KIMIA X KurMer).pptxmufidatulhasanah1
╠²
Dokumen ini membahas tentang media pengajaran kimia untuk siswa SMA/MA, khususnya hukum dasar dan perhitungan kimia. Termasuk konsep mol, massa atom relatif, dan penerapan hukum dalam kehidupan sehari-hari. Selain itu, juga mencakup relevansi hukum kimia terhadap produksi dan pengolahan bijih tembaga dan nikel di Indonesia.Hukum-Hukum Dasar Kimia
Hukum-Hukum Dasar KimiaAgus Triana
╠²
Hukum-hukum dasar kimia meliputi hukum Dalton tentang perbandingan massa unsur dalam senyawa, hukum Gay-Lussac tentang perbandingan volume gas yang bereaksi dan hasilnya, serta hukum Avogadro mengenai hubungan antara volume dan jumlah molekul gas. Ketiga hukum ini memberikan landasan penting dalam memahami reaksi kimia.Ad
Recently uploaded (20)
Bahan Bacaan BIOGRAFI Singkat Ir. SOEKARNO.pdf
Bahan Bacaan BIOGRAFI Singkat Ir. SOEKARNO.pdfZulzaman GMNI
╠²
Soekarno merupakan presiden Republik Indonesia dan seorang
proklamator kemerdekaan. Dari tahun 1945 hingga 1967 ia menjabat sebagai presiden. Kemahirannya diakui hampir dengan semua orang di seluruh penjuru dunia. Keahlian yang mendukung kemampuannya adalah dia menguasai 6 bahasa asing. Selain itu, Soekarno memiliki 26 gelar doktor kehormatan dari berbagai universitas di beberapa belahan dunia. Publikasi Laporan Keuangan Perusahaan_Pelatihan *Penyusunan LAPORAN KEUANGAN ...
Publikasi Laporan Keuangan Perusahaan_Pelatihan *Penyusunan LAPORAN KEUANGAN ...Kanaidi ken
╠²
Narasumber/ Pemateri Training: Kanaidi, SE., M.Si., cSAP., CBCM
HP/Wa Kanaidi: 0812 2353 284,
e-mail : kanaidi63@gmail.com
-------------------------------------------Hubungan Laporan Keuangan dan Laporan Keberlanjutan (Sustainability Report)_P...
Hubungan Laporan Keuangan dan Laporan Keberlanjutan (Sustainability Report)_P...Kanaidi ken
╠²
Narasumber/ Pemateri Training: Kanaidi, SE., M.Si., cSAP., CBCM
HP/Wa Kanaidi: 0812 2353 284,
e-mail : kanaidi63@gmail.com
-------------------------------------------Modul Ajar Prakarya Kerajinan Kelas 12 SMA/MA Fase F Kurikulum Merdeka
Modul Ajar Prakarya Kerajinan Kelas 12 SMA/MA Fase F Kurikulum MerdekaModul Kelas
╠²
Modul Ajar Prakarya Kerajinan Kelas 12 Fase F Kurikulum Merdeka [MODULKELAS.COM]SOSIALISASI PBG dan SLF Kota Madiun - STR - Rosyid Fix.pptx
SOSIALISASI PBG dan SLF Kota Madiun - STR - Rosyid Fix.pptxDinas Penanaman Modal dan Pelayanan Terpadu Satu Pintu Kota Madiun
╠²
SOSIALISASI PBG dan SLF Kota Madiun - STR - Rosyid Fix.pptxModul Ajar Prakarya Pengolahan Kelas 10 SMA/MA Fase E Kurikulum Merdeka
Modul Ajar Prakarya Pengolahan Kelas 10 SMA/MA Fase E Kurikulum MerdekaModul Kelas
╠²
Modul Ajar Prakarya Pengolahan Kelas 10 Fase E Kurikulum Merdeka [MODULKELAS.COM]Modul Ajar Matematika Kelas 7 Deep Learning
Modul Ajar Matematika Kelas 7 Deep LearningAdm Guru
╠²
Modul ajar dengan metode pembelajaran Deep Learning yaitu Meaningful Learning, Mindful Learning, dan Joyful LearningModul Ajar B Indonesia Kelas 9 Deep Learning
Modul Ajar B Indonesia Kelas 9 Deep LearningAdm Guru
╠²
Modul ajar dengan metode pembelajaran Deep Learning yaitu Meaningful Learning, Mindful Learning, dan Joyful LearningProses Audit dan Verifikasi Laporan Keuangan Perusahaan_Pelatihan *Penyusunan...
Proses Audit dan Verifikasi Laporan Keuangan Perusahaan_Pelatihan *Penyusunan...Kanaidi ken
╠²
Narasumber/ Pemateri Training: Kanaidi, SE., M.Si., cSAP., CBCM
HP/Wa Kanaidi: 0812 2353 284,
e-mail : kanaidi63@gmail.com
-------------------------------------------Modul Ajar Pendidikan Pancasila Kelas 7 Deep Learning
Modul Ajar Pendidikan Pancasila Kelas 7 Deep LearningAdm Guru
╠²
Modul ajar dengan metode pembelajaran Deep Learning yaitu Meaningful Learning, Mindful Learning, dan Joyful LearningModul Ajar Matematika Kelas 8 Deep Learning
Modul Ajar Matematika Kelas 8 Deep LearningAdm Guru
╠²
Modul ajar dengan metode pembelajaran Deep Learning yaitu Meaningful Learning, Mindful Learning, dan Joyful Learning12_Residu_dan_Kutub (Variabel Kompleks) - Unpak.pdf
12_Residu_dan_Kutub (Variabel Kompleks) - Unpak.pdfAsepSaepulrohman4
╠²
Residu dan kutub adalah dua konsep penting dalam analisis kompleks, khususnya dalam teori fungsi kompleks dan perhitungan integral kompleks. Keduanya berperan penting dalam teorema residu Cauchy yang digunakan untuk menghitung integral kontur (jalur tertutup) dari fungsi kompleks.Peta Jalan Dekarbonisasi Industri Nikel Indonesia 2025ŌĆō2045
Peta Jalan Dekarbonisasi Industri Nikel Indonesia 2025ŌĆō2045Dadang Solihin
╠²
Dekarbonisasi industri nikel bukan sekadar agenda teknis atau pemenuhan komitmen internasional terhadap pengurangan emisi karbon, tetapi merupakan langkah strategis yang menyentuh aspek geopolitik, ketahanan nasional, dan arah pembangunan jangka panjang Indonesia. Sebagai negara dengan cadangan dan produksi nikel terbesar di dunia, Indonesia memiliki posisi tawar yang signifikan dalam transisi energi global, terutama dalam penyediaan bahan baku utama untuk baterai kendaraan listrik dan sistem penyimpanan energi berbasis energi terbarukan.
Dokumen Peta Jalan Dekarbonisasi Industri Nikel Indonesia 2025ŌĆō2045 yang diterbitkan oleh Bappenas RI bukan sekadar roadmap teknokratis, tetapi representasi dari arah baru pembangunan nasional yang berorientasi pada keberlanjutan, kemandirian energi, dan peningkatan nilai tambah industri domestik. Buku ini menegaskan bahwa transformasi industri ekstraktif ke arah yang lebih hijau tidak bisa dilepaskan dari konteks kepentingan nasional yang lebih luas: memperkuat kedaulatan sumber daya alam, menjaga keberlanjutan lingkungan hidup, dan memperkokoh peran Indonesia dalam arsitektur energi hijau global.
Modul Ajar IPS Kelas 8 Deep Learning
Modul Ajar IPS Kelas 8 Deep LearningAdm Guru
╠²
Modul ajar dengan metode pembelajaran Deep Learning yaitu Meaningful Learning, Mindful Learning, dan Joyful LearningModul Ajar Biologi Kelas 12 Deep Learning
Modul Ajar Biologi Kelas 12 Deep LearningAdm Guru
╠²
Modul ajar dengan metode pembelajaran Deep Learning yaitu Meaningful Learning, Mindful Learning, dan Joyful LearningContoh Jurnal Modul 3 PPG 2025_ Filosofi Pendidikan dan Pendidikan Nilai - Ha...
Contoh Jurnal Modul 3 PPG 2025_ Filosofi Pendidikan dan Pendidikan Nilai - Ha...aryadus
╠²
Contoh Jurnal Modul 3 PPG 2025_ Filosofi Pendidikan dan Pendidikan Nilai - Halaman all - TribunNePRESENTASI Tentang Dunia Usaha dan juga Manfaat komputer dalam Dunia Usaha
PRESENTASI Tentang Dunia Usaha dan juga Manfaat komputer dalam Dunia Usahafebrianalkadir123
╠²
ini adalah presentasi tentang dunia usaha, dibuatnya presentasi ini adalah untuk memenuhi tugas perkuliahan saya di mata kuliah Komputer dan Masyarakat. Dibuat nya presentasi ini agar memudahkan orang orang yang sedang mencari document .pptx yang bertemakan Dunia UsahaSOSIALISASI PBG dan SLF Kota Madiun - STR - Rosyid Fix.pptx
SOSIALISASI PBG dan SLF Kota Madiun - STR - Rosyid Fix.pptxDinas Penanaman Modal dan Pelayanan Terpadu Satu Pintu Kota Madiun
╠²
Ad
hukum dasar kimia
- 1. Elvira Risyeu Eriston Pratama Mercy Nathalia Bregitna Natalie Christ Dame S. Nia Afrilea Gultom Ronaldo Kelompok 2
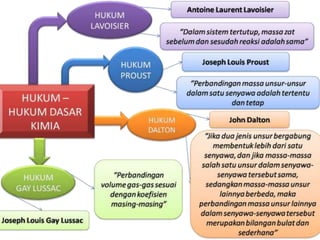
- 4. ŌĆó Hukum kekekalan massa dikemukakan oleh Antoine Laurent Lavoisier , sehingga dikenal sebagai ŌĆ£Hukum LavoisierŌĆØ ŌĆó Isi Hukum Lavoisier : ŌĆ£ massa total zat-zat sebelum reaksi akan selalu sama dengan massa total zat-zat hasil reaksi ŌĆ£ ŌĆó Misalnya reaksi antara raksa (merkuri) dengan oksigen. Bila senyawa merkuri oksida yang berwarna merah dipanaskan, akan dihasillkan logam merkuri dan gas oksigen. Sebaliknya, bila logam merkuri dipanaskan dengan oksigen akan dihasilkan merkuri oksida. Ternyata, diketahui bahwa massa oksigen yang dibutuhkan pada proses pemanasan logam merkuri sama dengan massa oksigen yang dihasilkan dari pemanasan merkuri oksida. ŌĆó Contoh : 14 gram besi bereaksi dengan 8 gram belerang membentuk senyawa besi belerang dengan massa 22 gram. Antoine Laurent Lovoisier adalah seorang ilmuwan Prancis ynag dijuluki Bapak Kimia Modern.
- 5. Berdasarkan penelitian terhadap berbagai senyawa yang dilakukan oleh Joseph Louis Proust, Proust menyimpulkan bahwa : ŌĆ£ perbandingan massa unsur-unsur dalam suatu senyawa adalah tertentu dan tetap ŌĆ£ Senyawa yang sama , meskipun berasal dari sumber yang berbeda atau dibuat dengan cara yang berbeda, ternyata mempunyai komposisi yang sama. Pernyataan tersebut dikenal dengan Hukum Perbandingan Tetap atau Hukum Proust. Contoh : Hasil analisis terhadap garam dari berbagai daerah. Asal garam Massa Natrium (Na) Massa Klorin (Cl) Massa Na : Cl Indramayu 0,786 g 1,214 g 0,786 : 1,214 = 1 : 1,54 Madura 0,59 g 0,91 g 0,59 : 0,91 = 1 : 1,54 Import 0,983 g 1,517 g 0,983 : 1,517 = 1 : 1,54
- 6. Contoh soal : Sebanyak 0,455 gr sampel magnesium, dibakar dalam 2,315 gr gas oksigen untuk menghasilkan magnesium oksida. Setelah reaksi terjadi, diperoleh massa oksigen yang tidak bereaksi sebanyak 2,15 gr. Berapakah massa magnesium oksida yang terbentuk? Jawab : Massa sebelum reaksi = massa magnesium + massa gas oksigen = 0,455 gr magnesium + 2,315 gr oksigen = 2,770 gr. Massa sesudah reaksi = massa magnesium yang terbentuk + massa gas oksigen (sisa) = 2,770 gr = massa magnesium yang terbentuk + 2,15 gr = 2,770 gr Massa magnesium yang terbentuk = 2,770 gr ŌĆō 2,15 gr = 0,620 gr.
- 7. Hukum dasar kimia yang dikemukakan oleh Dalton berkaitan dengan pasangan unsur yang mampu membentuk lebih dari satu senyawa. Berbunyi : ŌĆ£ Bila dua unsur dapat membentuk lebih dari satu senyawa, dan jika massa salah satu unsur tersebut tetap (sama), maka perbandingan massa unsur yang lain dalam senyawa-senyawa tersebut merupakan bilangan bulat dan sederhana.ŌĆØ Selain merumuskan hukum kelipatan ŌĆō perbandingan, John Dalton juga berperan dalam perkembangan teori atom modern.
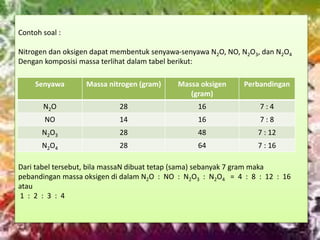
- 8. Contoh soal : Nitrogen dan oksigen dapat membentuk senyawa-senyawa N2O, NO, N2O3, dan N2O4 Dengan komposisi massa terlihat dalam tabel berikut: Dari tabel tersebut, bila massaN dibuat tetap (sama) sebanyak 7 gram maka pebandingan massa oksigen di dalam N2O : NO : N2O3 : N2O4 = 4 : 8 : 12 : 16 atau 1 : 2 : 3 : 4 Senyawa Massa nitrogen (gram) Massa oksigen (gram) Perbandingan N2O 28 16 7 : 4 NO 14 16 7 : 8 N2O3 28 48 7 : 12 N2O4 28 64 7 : 16
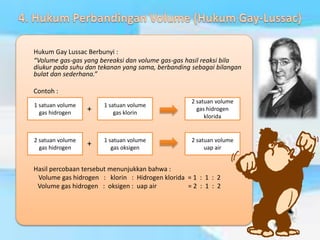
- 9. Hukum Gay Lussac Berbunyi : ŌĆ£Volume gas-gas yang bereaksi dan volume gas-gas hasil reaksi bila diukur pada suhu dan tekanan yang sama, berbanding sebagai bilangan bulat dan sederhana.ŌĆØ Contoh : + + Hasil percobaan tersebut menunjukkan bahwa : Volume gas hidrogen : klorin : Hidrogen klorida = 1 : 1 : 2 Volume gas hidrogen : oksigen : uap air = 2 : 1 : 2 1 satuan volume gas hidrogen 1 satuan volume gas klorin 2 satuan volume uap air 2 satuan volume gas hidrogen 2 satuan volume gas hidrogen klorida 1 satuan volume gas oksigen
- 11. Berbunyi : ŌĆ£ Pada suhu dan tekanan yang sama, semua gas yang volumenya sama akan mengandung jumlah molekul yang samaŌĆØ. Amadeo Avogadro berpendapat bahwa satuan terkecil dari suatu zat tidak harus atom, tetapi dapat berupa gabungan atom-atom yang sejenis maupun berbeda jenis, yang disebut molekul. Sehingga, bila bagian terkecil dari gas hidrogen dan oksigen adalah molekul yang merupakan gabungan dari dua atom, maka didapatkan : 1 molekul hidrogen + ┬Į molekul oksigen 1 molekul air (2 atom hidrogen) + (1 atom oksigen) (2 atom hidrogen + 1 atom oksigen) + Berdasarkan konsep tersebut, maka sampai sekarang gas-gas (kecuali gas mulia) dianggap sebagai molekul diatomik (gabungan dari dua atom) sehingga penulisan rumus kimia gas hidrogen adalah H2 ; oksigen O2 ; nitrogen N2 ; dan seterusnya.
- 12. Misal : 3 volume higdrogen + 1 volume nitrogen 2 volume amoniak 3 H2 + N2 2NH2 Hubungan volume gas, jumlah molekul, dan koefisien reaksi adalah : Volume yang dicari = koefisien yang dicari x volume yang diketahui koefisien yang diketahui Jumlah molekul yang dicari = koefisien yang dicari x jumlah molekul koefisien yang diketahui yang diketahui
