Ikatan kimia
- 1. SMA NEGERI 1 TENGGARONG KOMPETENSI MATERI LATIHAN EVALUASI IKATAN KIMIA Kelas x semester 1 ANDRIYANI,S.Pd
- 2. IKATAN KIMIA INDIKATOR SK/KD LIHAT KOMPETENSINYA? KLIK AJA KOMPETENSI MATERI LATIHAN EVALUASI
- 3. IKATAN KIMIA STANDAR KOMPETENSI Memahami struktur atom, sifat-sifat periodik unsur, dan ikatan kimia KOMPETENSI DASAR Membandingkan proses pembentukan ikatan ion, ikatan kovalen, ikatan kovalen koordinasi, dan ikatan logam serta hubungannya dengan sifat fisik senyawa yang terbentuk KOMPETENSI MATERI LATIHAN EVALUASI
- 4. Mengapa dalam 1 molekul air 1 atom O berikatan dengan 2 atom H, bukan 1 atom H dan 1 atom O sehingga rumusnya HO? Apakah hakikat dari ikatan kimia tersebut? KOMPETENSI MATERI LATIHAN EVALUASI Mari temukan jawabannya dari pertanyaan tersebut !
- 5. IKATAN KIMIA MATERI PEMBELAJARAN KestabilanAtom Ikatan Ion KOMPETENSI MATERI LATIHAN EVALUASI
- 6. IKATAN KIMIA INDIKATOR Menjelaskan kecenderungan suatu unsur untuk mencapai kestabilannya. Menggambarkan susunan elektron valensi atom gas mulia (duplet dan oktet) dan elektron valensi bukan gas mulia . KOMPETENSI MATERI LATIHAN EVALUASI
- 8. IKATAN KIMIA Kestabilan Atom Atom-atom bergabung molekul ion Ikatan Kimia KOMPETENSI MATERI LATIHAN EVALUASI
- 9. IKATAN KIMIA Perhatikan konfigurasi elektron gas mulia berikut: 2 He = 2 10 Ne = 2 8 18 Ar = 2 8 8 36 Kr = 2 8 18 8 54 Xe = 2 8 18 18 8 86 Rn = 2 8 18 32 18 8 Jelas sekali susunan elektron stabil adalah 8 elektron di kulit terluar (kaidah oktet) kecuali He yang hanya 2 elektron (kaidah duplet) KOMPETENSI MATERI LATIHAN EVALUASI G.N.Lewis dan Albrecht Kossel mengaitkan kestabilan gas mulia dengan konfigurasi elektronnya.
- 10. IKATAN KIMIA Perhatikan konfigurasi elektron berikut: I A misalnya = 2 8 1 II A misalnya = 2 8 2 VI A misalnya = 2 6 VII A misalnya = 2 8 7 KOMPETENSI MATERI LATIHAN EVALUASI 11 Na 12 Mg 17 Cl 8 O
- 11. IKATAN KIMIA Konsep Ikatan Kimia pertama kali dikemukakan oleh Gilbert Newton Lewis dan Albrecht Kossel. Konsepnya adalah sebagai berikut: Gas mulia bersifat stabil karena konfigurasinya sudah oktet (Duplet untuk helium) Unsur selain gas mulia membentuk ikatan dalam rangka mencapai konfigurasi oktet KOMPETENSI MATERI LATIHAN EVALUASI CARA mencapai kestabilan?
- 12. Cara unsur selain gas mulia mencapai kestabilan adalah: 1. Serah terima elektron antar atom ikatan ion 2. Pemakaian bersama pasangan elektron ikatan kovalen IKATAN KIMIA KOMPETENSI MATERI LATIHAN EVALUASI
- 13. IKATAN KIMIA INGAT…..!! Atom dengan elektron valensi 1, 2, 3 maka atom itu melepaskan elektron (ion positif) Atom dengan elektron valensi 4,5,6,7 maka atom itu menangkap elektron (ion negatif) Atom dengan elektron valensi 8 adalah atom stabil KOMPETENSI MATERI LATIHAN EVALUASI
- 14. IKATAN KIMIA KOMPETENSI MATERI LATIHAN EVALUASI Contoh: Bagaimana kecenderungan atom Na dan Cl mencapai kestabilan? 11 Na = 2 8 1 maka untuk mencapai kestabilan akan melepas 1 elektron sehingga menjadi ion Na + 17 Cl = 2 8 7 maka untuk mencapai kestabilan akan menangkap 1 elektron sehingga menjadi ion Cl -
- 15. IKATAN KIMIA Ikatan ion Adalah ikatan yang terjadi akibat adanya serah terima elektron antar atom. Terbentuk antara atom yang melepaskan elekron (logam) dengan atom yang menangkap elektron (non logam) Atom logam melepaskan elektron ion positif Atom non logam menangkap elektron ion negatif Antara ion positif dan ion negatif terjadi tarik menarik ( gaya elektrostatis) yang disebut ikatan ion (ikatan elektrovalen) KOMPETENSI MATERI LATIHAN EVALUASI
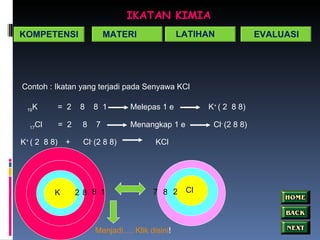
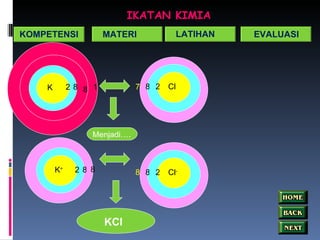
- 16. IKATAN KIMIA Contoh : Ikatan yang terjadi pada Senyawa KCl 19 K = 2 8 8 1 Melepas 1 e K + ( 2 8 8) 17 Cl = 2 8 7 Menangkap 1 e Cl - (2 8 8) K + ( 2 8 8) + Cl - (2 8 8) KCl K 2 8 1 Cl 8 2 7 Menjadi …. Klik disini ! KOMPETENSI MATERI LATIHAN EVALUASI 8
- 17. IKATAN KIMIA 8 Cl 8 2 7 Menjadi…. K + 2 8 Cl - 8 2 8 KCl KOMPETENSI MATERI LATIHAN EVALUASI K 8 2 1 8 8
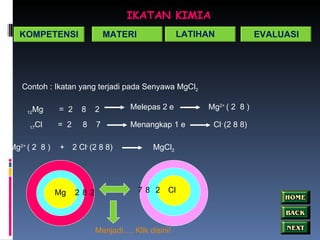
- 18. IKATAN KIMIA Contoh : Ikatan yang terjadi pada Senyawa MgCl 2 12 Mg = 2 8 2 Melepas 2 e Mg 2+ ( 2 8 ) 17 Cl = 2 8 7 Menangkap 1 e Cl - (2 8 8) Mg 2+ ( 2 8 ) + 2 Cl - (2 8 8) MgCl 2 Mg 2 8 2 Cl 8 2 7 Menjadi …. Klik disini ! KOMPETENSI MATERI LATIHAN EVALUASI
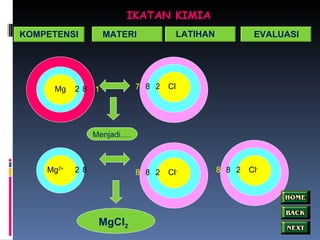
- 19. IKATAN KIMIA Mg 2 8 1 Cl 8 2 7 Menjadi…. Mg 2+ 2 8 Cl - 8 2 8 MgCl 2 Cl - 8 2 8 KOMPETENSI MATERI LATIHAN EVALUASI
- 20. Ěý