Passaggi di stato
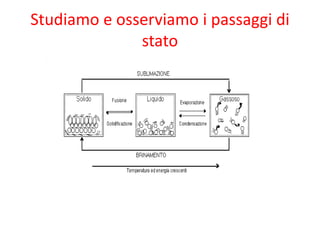
- 1. Studiamo e osserviamo i passaggi di stato
- 2. Breve ripasso Ogni elemento chimico può esistere allo stato gassoso, allo stato liquido e in quello solido. Il passaggio da uno all'altro di questi stati è detto passaggio di stato.
- 3. Stato solido: le particelle costituenti la materia sono strettamente unite una all'altra in modo piĂą o meno geometricamente ordinato. Stato liquido: le particelle hanno una energia cinetica maggiore di quella dello stato solido, possono muoversi disordinatamente ed urtarsi tra loro. Stato gassoso: le particelle si muovono in maniera caotica e le forze di coesione sono del tutto trascurabili.
- 4. Perché avviene un passaggio di stato? • Il passaggio da uno stato all’altro avviene grazie ad una variazione della Pressione , della temperatura, o di entrambe
- 5. Cosa faremo: • 1) osserveremo la sublimazione dello iodio • 2) osserveremo i passaggi di stato dell’acqua e costruiremo la curva T (°C) – t (min), fusione ed evaporazione • 3) osserveremo come cambia la temperatura di ebollizione dell’acqua se aggiungiamo del sale.
- 6. Materiali occorrenti • Iodio • Termometri • Becco bunsen • Ghiaccio • Vetreria.
- 7. 1 - sublimazione dello iodio: • 1 - In un becker perfettamente asciutto si pongono alcuni cristalli di iodio, si copre con un vetro da orologio su cui è posto, come refrigerante, un cubetto di ghiaccio; • 2 - si sottopone il becker a moderato riscaldamento sul bunsen e si osserva uno svolgimento di vapori rossastri, senza la formazione di liquido ( sublimazione ).
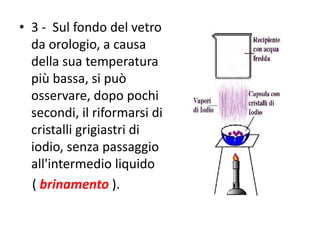
- 8. • 3 - Sul fondo del vetro da orologio, a causa della sua temperatura più bassa, si può osservare, dopo pochi secondi, il riformarsi di cristalli grigiastri di iodio, senza passaggio all'intermedio liquido ( brinamento ).
- 9. 2 - Fusione del ghiaccio: • 1 - Si pone in un becker un cubetto di ghiaccio e si osserva il passaggio ad acqua liquida che avviene a temperatura ambiente ( fusione ). • 2 - Si sottopone poi il becker a moderato riscaldamento coprendolo con un vetro da orologio; si nota la vaporizzazione dell'acqua. T (°C) t (min)
- 10. • 3 - Il vapore d'acqua subito condensa sul fondo del vetro da orologio a causa della temperatura più bassa di questo trasformandosi, nuovamente in acqua allo stato liquido. • 4 - La solidificazione a ghiaccio implicherebbe una ulteriore sottrazione di calore che può essere effettuata solo in un freezer.
- 11. Temperatura ebollizione dell’acqua salata • Ripeti le stesse osservazioni con aggiunta di sale. • Costruisci un’altra tabella e commenta i risultati. T (°C) acqua salata t (min)
- 12. 3 – Temperatura dell’ebollizione dell’acqua con aggiunta di sale • Quando sciogli in acqua del sale la temperatura di ebollizione dell’acqua diviene più elevata. • Il sale fa alzare la temperatura di ebollizione dell’acqua. • Allo stesso modo l’acqua salata non ghiaccia alla temperatura di 0°C, perché il sale fa diminuire la temperatura di congelamento.