praktikum biokimia
- 1. I. No Praktikum : 3 II. Tanggal Praktikum : 18 September 2014 III. Judul Praktikum : Reaksi Uji Protein IV. Tujuan Praktikum : Untuk menguji kandungan yang tedapat dalam protein V. Alat dan Bahan : Alat : - Pipet tetes - Rak tabung reaksi - Tabung reaksi - Beker gelas - Gelas ukur Bahan : - Larutan (NH4)2SO4 - Putih Telur 1% - 5% - Reagen millon - Larutan Ikan 1% - 5% - Kuning Telur 1% - 5 % - H2O - Asam asetat 1 M - Reagen untuk uji biuret VI. Dasar Teori Protein adalah biopolimer yang terdiri atas banyak asam amino yang berhubungan satu dengan yang lainnya lewat ikatan amida (peptida). Protein memainkan berbagai peran dalam sistem biologis. Beberapa protein merupakan komponen utama dari jaringan struktur (otot, kulit, kuku, rambut). Protein lain mengangkut molekul dari satu bagian ke bagian lain dalam makhluk hidup, ada yang bertindak sebagai katalis dalam banyak reaksi biologis yang diperlukan untuk mempertahankan hidup. Protein bersifat amfoter, yaitu dapat bereaksi dengan larutan asam dan basa. Apabila protein dipanaskan atau ditambah etanol absolut, maka protein akan menggumpal (terkoagulasi). Proses koagulasi protein timbul seiring dengan proses denaturasi. Denaturasi merupakan perubahan bentuk protein, yaitu keadaan suatu protein kehilangan fungsi biologisnya dan terjadi perubahan atau modifikasi terhadap struktur sekunder, tersier dan kuartener molekul protein tanpa terjadinya pemecahan ikatan-ikatan kovalen. Praktikum Biokimia Page 1
- 2. Protein yang terdenaturasi akan berkurang kelarutannya. Lapisan molekul bagian dalam yang bersifat hidrofobik akan keluar sedangkan bagian hidrofilik akan terlipat ke dalam. Pelipatan atau pembalikkan akan terjadi bila protein mendekati pH isoelektrik lalu protein akan menggumpal dan mengendap. Titik Isoelektrik (TI) adalah keadaan dimana protein tidak mempunyai selisih muatan atau jumlah muatan positif dan negatifnya sama, sehingga tidak bergerak ketika diletakkan dalam medan listrik. Pada pH isoelektrik (pI), suatu protein sangat mudah diendapkan karena pada saat itu muatan listriknya nol. Pada denaturasi ringan yang disebabkan oleh penambahan salah satu reagensia, ada kemungkinan rantai peptida yang telah terbentang menjadi terlipat kembali sehingga bentuk protein menyerupai semula, yang disebut renaturasi. Renaturasi adalah proses pembentukan kembali struktur untai ganda dari keadaan terdenaturasi. Renaturasi merupakan suatu proses yang dapat terjadi secara in vivo maupun in vitro. Albumin merupakan protein plasma yang paling banyak dalam tubuh manusia, yaitu sekitar 55- 60% dari protein serum yang terukur. Albumin terdiri dari rantai polipeptida tunggal dengan berat molekul 66.4 kDa dan terdiri dari 585 asam amino. Pada molekul albumin terdapat 17 ikatan dislufida yang menghubungkan asam-asam amino yang mengandung sulfur. Molekul albumin berbentuk elips sehingga bentuk molekul seperti itu tidak akan meningkkatkan viskositas plasma dan terlarut sempurna. Protein merupakan makromolekul turunan polipeptida. Protein mempunyai molekul besar antara ribuan hingga jutaan satuan (g/mol). Protein tersusun dari atom ŌĆō atom C, H, O dan N di tambah dengan beberapa unsur lainnya seperti P dan S. Atom-atom itu membentuk unit-unit asam amino. Urutan asam amino dalam protein maupun hubungan antara asam amino satu dengan yang lain, menentukan sifat biologis protein. Secara kimia dibedakan antara protein sederhana dan protein kompleks yang mengandung zat-zat makanan tambahan seperti karbohidrat, lipid atau asam nukleat. Pada protein kompleks, bagian polipeptida dinamakan approprotein dan keseluruhannya dinamakan haloprotein. Secara fungsional protein juga menunjukkan banyak perbedaan. Protein mempunyai berbagai fungsi diantaranya: merupakan katalis biokimia (enzim), alat pengangkut dan penyimpan, penunjang mekanisme tubuh, pertahanan tubuh, perambatan impuls syaraf dan pengendali pertumbuhan. Praktikum Biokimia Page 2
- 3. Struktur protein dapat dilihat sebagai hierarki yaitu berupa struktur primer (tingkat satu), struktur sekunder (tingkat dua), tersier (tingkat tiga), dan kuartener (tingkat empat). Struktur primer protein bisa ditentukan dengan beberapa metode: hidrolisis protein dengan asam kuat. Sifat-sifat protein berbeda-beda saat bereaksi dengan air, beberapa reagen dan pemanasan serta beberapa perlakuan lainnya. Kelarutan protein akan berkurang bila kedalam larutan protein ditambahkan garam-garam anorganik. Pengendapan terus terjadi karena pengendapan ion garam untuk menghidrasi, sehingga terjadi kompetisi antara garam anorganik dengan molekul protein untuk mengikat air. Garam anorganik lebih menarik air maka jumlah air yang tersedia untuk molekul protein akan berkurang. Protein yang mengandung gugus hidroksil Phenil (--OH) dapat bereaksi dengan larutan merkuri nitrat menghasilkan larutan atau endapan yang berwarna merah. Dalam suasana basa, Cu bereaksi dengan beberapa jenis larutan protein dan menghasilkan warna violet. Protein dengan penambahan asam atau pemanasan akan mengalami koagulasi. Pada pH iso-elektrik (pH larutan tertentu biasanya bekisar 4-4,5 protein mempunyai muatan positif dan negatif sama, sehingga saling menetralkan), kelarutan protein sangat menurun atau mengendap. Pada temperatur diatas 600C kelarutan protein akan berkurang karena pada temperatur yang tinggi energi kinetik molekul protein meningkat sehingga terjadi getaran yang cukup kuat untuk merusak ikatan atau struktur sekunder, tersier dan kuartener yang menyebabkan koagulasi. Protein dapat diendapkan dengan penambahan alkohol. Pelarut organik akan mengubah (mengurangi) konstanta dielektrika dari air, sehingga kelarutan protein berkurang, dan juga karena lkohol berkompetisi dengan protein terhadap air. Ada empat tingkat stuktur dasar protein, yaitu struktur primer, sekunder, tersier dan kwartener. Dan protein digolongkan dalam golongan besar, yaitu : 1. Protein sederhana : protein fiber dan protein globular 2. Protein gabungan : mukoprotein, glikoprotein, lipoprotein dan nucleoprotein Sifat ŌĆō sifat protein : 1. Ionisasi : protein yang larut dalam air akan membentuk ion yang mempunyai muatan positif dan negatif 2. Denaturasi : perubahan konformasi alamiah menjadi suatu konformasi yang tidak menentu. Praktikum Biokimia Page 3
- 4. 3. Viskositas : suatu larutan protein dalam air mempunyai viskositas atau kekentalan yang relatif lebih besar daripada viskositas air sebagai pelarutnya. 4. Kristalisasi : sering dilakukan dengan jalan penambahangaram aminosulfat atau NaCl pada larutan dengan pengaturan pH pada titik isolistriknya. 5. Sistem koloid : protein mempunyai molekul besar dan karenanya larutan protein bersifat koloid VII. Prosedur Percobaan 1. Pengendapan dengan garam Jenuhkan 10 ml larutan protein dengan ammonium sulfat. Untuk pekerjaan ini dilakukan dengan, pertama tambahkan sedikit garam tersebut. Aduk hingga melarut. Tambahkan lagi sedikit ammonium sulfat dan aduk lagi, kontinyu sehingga sedikit garam tertinggal tidak terlarut. Apabila larutan jenuh, kemudian disaring, uji kelarutan dari endapan didalam air. Uji endapan dengan reagen millon dan filtrate dengan uji biuret. 2. Uji koagulasi Tambahkan 2 tetes CH3COOH 1 M ke dalam 5 ml larutan protein. Letakkan tabung dalam air mendidih selama 5 menit. Ambil endapan dengan batang pengaduk. Uji kelarutan endapan di dalam air. Uji endapan dengan reagen millon. Praktikum Biokimia Page 4
- 5. VIII. Hasil Pengamatan 1. Uji Pengendapan dengan Garam Percobaan Hasil Pengamatan a. Larutan kuning telur ’éĘ Larutan kuning telur 1% + (NH4)2SO4 ’éĘ Endapan kuning telur 1% + reagen millon (bening tidak berwarna) ’éĘ Endapan kuning telur + H2O (bening tidak berwarna) ’éĘ Filtrat kuning telur + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Warna larutan berubah menjadi endapan merah bata ’éĘ Endapan kuning telur larut dalam air dan warna larutan tetap kuning. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan kuning telur 2% + (NH4)2SO4 ’éĘ Endapan kuning telur 2% + reagen millon (bening tidak berwarna) ’éĘ Endapan kuning telur + H2O (bening tidak berwarna) ’éĘ Filtrat kuning telur + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Warna larutan berubah menjadi endapan merah bata. ’éĘ Endapan kuning telur larut dalam air dan warna larutan tetap kuning. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan kuning telur 3% + (NH4)2SO4 ’éĘ Endapan kuning telur 3%+ reagen millon (bening tidak ’éĘ Larutan menjadi jenuh ’éĘ Warna larutan berubah menjadi endapan merah bata. Praktikum Biokimia Page 5
- 6. berwarna) ’éĘ Endapan kuning telur + H2O (bening tidak berwarna) ’éĘ Filtrat kuning telur + reagen biuret ’éĘ Endapan kuning telur larut dalam air dan warna larutan tetap kuning. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan kuning telur 4% + (NH4)2SO4 ’éĘ Endapan kuning telur 4% + reagen millon (bening tidak berwarna) ’éĘ Endapan kuning telur + H2O (bening tidak berwarna) ’éĘ Filtrat kuning telur + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Warna larutan berubah menjadi endapan merah bata. ’éĘ Endapan kuning telur larut dalam air dan warna larutan tetap kuning. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan kuning telur 5% + (NH4)2SO4 ’éĘ Endapan kuning telur 5% + reagen millon (bening tidak berwarna) ’éĘ Endapan kuning telur + H2O (bening tidak berwarna) ’éĘ Filtrat kuning telur + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Warna larutan berubah menjadi endapan merah bata. ’éĘ Endapan kuning telur larut dalam air dan warna larutan tetap kuning. ’éĘ Larutan berubah warna menjadi biru prusia. b. Larutan putih telur ’éĘ Larutan putih telur 1% + ’éĘ Larutan menjadi jenuh Praktikum Biokimia Page 6
- 7. (NH4)2SO4 ’éĘ Endapan Putih telur 1% (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan Putih telur (putih) + H2O (bening tidak berwarna) ’éĘ Filtrat Putih telur (bening) + reagen biuret ’éĘ Endapan larut dalam reagen millon dan warna larutan berubah menjadi merah bata dan terdapat gelatin. ’éĘ Endapan putih telur larut dalam air dan warna larutan menjadi putih keruh. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan putih telur 2% + (NH4)2SO4 ’éĘ Endapan Putih telur 2% (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan Putih telur (putih) + H2O (bening tidak berwarna) ’éĘ Filtrat Putih telur (bening) + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Endapan larut dalam reagen millon dan warna larutan berubah menjadi merah bata dan terdapat gelatin. ’éĘ Endapan putih telur larut dalam air dan warna larutan menjadi putih keruh. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan putih telur 4% + (NH4)2SO4 ’éĘ Endapan Putih telur 3% (putih) + reagen millon (bening tidak berwarna) ’éĘ Larutan menjadi jenuh ’éĘ Endapan larut dalam reagen millon dan warna larutan berubah menjadi merah bata dan terdapat gelatin. Praktikum Biokimia Page 7
- 8. ’éĘ Endapan Putih telur (putih) + H2O (bening tidak berwarna) ’éĘ Filtrat Putih telur (bening) + reagen biuret ’éĘ Endapan putih telur larut dalam air dan warna larutan menjadi putih keruh. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan putih telur 4% + (NH4)2SO4 ’éĘ Endapan Putih telur 4% (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan Putih telur (putih) + H2O (bening tidak berwarna) ’éĘ Filtrat Putih telur (bening) + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Endapan larut dalam reagen millon dan warna larutan berubah menjadi merah bata dan terdapat gelatin. ’éĘ Endapan putih telur larut dalam air dan warna larutan menjadi putih keruh. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan putih telur 5% + (NH4)2SO4 ’éĘ Endapan Putih telur 5% (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan Putih telur (putih) + H2O (bening tidak berwarna) ’éĘ Filtrat Putih telur (bening) + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Endapan larut dalam reagen millon dan warna larutan berubah menjadi merah bata dan terdapat gelatin. ’éĘ Endapan putih telur larut dalam air dan warna larutan menjadi putih keruh. ’éĘ Larutan berubah warna menjadi biru prusia. c. Larutan ikan Praktikum Biokimia Page 8
- 9. ’éĘ Larutan putih telur 1% + (NH4)2SO4 ’éĘ Endapan ikan 1%+ reagen millon (bening tidak berwarna) ’éĘ Endapan ikan + H2O (bening tidak berwarna) ’éĘ Filtrat ikan + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Endapan larut dalam reagen millon dan warna larutan berubah menjadi merah bata dan terdapat gelatin. ’éĘ Endapan putih telur larut dalam air dan warna larutan menjadi putih keruh. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan putih telur 2% + (NH4)2SO4 ’éĘ Endapan ikan 2% + reagen millon (bening tidak berwarna) ’éĘ Endapan ikan + H2O (bening tidak berwarna) ’éĘ Filtrat ikan + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Endapan larut dalam reagen millon dan warna larutan berubah menjadi merah bata dan terdapat gelatin. ’éĘ Endapan putih telur larut dalam air dan warna larutan menjadi putih keruh. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan putih telur 3% + (NH4)2SO4 ’éĘ Endapan ikan 3% + reagen millon (bening tidak berwarna) ’éĘ Endapan ikan + H2O (bening ’éĘ Larutan menjadi jenuh ’éĘ Endapan larut dalam reagen millon dan warna larutan berubah menjadi merah bata dan terdapat gelatin. ’éĘ Endapan putih telur larut dalam Praktikum Biokimia Page 9
- 10. tidak berwarna) ’éĘ Filtrat ikan + reagen biuret air dan warna larutan menjadi putih keruh. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan putih telur 4% + (NH4)2SO4 ’éĘ Endapan ikan 4% + reagen millon (bening tidak berwarna) ’éĘ Endapan ikan + H2O (bening tidak berwarna) ’éĘ Filtrat ikan + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Endapan larut dalam reagen millon dan warna larutan berubah menjadi merah bata dan terdapat gelatin. ’éĘ Endapan putih telur larut dalam air dan warna larutan menjadi putih keruh. ’éĘ Larutan berubah warna menjadi biru prusia. ’éĘ Larutan putih telur 5% + (NH4)2SO4 ’éĘ Endapan ikan 5% + reagen millon (bening tidak berwarna) ’éĘ Endapan ikan + H2O (bening tidak berwarna) ’éĘ Filtrat ikan + reagen biuret ’éĘ Larutan menjadi jenuh ’éĘ Endapan larut dalam reagen millon dan warna larutan berubah menjadi merah bata dan terdapat gelatin. ’éĘ Endapan putih telur larut dalam air dan warna larutan menjadi putih keruh. ’éĘ Larutan berubah warna menjadi biru prusia 2. Uji koagulasi a. Kuning telur ’éĘ Kuning telur 1% (kuning ’éĘ Larutan tidak berubah warna dan Praktikum Biokimia Page 10
- 11. bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan kuning telur (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan kuning telur (putih) + air (bening tidak berwarna) setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ Endapan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan larut dalam air tetapi tidak berubah warna. ’éĘ Kuning telur 2% (kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan kuning telur (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan kuning telur (putih) + air (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ Endapan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan larut dalam air tetapi tidak berubah warna. ’éĘ Kuning telur 3% (kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan kuning telur (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan kuning telur (putih) + air (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ Endapan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan larut dalam air tetapi tidak berubah warna. ’éĘ Kuning telur 4% (kuning bening) + larutan CH3COOH ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit Praktikum Biokimia Page 11
- 12. (bening tidak berwarna) ’éĘ Endapan kuning telur (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan kuning telur (putih) + air (bening tidak berwarna) dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ Gumpalan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Gumpalan larut dalam air tetapi tidak berubah warna. ’éĘ Kuning telur 5% (kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan kuning telur (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan kuning telur (putih) + air (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ Endapan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan larut dalam air tetapi tidak berubah warna. b. Putih telur ’éĘ Putih telur 1% (kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan putih telur (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan putih telur (putih) + air (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ endapan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan tidak larut dalam air ’éĘ Putih telur 2% (kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. Praktikum Biokimia Page 12
- 13. ’éĘ Endapan putih telur (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan putih telur (putih) + air (bening tidak berwarna) ’éĘ Endapan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan tidak larut dalam air ’éĘ Putih telur 3%(kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan putih telur (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan putih telur (putih) + air (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ Gumpalan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan tidak larut dalam air ’éĘ Putih telur 4%(kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan putih telur (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan putih telur (putih) + air (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ Endapan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan tidak larut dalam air ’éĘ Putih telur 5%(kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk gumpalan berwarna putih. Praktikum Biokimia Page 13
- 14. ’éĘ Endapan putih telur (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan putih telur (putih) + air (bening tidak berwarna) ’éĘ Endapan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan tidak larut dalam air c. Ikan ’éĘ Ikan 1%(kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan ikan (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan putih telur (putih) + air (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ Endapan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan tidak larut dalam air ’éĘ Ikan 2%(kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan ikan (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan ikan (putih) + air (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ Endapan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Endapan tidak larut dalam air ’éĘ Ikan 3%(kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan ikan (putih) + reagen millon (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk endapan berwarna putih. ’éĘ Endapan tidak larut dalam reagen millon tetapi berubah warna Praktikum Biokimia Page 14
- 15. ’éĘ Endapan ikan (putih) + air (bening tidak berwarna) menjadi merah bata. ’éĘ Endapan tidak larut dalam air ’éĘ Ikan 4%(kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan ikan (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan ikan (putih) + air (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk gumpalan berwarna putih. ’éĘ Gumpalan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Gumpalan larut dalam air tetapi tidak berubah warna. ’éĘ Ikan 5% (kuning bening) + larutan CH3COOH (bening tidak berwarna) ’éĘ Endapan ikan (putih) + reagen millon (bening tidak berwarna) ’éĘ Endapan ikan (putih) + air (bening tidak berwarna) ’éĘ Larutan tidak berubah warna dan setelah dipanaskan selama 5 menit dalam air panas, larutan berubah berbentuk gumpalan berwarna putih. ’éĘ Gumpalan tidak larut dalam reagen millon tetapi berubah warna menjadi merah bata. ’éĘ Gumpalan larut dalam air tetapi tidak berubah warna. Praktikum Biokimia Page 15
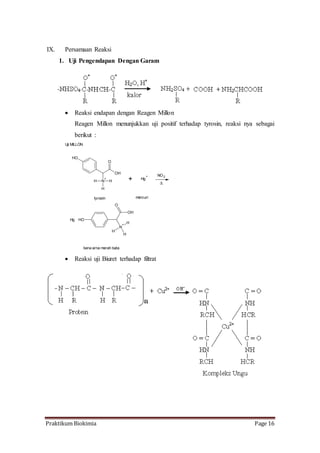
- 16. IX. Persamaan Reaksi 1. Uji Pengendapan Dengan Garam ’éĘ Reaksi endapan dengan Reagen Millon Reagen Millon menunjukkan uji positif terhadap tyrosin, reaksi nya sebagai berikut : Uji MILLON HO O OH + N H H H tyrosin + Hg + NO2 HO O OH + N H H H Hg mercuri berwarna merah bata ’üä ’éĘ Reaksi uji Biuret terhadap filtrat Praktikum Biokimia Page 16
- 17. 2. Uji Koagulasi Uji MILLON HO O OH + N H H H tyrosin + Hg + NO2 HO O OH + N H H H Hg mercuri berwarna merah bata Reaksi dengan air Air (H2O) H H H2O R ŌĆō C ŌĆō COO- R ŌĆō C ŌĆō COO- + H+ (suasana asam) N+H3 NH2 Atau H H H2O R ŌĆō C ŌĆō COO- + H+ R ŌĆō C ŌĆō COOH (suasana basa) N+H3 NH2 Praktikum Biokimia Page 17
- 18. X. Pembahasan Pada percobaan uji protein ini dilakukan berbagai macam uji, yaitu uji pengendapan dengan garam dan uji koagulasi. Pada percobaan uji pengendapan dengan garam terbentuk larutan jenuh, kemudian endapan dibagi 2 untuk uji millon dan uji air sedangkan filtratnya untuk uji biuret. Pada saat ditetsekan reagen millon dan dipanaskan hasil yang diperoleh yaitu endapan yang bewarna merah. Endapan ini menunjukkan atau merupakan hasil dari garam-garam organik dalam persentase tinggi yang dapat mempengaruhi sifat kelarutan protein. Pengendapan yang dikarenakan penambahan ammonium sulfat menyebabkan terjadi dehidrasi protein atau sering dikenal dengan kehilangan air, sehingga proses dehidrasi ini molekul protein yang mempunyai kelarutan paling kecil akan mudah mengendap. Untuk endapan dilakukan uji millon dan menghasilkan larutan dengan endapan merah, hal ini dikarenakan karena pereaksi millon adalah larutan merkuro dan merkuri nitrat dalam asam nitrit. Apabila pereaksi ini ditambahkan pada larutan protein, akan menghasilkan endapan putih yang dapat menjadi merah pada pemanasan. Pada dasarnya reaksi ini positif untuk fenol-fenol dikarenakan terbentuknya senyawa merkuri dengan gugus hidroksifenil yang bewarna, protein yang mengandung tirosin akan memberikan uji positif. Pada saat endapan ditambahkan dengan air (aquadest) maka larutan akan larut dalam air. Sedangkan pada ssat diberi reagen biuret filtratnya berubah wwarna menjadi biru pursia. Pada percobaan uji koagulasi ini dimana berdasarkan literatur jika protein ditambahkan dengan larutan asam atau basa, maka akan terdenaturasi atau terjadi penggumpalan atau terbentuk endapan. Penggumpalan / endapan ini dapat juga terjadi karena pemanasan yang dilakukan, dengan proses pemanasan struktur protein akan menjadi rusak, untuk itulah pada percobaan ini diperoleh endapan, setelah endapan diperoleh ditambahkan dengan reagen millon dan menghasilkan larutan bening dan endapan merah. Hal ini menunjukkan bahwa uji koagulasi menghasilkan positif terhadap uji millon. Pada pemanasan 40 derajat protein sudah mengalami koagulasi. Koagulasi ini terjadi bila larutan protein berada pada titik isoelektriknya. Ion-ion logam berat yang masuk ke dalam tubuh akan bereaksi dengan sebagian protein, sehingga menyebabkan terjadinya koagulasi (penggumpalan). Praktikum Biokimia Page 18
- 19. XI. Kesimpulan 1. Koagulasi dapat terjadi bila larutan protein berada pada titik isoelektriknya. Ion-ion logam berat yang masuk ke dalam tubuh akan bereaksi dengan sebagian protein, sehingga menyebabkan terjadinya koagulasi (penggumpalan). 2. Endapan yang bewarna merah pada uji pengendapan garam merupakan hasil dari garam-garam organik dalam persentase tinggi yang dapat mempengaruhi sifat kelarutan protein. 3. Pada uji pengendapan dengan garam pada saat di beri reagen millon dan dipanaskan akan mneghasilkan larutan bening dan endapan merah bata. 4. Pada uji pengendapan dengan garam, pada saat penambahan uji biuret pada filtrat akan menghasilkan warna biru pursia. 5. Endapan tidak larut dalam air pada uji koagulasi, sedangkan endapan larut pada uji pengendapan dengan garam. Praktikum Biokimia Page 19
- 20. Daftar Pustaka Anonim. 2010. Reaksi Uji protein. http://memofarmasi.blogspot.com/2010/12/reaksi-uji- protein.html. Diakses tanggal 19 September 2014 Hadi, Abdul. 2013. Pengertian, Fungsi dan Struktur Protein. http://softilmu.blogspot. com /2013/07/pengertian-dan-fungsi-protein.html. Diakses tanggal 05 September 2014. Hidayah, lutfiyatul . 2013. Pengamatan Koagulasi dan Pengendapan Protein. http://c31120065.blogspot.com/2013/06/pengamatan-koagulasi-dan-pengendapan. html. Diakses tanggal 19 September 2014 Nuraini, Hanis. 2013. Laporan Praktikum Biokimia Koagulasi dan Pengendapan Protein.http://c-31120062.blogspot.com/2013/06/laporan-praktikum-koagulasi-dan. html . Diakses tanggal 19 september 2014 Samuel, Joksan. 2013. Pengertian Protein Uji Biuret. http://joksansamuel.blogspot.com /2013/05/pengertian-protein-uji-biuret.html. Diakses tanggal 05 September 2014. Ukhtiadi. 2013. Reaksi Uji Protein. http://sitiaminahfkip.wordpress.com/2013/08/28/ reaksi-uji-protein/. Diakses tanggal 05 September 2014. Praktikum Biokimia Page 20