Reaksi penggaraman 3 KD 2 SMK-SMAK Bogor
- 1. X.9
- 3. Reaksi Penggaraman III Syarat-syarat reaksi: Reaksi dapat berlangsung asal semua syarat-syarat dibawah ini terpenuhi: 1. Garam MZ dan PQ kedua-duanya harus mudah larut dalam air. 2. Garam MQ atau PZ kedua-duanya harus sukar larut dalam air sehingga mengendap.
- 4. Reaksi Penggaraman III Contoh-contoh: AgNO3 + NaCl → AgCl↓ + NaNO3 Na2SO4 + CaCl2 → 2NaCl + CaSO4↓ MgCl2 + Pb(NO3)2 → Mg(NO3)2 + PbCl2↓
- 5. Tabel Kelarutan GARAM Kelarutan dalam air Kelaruan dalam asam encer Mudah larut Sukar larut Mudah larut Sukar larut 1. Nitrat Semua - Semua - 2. Sulfat Lain - lainnya CaSO4 Putih SrSO4 Putih BaSO4 Putih PbSO4 Putih Lain - lainnya CaSO4 SrSO4 BaSO4 PbSO4 3. Khlorida Lain - lainnya AgCl Putih Hg2Cl2 Putih PbCl2 Putih Lain - lainnya AgCl Hg2Cl2 PbCl2 4. Bromida Lain - lainnya AgBr Kuning Hg2Br2 Putih PbBr2 Putih Lain - lainnya AgBr Hg2Br2 PbBr2 5. Iodida Lain - lainnya AgI Kuning muda Hg2I2 kuning HgI2 merah PbI2 Kuning Lain - lainnya AgI Hg2I2 HgI2 PbI2 Catatan : PbCl2, PbBr2 dan PbI2 lebih mudah larut dalam air panas
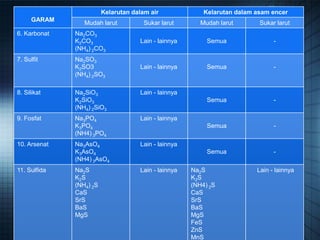
- 6. GARAM Kelarutan dalam air Kelarutan dalam asam encer Mudah larut Sukar larut Mudah larut Sukar larut 6. Karbonat Na2CO3 K2CO3 (NH4) 2CO3 Lain - lainnya Semua - 7. Sulfit Na2SO3 K2SO3 (NH4) 2SO3 Lain - lainnya Semua - 8. Silikat Na2SiO3 K2SiO3 (NH4) 2SiO3 Lain - lainnya Semua - 9. Fosfat Na3PO4 K3PO4 (NH4) 3PO4 Lain - lainnya Semua - 10. Arsenat Na3AsO4 K3AsO4 (NH4) 3AsO4 Lain - lainnya Semua - 11. Sulfida Na2S K2S (NH4) 2S CaS SrS BaS MgS Lain - lainnya Na2S K2S (NH4) 2S CaS SrS BaS MgS FeS ZnS MnS Lain - lainnya
- 7. Reaksi Penggaraman III Pada Reaksi ini, ada beberapa hal yang perlu diperhatikan: a) Apabila garam MQ dan garam PZ yang dihasilkan adalah FeI3, Fe2S3, CuI2, dan Cu(CN)2 maka garam-garam tersebut seketika terurai sebagai berikut: 2FeI3 → 2FeI2 + I2 Fe2S3 → 2FeS ↓ + S 2CuI2 → 2Cu2I2↓ + I2 2Cu(CN)2 → Cu2(CN)2 + (CN)2↑
- 8. Contoh 2FeCl3 + KI → 2FeI3 + 6KCl 2FeI2 + I2 2FeCl3 + 3Na2S → Fe2S3 + 6NaCl 2FeS↓ + S
- 9. Reaksi Penggaraman III b) Bila garam MQ atau PZ yang terbentuk itu ialah Al2(CO3)3, Al(CN)3, Al2S3, Cr(CN)3, Cr2(CO3)3, Cr2S3, Fe2(CO3)3, atau Fe(CN)3 masing-masing garam itu seketika bereaksi lagi dengan H2O sebagai berikut: Al2(CO3)3 + 6H2O → 2Al(OH)3↓ + 3H2CO3 3H2O + 3CO2↑ Cr(CN)3 + 3H2O → Cr(OH)3↓ + 3HCN↑
- 10. Contoh 2FeCl3 + 3Na2CO3 → Fe2(CO3)3 + 6NaCl Fe2(CO3)3 + 6H2O → 2Fe(OH)3 + 3H2CO3 2FeCl3 + 3Na2CO3 + 6H2O → 2Fe(OH)3↓ + 6NaCl + 3H2CO3 3H2O+3CO2↑
- 11. Reaksi Penggaraman III c) Jika salah satu garam direaksikan adalah KCN (kaliumsianida) maka garam sianida yang dihasilkan mungkin masih dapat bereaksi lagi dengan KCN berlebihan sehingga terbentuklah suatu garam kompleks. Yang masih dapat bereaksi dengan KCN adalah : AgCN, Cu2(CN)2, dan Fe(CN)2. K[Ag(CN)2] = Kalium disiano argenat (I) K3[Cu(CN)4] = Kalium tetrasiano kuprat (I) K4[Fe(CN)6] = Kalium heksasiano ferat (II)
- 12. Contoh Larutan AgNO3 + Larutan KCN berlebih AgNO3 + KCN → AgCN↓ + KNO3 AgCN + KCN → K[Ag(CN)2] AgNO3 + 2KCN → K[Ag(CN)2] + KNO3
- 13. Aplikasi Pengaplikasian Garam + Garam seperti pada praktek gravimetri dalam Penetapan Kadar SO4 2- dalam Na2SO4.10H2O Reaksinya: Na2SO4 + BaCl2 → BaSO4↓ + 2NaCl
- 14. Latihan Soal 1. REAKSIKANLAH! a. Perak Nitrat dengan Natrium Karbonat. b. Kalsium Klorida dengan Tembaga (II) Sulfat. c. Amonium Sulfida dengan Besi (III) Sulfat. d. Kalium Karbonat dengan Seng Sulfat. e. Besi (II) Sulfat dengan Kalium Sianida berlebihan. 2. Buatlah Kalsium Sulfat dari Kalsium Klorida yang hasil garamnya sukar larut keduanya.










![Reaksi Penggaraman III
c) Jika salah satu garam direaksikan adalah KCN
(kaliumsianida) maka garam sianida yang dihasilkan
mungkin masih dapat bereaksi lagi dengan KCN berlebihan
sehingga terbentuklah suatu garam kompleks. Yang masih
dapat bereaksi dengan KCN adalah : AgCN, Cu2(CN)2, dan
Fe(CN)2.
K[Ag(CN)2] = Kalium disiano argenat (I)
K3[Cu(CN)4] = Kalium tetrasiano kuprat (I)
K4[Fe(CN)6] = Kalium heksasiano ferat (II)](https://image.slidesharecdn.com/reaksipenggaramaniii-161028224006/85/Reaksi-penggaraman-3-KD-2-SMK-SMAK-Bogor-11-320.jpg)
![Contoh
Larutan AgNO3 + Larutan KCN berlebih
AgNO3 + KCN → AgCN↓ + KNO3
AgCN + KCN → K[Ag(CN)2]
AgNO3 + 2KCN → K[Ag(CN)2] + KNO3](https://image.slidesharecdn.com/reaksipenggaramaniii-161028224006/85/Reaksi-penggaraman-3-KD-2-SMK-SMAK-Bogor-12-320.jpg)


