1 of 17
Downloaded 18 times












Recommended
Atomul. Structura atomului



Atomul. Structura atomuluiconstantinalucretia
Ã˝
- definitia atomului, respectiv a elementului chimic
- structura atomului
- nucleul atomului; protonul si neutronul
- invelisul electronic al atomilor; electronul
- structura invelisului electronic
ocuparea straturilor electonice cu electroniAtomul.....



Atomul.....Negotei Elena
Ã˝
Termenul de atom apare pentru prima dată către anul 450 î.e.n. Filozoful grec Leucip dezvoltă teoria conform căreia materia nu este infinit divizibilă și introduce noțiunea de atomos, ceea ce nu poate fi divizat. Câțiva ani mai târziu, Democrit, un discipol al lui Leucip, definește materia ca fiind un ansamblu de particule indivizibile, invizibile și eterne: atomul. Această nouă concepție nu a fost rezultatul unor observații sau experiențe, ci mai degrabă al unor intuiții. Teoria a fost dezvoltată ulterior de Epicur, apoi de poetul latin Lucrețiu. Au trecut însă 2000 de ani până când teoria atomică a fost formulată științific.2024 Trend Updates: What Really Works In SEO & Content Marketing



2024 Trend Updates: What Really Works In SEO & Content MarketingSearch Engine Journal
Ã˝
The future of SEO is trending toward a more human-first and user-centric approach, powered by AI intelligence and collaboration. Are you ready?
Watch as we explore which SEO trends to prioritize to achieve sustainable growth and deliver reliable results. We’ll dive into best practices to adapt your strategy around industry-wide disruptions like SGE, how to navigate the top challenges SEO professionals are facing, and proven tactics for prioritizing quality and building trust.
You’ll hear:
- The top SEO trends to prioritize in 2024 to achieve long-term success.
- Predictions for SGE’s impact, and how to adapt.
- What E-E-A-T really means, and how to implement it holistically (hint: it’s never been more important).
With Zack Kadish and Alex Carchietta, we’ll show you which SEO trends to ignore and which to focus on, along with the solution to overcoming rapid, significant and disruptive Google algorithm updates.
If you’re looking to cut through the noise of constant SEO and content trends to drive success, you won’t want to miss this webinar.
Storytelling For The Web: Integrate Storytelling in your Design Process



Storytelling For The Web: Integrate Storytelling in your Design ProcessChiara Aliotta
Ã˝
In this slides I explain how I have used storytelling techniques to elevate websites and brands and create memorable user experiences. You can discover practical tips as I showcase the elements of good storytelling and its applied to some examples of diverse brands/projects..Artificial Intelligence, Data and Competition – SCHREPEL – June 2024 OECD dis...



Artificial Intelligence, Data and Competition – SCHREPEL – June 2024 OECD dis...OECD Directorate for Financial and Enterprise Affairs
Ã˝
This presentation by Thibault Schrepel, Associate Professor of Law at Vrije Universiteit Amsterdam University, was made during the discussion “Artificial Intelligence, Data and Competition” held at the 143rd meeting of the OECD Competition Committee on 12 June 2024. More papers and presentations on the topic can be found at oe.cd/aicomp.
This presentation was uploaded with the author’s consent.
How to Leverage AI to Boost Employee Wellness - Lydia Di Francesco - SocialHR...



How to Leverage AI to Boost Employee Wellness - Lydia Di Francesco - SocialHR...SocialHRCamp
Ã˝
Speaker: Lydia Di Francesco
In this workshop, participants will delve into the realm of AI and its profound potential to revolutionize employee wellness initiatives. From stress management to fostering work-life harmony, AI offers a myriad of innovative tools and strategies that can significantly enhance the wellbeing of employees in any organization. Attendees will learn how to effectively leverage AI technologies to cultivate a healthier, happier, and more productive workforce. Whether it's utilizing AI-powered chatbots for mental health support, implementing data analytics to identify internal, systemic risk factors, or deploying personalized wellness apps, this workshop will equip participants with actionable insights and best practices to harness the power of AI for boosting employee wellness. Join us and discover how AI can be a strategic partner towards a culture of wellbeing and resilience in the workplace.2024 State of Marketing Report – by Hubspot



2024 State of Marketing Report – by HubspotMarius Sescu
Ã˝
https://www.hubspot.com/state-of-marketing
· Scaling relationships and proving ROI
· Social media is the place for search, sales, and service
· Authentic influencer partnerships fuel brand growth
· The strongest connections happen via call, click, chat, and camera.
· Time saved with AI leads to more creative work
· Seeking: A single source of truth
· TLDR; Get on social, try AI, and align your systems.
· More human marketing, powered by robotsEverything You Need To Know About ChatGPT



Everything You Need To Know About ChatGPTExpeed Software
Ã˝
ChatGPT is a revolutionary addition to the world since its introduction in 2022. A big shift in the sector of information gathering and processing happened because of this chatbot. What is the story of ChatGPT? How is the bot responding to prompts and generating contents? Swipe through these slides prepared by Expeed Software, a web development company regarding the development and technical intricacies of ChatGPT!Product Design Trends in 2024 | Teenage Engineerings



Product Design Trends in 2024 | Teenage EngineeringsPixeldarts
Ã˝
The realm of product design is a constantly changing environment where technology and style intersect. Every year introduces fresh challenges and exciting trends that mold the future of this captivating art form. In this piece, we delve into the significant trends set to influence the look and functionality of product design in the year 2024.How Race, Age and Gender Shape Attitudes Towards Mental Health



How Race, Age and Gender Shape Attitudes Towards Mental HealthThinkNow
Ã˝
Mental health has been in the news quite a bit lately. Dozens of U.S. states are currently suing Meta for contributing to the youth mental health crisis by inserting addictive features into their products, while the U.S. Surgeon General is touring the nation to bring awareness to the growing epidemic of loneliness and isolation. The country has endured periods of low national morale, such as in the 1970s when high inflation and the energy crisis worsened public sentiment following the Vietnam War. The current mood, however, feels different. Gallup recently reported that national mental health is at an all-time low, with few bright spots to lift spirits.
To better understand how Americans are feeling and their attitudes towards mental health in general, ThinkNow conducted a nationally representative quantitative survey of 1,500 respondents and found some interesting differences among ethnic, age and gender groups.
Technology
For example, 52% agree that technology and social media have a negative impact on mental health, but when broken out by race, 61% of Whites felt technology had a negative effect, and only 48% of Hispanics thought it did.
While technology has helped us keep in touch with friends and family in faraway places, it appears to have degraded our ability to connect in person. Staying connected online is a double-edged sword since the same news feed that brings us pictures of the grandkids and fluffy kittens also feeds us news about the wars in Israel and Ukraine, the dysfunction in Washington, the latest mass shooting and the climate crisis.
Hispanics may have a built-in defense against the isolation technology breeds, owing to their large, multigenerational households, strong social support systems, and tendency to use social media to stay connected with relatives abroad.
Age and Gender
When asked how individuals rate their mental health, men rate it higher than women by 11 percentage points, and Baby Boomers rank it highest at 83%, saying it’s good or excellent vs. 57% of Gen Z saying the same.
Gen Z spends the most amount of time on social media, so the notion that social media negatively affects mental health appears to be correlated. Unfortunately, Gen Z is also the generation that’s least comfortable discussing mental health concerns with healthcare professionals. Only 40% of them state they’re comfortable discussing their issues with a professional compared to 60% of Millennials and 65% of Boomers.
Race Affects Attitudes
As seen in previous research conducted by ThinkNow, Asian Americans lag other groups when it comes to awareness of mental health issues. Twenty-four percent of Asian Americans believe that having a mental health issue is a sign of weakness compared to the 16% average for all groups. Asians are also considerably less likely to be aware of mental health services in their communities (42% vs. 55%) and most likely to seek out information on social media (51% vs. 35%).AI Trends in Creative Operations 2024 by Artwork Flow.pdf



AI Trends in Creative Operations 2024 by Artwork Flow.pdfmarketingartwork
Ã˝
Creative operations teams expect increased AI use in 2024. Currently, over half of tasks are not AI-enabled, but this is expected to decrease in the coming year. ChatGPT is the most popular AI tool currently. Business leaders are more actively exploring AI benefits than individual contributors. Most respondents do not believe AI will impact workforce size in 2024. However, some inhibitions still exist around AI accuracy and lack of understanding. Creatives primarily want to use AI to save time on mundane tasks and boost productivity.Skeleton Culture Code



Skeleton Culture CodeSkeleton Technologies
Ã˝
Organizational culture includes values, norms, systems, symbols, language, assumptions, beliefs, and habits that influence employee behaviors and how people interpret those behaviors. It is important because culture can help or hinder a company's success. Some key aspects of Netflix's culture that help it achieve results include hiring smartly so every position has stars, focusing on attitude over just aptitude, and having a strict policy against peacocks, whiners, and jerks.PEPSICO Presentation to CAGNY Conference Feb 2024



PEPSICO Presentation to CAGNY Conference Feb 2024Neil Kimberley
Ã˝
PepsiCo provided a safe harbor statement noting that any forward-looking statements are based on currently available information and are subject to risks and uncertainties. It also provided information on non-GAAP measures and directing readers to its website for disclosure and reconciliation. The document then discussed PepsiCo's business overview, including that it is a global beverage and convenient food company with iconic brands, $91 billion in net revenue in 2023, and nearly $14 billion in core operating profit. It operates through a divisional structure with a focus on local consumers.Content Methodology: A Best Practices Report (Webinar)



Content Methodology: A Best Practices Report (Webinar)contently
Ã˝
This document provides an overview of content methodology best practices. It defines content methodology as establishing objectives, KPIs, and a culture of continuous learning and iteration. An effective methodology focuses on connecting with audiences, creating optimal content, and optimizing processes. It also discusses why a methodology is needed due to the competitive landscape, proliferation of channels, and opportunities for improvement. Components of an effective methodology include defining objectives and KPIs, audience analysis, identifying opportunities, and evaluating resources. The document concludes with recommendations around creating a content plan, testing and optimizing content over 90 days.How to Prepare For a Successful Job Search for 2024



How to Prepare For a Successful Job Search for 2024Albert Qian
Ã˝
The document provides guidance on preparing a job search for 2024. It discusses the state of the job market, focusing on growth in AI and healthcare but also continued layoffs. It recommends figuring out what you want to do by researching interests and skills, then conducting informational interviews. The job search should involve building a personal brand on LinkedIn, actively applying to jobs, tailoring resumes and interviews, maintaining job hunting as a habit, and continuing self-improvement. Once hired, the document advises setting new goals and keeping skills and networking active in case of future opportunities.Social Media Marketing Trends 2024 // The Global Indie Insights



Social Media Marketing Trends 2024 // The Global Indie InsightsKurio // The Social Media Age(ncy)
Ã˝
A report by thenetworkone and Kurio.
The contributing experts and agencies are (in an alphabetical order): Sylwia Rytel, Social Media Supervisor, 180heartbeats + JUNG v MATT (PL), Sharlene Jenner, Vice President - Director of Engagement Strategy, Abelson Taylor (USA), Alex Casanovas, Digital Director, Atrevia (ES), Dora Beilin, Senior Social Strategist, Barrett Hoffher (USA), Min Seo, Campaign Director, Brand New Agency (KR), Deshé M. Gully, Associate Strategist, Day One Agency (USA), Francesca Trevisan, Strategist, Different (IT), Trevor Crossman, CX and Digital Transformation Director; Olivia Hussey, Strategic Planner; Simi Srinarula, Social Media Manager, The Hallway (AUS), James Hebbert, Managing Director, Hylink (CN / UK), Mundy Álvarez, Planning Director; Pedro Rojas, Social Media Manager; Pancho González, CCO, Inbrax (CH), Oana Oprea, Head of Digital Planning, Jam Session Agency (RO), Amy Bottrill, Social Account Director, Launch (UK), Gaby Arriaga, Founder, Leonardo1452 (MX), Shantesh S Row, Creative Director, Liwa (UAE), Rajesh Mehta, Chief Strategy Officer; Dhruv Gaur, Digital Planning Lead; Leonie Mergulhao, Account Supervisor - Social Media & PR, Medulla (IN), Aurelija Plioplytė, Head of Digital & Social, Not Perfect (LI), Daiana Khaidargaliyeva, Account Manager, Osaka Labs (UK / USA), Stefanie Söhnchen, Vice President Digital, PIABO Communications (DE), Elisabeth Winiartati, Managing Consultant, Head of Global Integrated Communications; Lydia Aprina, Account Manager, Integrated Marketing and Communications; Nita Prabowo, Account Manager, Integrated Marketing and Communications; Okhi, Web Developer, PNTR Group (ID), Kei Obusan, Insights Director; Daffi Ranandi, Insights Manager, Radarr (SG), Gautam Reghunath, Co-founder & CEO, Talented (IN), Donagh Humphreys, Head of Social and Digital Innovation, THINKHOUSE (IRE), Sarah Yim, Strategy Director, Zulu Alpha Kilo (CA).Trends In Paid Search: Navigating The Digital Landscape In 2024



Trends In Paid Search: Navigating The Digital Landscape In 2024Search Engine Journal
Ã˝
The search marketing landscape is evolving rapidly with new technologies, and professionals, like you, rely on innovative paid search strategies to meet changing demands.
It’s important that you’re ready to implement new strategies in 2024.
Check this out and learn the top trends in paid search advertising that are expected to gain traction, so you can drive higher ROI more efficiently in 2024.
You’ll learn:
- The latest trends in AI and automation, and what this means for an evolving paid search ecosystem.
- New developments in privacy and data regulation.
- Emerging ad formats that are expected to make an impact next year.
Watch Sreekant Lanka from iQuanti and Irina Klein from OneMain Financial as they dive into the future of paid search and explore the trends, strategies, and technologies that will shape the search marketing landscape.
If you’re looking to assess your paid search strategy and design an industry-aligned plan for 2024, then this webinar is for you.5 Public speaking tips from TED - Visualized summary



5 Public speaking tips from TED - Visualized summarySpeakerHub
Ã˝
From their humble beginnings in 1984, TED has grown into the world’s most powerful amplifier for speakers and thought-leaders to share their ideas. They have over 2,400 filmed talks (not including the 30,000+ TEDx videos) freely available online, and have hosted over 17,500 events around the world.
With over one billion views in a year, it’s no wonder that so many speakers are looking to TED for ideas on how to share their message more effectively.
The article “5 Public-Speaking Tips TED Gives Its Speakers”, by Carmine Gallo for Forbes, gives speakers five practical ways to connect with their audience, and effectively share their ideas on stage.
Whether you are gearing up to get on a TED stage yourself, or just want to master the skills that so many of their speakers possess, these tips and quotes from Chris Anderson, the TED Talks Curator, will encourage you to make the most impactful impression on your audience.
See the full article and more summaries like this on SpeakerHub here: https://speakerhub.com/blog/5-presentation-tips-ted-gives-its-speakers
See the original article on Forbes here:
http://www.forbes.com/forbes/welcome/?toURL=http://www.forbes.com/sites/carminegallo/2016/05/06/5-public-speaking-tips-ted-gives-its-speakers/&refURL=&referrer=#5c07a8221d9bChatGPT and the Future of Work - Clark Boyd 



ChatGPT and the Future of Work - Clark Boyd Clark Boyd
Ã˝
Everyone is in agreement that ChatGPT (and other generative AI tools) will shape the future of work. Yet there is little consensus on exactly how, when, and to what extent this technology will change our world.
Businesses that extract maximum value from ChatGPT will use it as a collaborative tool for everything from brainstorming to technical maintenance.
For individuals, now is the time to pinpoint the skills the future professional will need to thrive in the AI age.
Check out this presentation to understand what ChatGPT is, how it will shape the future of work, and how you can prepare to take advantage. Getting into the tech field. what next 



Getting into the tech field. what next Tessa Mero
Ã˝
The document provides career advice for getting into the tech field, including:
- Doing projects and internships in college to build a portfolio.
- Learning about different roles and technologies through industry research.
- Contributing to open source projects to build experience and network.
- Developing a personal brand through a website and social media presence.
- Networking through events, communities, and finding a mentor.
- Practicing interviews through mock interviews and whiteboarding coding questions.Google's Just Not That Into You: Understanding Core Updates & Search Intent



Google's Just Not That Into You: Understanding Core Updates & Search IntentLily Ray
Ã˝
1. Core updates from Google periodically change how its algorithms assess and rank websites and pages. This can impact rankings through shifts in user intent, site quality issues being caught up to, world events influencing queries, and overhauls to search like the E-A-T framework.
2. There are many possible user intents beyond just transactional, navigational and informational. Identifying intent shifts is important during core updates. Sites may need to optimize for new intents through different content types and sections.
3. Responding effectively to core updates requires analyzing "before and after" data to understand changes, identifying new intents or page types, and ensuring content matches appropriate intents across video, images, knowledge graphs and more.How to have difficult conversations 



How to have difficult conversations Rajiv Jayarajah, MAppComm, ACC
Ã˝
Stop putting off having difficult conversations. Seven practical tips to ensure your next difficult conversation go smoothly. Introduction to Data Science



Introduction to Data ScienceChristy Abraham Joy
Ã˝
A brief introduction to DataScience with explaining of the concepts, algorithms, machine learning, supervised and unsupervised learning, clustering, statistics, data preprocessing, real-world applications etc.
It's part of a Data Science Corner Campaign where I will be discussing the fundamentals of DataScience, AIML, Statistics etc.Time Management & Productivity - Best Practices



Time Management & Productivity - Best PracticesVit Horky
Ã˝
Here's my presentation on by proven best practices how to manage your work time effectively and how to improve your productivity. It includes practical tips and how to use tools such as Slack, Google Apps, Hubspot, Google Calendar, Gmail and others.The six step guide to practical project management



The six step guide to practical project managementMindGenius
Ã˝
The six step guide to practical project management
If you think managing projects is too difficult, think again.
We’ve stripped back project management processes to the
basics – to make it quicker and easier, without sacrificing
the vital ingredients for success.
“If you’re looking for some real-world guidance, then The Six Step Guide to Practical Project Management will help.”
Dr Andrew Makar, Tactical Project ManagementBeginners Guide to TikTok for Search - Rachel Pearson - We are Tilt __ Bright...



Beginners Guide to TikTok for Search - Rachel Pearson - We are Tilt __ Bright...RachelPearson36
Ã˝
A presentation for absolute beginners who have never touched TikTok and may be a bit scared of it!Unlocking the Power of ChatGPT and AI in Testing - A Real-World Look, present...



Unlocking the Power of ChatGPT and AI in Testing - A Real-World Look, present...Applitools
Ã˝
During this webinar, Anand Bagmar demonstrates how AI tools such as ChatGPT can be applied to various stages of the software development life cycle (SDLC) using an eCommerce application case study. Find the on-demand recording and more info at https://applitools.info/b59
Key takeaways:
• Learn how to use ChatGPT to add AI power to your testing and test automation
• Understand the limitations of the technology and where human expertise is crucial
• Gain insight into different AI-based tools
• Adopt AI-based tools to stay relevant and optimize work for developers and testers
* ChatGPT and OpenAI belong to OpenAI, L.L.C.More Related Content
Featured (20)
Everything You Need To Know About ChatGPT



Everything You Need To Know About ChatGPTExpeed Software
Ã˝
ChatGPT is a revolutionary addition to the world since its introduction in 2022. A big shift in the sector of information gathering and processing happened because of this chatbot. What is the story of ChatGPT? How is the bot responding to prompts and generating contents? Swipe through these slides prepared by Expeed Software, a web development company regarding the development and technical intricacies of ChatGPT!Product Design Trends in 2024 | Teenage Engineerings



Product Design Trends in 2024 | Teenage EngineeringsPixeldarts
Ã˝
The realm of product design is a constantly changing environment where technology and style intersect. Every year introduces fresh challenges and exciting trends that mold the future of this captivating art form. In this piece, we delve into the significant trends set to influence the look and functionality of product design in the year 2024.How Race, Age and Gender Shape Attitudes Towards Mental Health



How Race, Age and Gender Shape Attitudes Towards Mental HealthThinkNow
Ã˝
Mental health has been in the news quite a bit lately. Dozens of U.S. states are currently suing Meta for contributing to the youth mental health crisis by inserting addictive features into their products, while the U.S. Surgeon General is touring the nation to bring awareness to the growing epidemic of loneliness and isolation. The country has endured periods of low national morale, such as in the 1970s when high inflation and the energy crisis worsened public sentiment following the Vietnam War. The current mood, however, feels different. Gallup recently reported that national mental health is at an all-time low, with few bright spots to lift spirits.
To better understand how Americans are feeling and their attitudes towards mental health in general, ThinkNow conducted a nationally representative quantitative survey of 1,500 respondents and found some interesting differences among ethnic, age and gender groups.
Technology
For example, 52% agree that technology and social media have a negative impact on mental health, but when broken out by race, 61% of Whites felt technology had a negative effect, and only 48% of Hispanics thought it did.
While technology has helped us keep in touch with friends and family in faraway places, it appears to have degraded our ability to connect in person. Staying connected online is a double-edged sword since the same news feed that brings us pictures of the grandkids and fluffy kittens also feeds us news about the wars in Israel and Ukraine, the dysfunction in Washington, the latest mass shooting and the climate crisis.
Hispanics may have a built-in defense against the isolation technology breeds, owing to their large, multigenerational households, strong social support systems, and tendency to use social media to stay connected with relatives abroad.
Age and Gender
When asked how individuals rate their mental health, men rate it higher than women by 11 percentage points, and Baby Boomers rank it highest at 83%, saying it’s good or excellent vs. 57% of Gen Z saying the same.
Gen Z spends the most amount of time on social media, so the notion that social media negatively affects mental health appears to be correlated. Unfortunately, Gen Z is also the generation that’s least comfortable discussing mental health concerns with healthcare professionals. Only 40% of them state they’re comfortable discussing their issues with a professional compared to 60% of Millennials and 65% of Boomers.
Race Affects Attitudes
As seen in previous research conducted by ThinkNow, Asian Americans lag other groups when it comes to awareness of mental health issues. Twenty-four percent of Asian Americans believe that having a mental health issue is a sign of weakness compared to the 16% average for all groups. Asians are also considerably less likely to be aware of mental health services in their communities (42% vs. 55%) and most likely to seek out information on social media (51% vs. 35%).AI Trends in Creative Operations 2024 by Artwork Flow.pdf



AI Trends in Creative Operations 2024 by Artwork Flow.pdfmarketingartwork
Ã˝
Creative operations teams expect increased AI use in 2024. Currently, over half of tasks are not AI-enabled, but this is expected to decrease in the coming year. ChatGPT is the most popular AI tool currently. Business leaders are more actively exploring AI benefits than individual contributors. Most respondents do not believe AI will impact workforce size in 2024. However, some inhibitions still exist around AI accuracy and lack of understanding. Creatives primarily want to use AI to save time on mundane tasks and boost productivity.Skeleton Culture Code



Skeleton Culture CodeSkeleton Technologies
Ã˝
Organizational culture includes values, norms, systems, symbols, language, assumptions, beliefs, and habits that influence employee behaviors and how people interpret those behaviors. It is important because culture can help or hinder a company's success. Some key aspects of Netflix's culture that help it achieve results include hiring smartly so every position has stars, focusing on attitude over just aptitude, and having a strict policy against peacocks, whiners, and jerks.PEPSICO Presentation to CAGNY Conference Feb 2024



PEPSICO Presentation to CAGNY Conference Feb 2024Neil Kimberley
Ã˝
PepsiCo provided a safe harbor statement noting that any forward-looking statements are based on currently available information and are subject to risks and uncertainties. It also provided information on non-GAAP measures and directing readers to its website for disclosure and reconciliation. The document then discussed PepsiCo's business overview, including that it is a global beverage and convenient food company with iconic brands, $91 billion in net revenue in 2023, and nearly $14 billion in core operating profit. It operates through a divisional structure with a focus on local consumers.Content Methodology: A Best Practices Report (Webinar)



Content Methodology: A Best Practices Report (Webinar)contently
Ã˝
This document provides an overview of content methodology best practices. It defines content methodology as establishing objectives, KPIs, and a culture of continuous learning and iteration. An effective methodology focuses on connecting with audiences, creating optimal content, and optimizing processes. It also discusses why a methodology is needed due to the competitive landscape, proliferation of channels, and opportunities for improvement. Components of an effective methodology include defining objectives and KPIs, audience analysis, identifying opportunities, and evaluating resources. The document concludes with recommendations around creating a content plan, testing and optimizing content over 90 days.How to Prepare For a Successful Job Search for 2024



How to Prepare For a Successful Job Search for 2024Albert Qian
Ã˝
The document provides guidance on preparing a job search for 2024. It discusses the state of the job market, focusing on growth in AI and healthcare but also continued layoffs. It recommends figuring out what you want to do by researching interests and skills, then conducting informational interviews. The job search should involve building a personal brand on LinkedIn, actively applying to jobs, tailoring resumes and interviews, maintaining job hunting as a habit, and continuing self-improvement. Once hired, the document advises setting new goals and keeping skills and networking active in case of future opportunities.Social Media Marketing Trends 2024 // The Global Indie Insights



Social Media Marketing Trends 2024 // The Global Indie InsightsKurio // The Social Media Age(ncy)
Ã˝
A report by thenetworkone and Kurio.
The contributing experts and agencies are (in an alphabetical order): Sylwia Rytel, Social Media Supervisor, 180heartbeats + JUNG v MATT (PL), Sharlene Jenner, Vice President - Director of Engagement Strategy, Abelson Taylor (USA), Alex Casanovas, Digital Director, Atrevia (ES), Dora Beilin, Senior Social Strategist, Barrett Hoffher (USA), Min Seo, Campaign Director, Brand New Agency (KR), Deshé M. Gully, Associate Strategist, Day One Agency (USA), Francesca Trevisan, Strategist, Different (IT), Trevor Crossman, CX and Digital Transformation Director; Olivia Hussey, Strategic Planner; Simi Srinarula, Social Media Manager, The Hallway (AUS), James Hebbert, Managing Director, Hylink (CN / UK), Mundy Álvarez, Planning Director; Pedro Rojas, Social Media Manager; Pancho González, CCO, Inbrax (CH), Oana Oprea, Head of Digital Planning, Jam Session Agency (RO), Amy Bottrill, Social Account Director, Launch (UK), Gaby Arriaga, Founder, Leonardo1452 (MX), Shantesh S Row, Creative Director, Liwa (UAE), Rajesh Mehta, Chief Strategy Officer; Dhruv Gaur, Digital Planning Lead; Leonie Mergulhao, Account Supervisor - Social Media & PR, Medulla (IN), Aurelija Plioplytė, Head of Digital & Social, Not Perfect (LI), Daiana Khaidargaliyeva, Account Manager, Osaka Labs (UK / USA), Stefanie Söhnchen, Vice President Digital, PIABO Communications (DE), Elisabeth Winiartati, Managing Consultant, Head of Global Integrated Communications; Lydia Aprina, Account Manager, Integrated Marketing and Communications; Nita Prabowo, Account Manager, Integrated Marketing and Communications; Okhi, Web Developer, PNTR Group (ID), Kei Obusan, Insights Director; Daffi Ranandi, Insights Manager, Radarr (SG), Gautam Reghunath, Co-founder & CEO, Talented (IN), Donagh Humphreys, Head of Social and Digital Innovation, THINKHOUSE (IRE), Sarah Yim, Strategy Director, Zulu Alpha Kilo (CA).Trends In Paid Search: Navigating The Digital Landscape In 2024



Trends In Paid Search: Navigating The Digital Landscape In 2024Search Engine Journal
Ã˝
The search marketing landscape is evolving rapidly with new technologies, and professionals, like you, rely on innovative paid search strategies to meet changing demands.
It’s important that you’re ready to implement new strategies in 2024.
Check this out and learn the top trends in paid search advertising that are expected to gain traction, so you can drive higher ROI more efficiently in 2024.
You’ll learn:
- The latest trends in AI and automation, and what this means for an evolving paid search ecosystem.
- New developments in privacy and data regulation.
- Emerging ad formats that are expected to make an impact next year.
Watch Sreekant Lanka from iQuanti and Irina Klein from OneMain Financial as they dive into the future of paid search and explore the trends, strategies, and technologies that will shape the search marketing landscape.
If you’re looking to assess your paid search strategy and design an industry-aligned plan for 2024, then this webinar is for you.5 Public speaking tips from TED - Visualized summary



5 Public speaking tips from TED - Visualized summarySpeakerHub
Ã˝
From their humble beginnings in 1984, TED has grown into the world’s most powerful amplifier for speakers and thought-leaders to share their ideas. They have over 2,400 filmed talks (not including the 30,000+ TEDx videos) freely available online, and have hosted over 17,500 events around the world.
With over one billion views in a year, it’s no wonder that so many speakers are looking to TED for ideas on how to share their message more effectively.
The article “5 Public-Speaking Tips TED Gives Its Speakers”, by Carmine Gallo for Forbes, gives speakers five practical ways to connect with their audience, and effectively share their ideas on stage.
Whether you are gearing up to get on a TED stage yourself, or just want to master the skills that so many of their speakers possess, these tips and quotes from Chris Anderson, the TED Talks Curator, will encourage you to make the most impactful impression on your audience.
See the full article and more summaries like this on SpeakerHub here: https://speakerhub.com/blog/5-presentation-tips-ted-gives-its-speakers
See the original article on Forbes here:
http://www.forbes.com/forbes/welcome/?toURL=http://www.forbes.com/sites/carminegallo/2016/05/06/5-public-speaking-tips-ted-gives-its-speakers/&refURL=&referrer=#5c07a8221d9bChatGPT and the Future of Work - Clark Boyd 



ChatGPT and the Future of Work - Clark Boyd Clark Boyd
Ã˝
Everyone is in agreement that ChatGPT (and other generative AI tools) will shape the future of work. Yet there is little consensus on exactly how, when, and to what extent this technology will change our world.
Businesses that extract maximum value from ChatGPT will use it as a collaborative tool for everything from brainstorming to technical maintenance.
For individuals, now is the time to pinpoint the skills the future professional will need to thrive in the AI age.
Check out this presentation to understand what ChatGPT is, how it will shape the future of work, and how you can prepare to take advantage. Getting into the tech field. what next 



Getting into the tech field. what next Tessa Mero
Ã˝
The document provides career advice for getting into the tech field, including:
- Doing projects and internships in college to build a portfolio.
- Learning about different roles and technologies through industry research.
- Contributing to open source projects to build experience and network.
- Developing a personal brand through a website and social media presence.
- Networking through events, communities, and finding a mentor.
- Practicing interviews through mock interviews and whiteboarding coding questions.Google's Just Not That Into You: Understanding Core Updates & Search Intent



Google's Just Not That Into You: Understanding Core Updates & Search IntentLily Ray
Ã˝
1. Core updates from Google periodically change how its algorithms assess and rank websites and pages. This can impact rankings through shifts in user intent, site quality issues being caught up to, world events influencing queries, and overhauls to search like the E-A-T framework.
2. There are many possible user intents beyond just transactional, navigational and informational. Identifying intent shifts is important during core updates. Sites may need to optimize for new intents through different content types and sections.
3. Responding effectively to core updates requires analyzing "before and after" data to understand changes, identifying new intents or page types, and ensuring content matches appropriate intents across video, images, knowledge graphs and more.How to have difficult conversations 



How to have difficult conversations Rajiv Jayarajah, MAppComm, ACC
Ã˝
Stop putting off having difficult conversations. Seven practical tips to ensure your next difficult conversation go smoothly. Introduction to Data Science



Introduction to Data ScienceChristy Abraham Joy
Ã˝
A brief introduction to DataScience with explaining of the concepts, algorithms, machine learning, supervised and unsupervised learning, clustering, statistics, data preprocessing, real-world applications etc.
It's part of a Data Science Corner Campaign where I will be discussing the fundamentals of DataScience, AIML, Statistics etc.Time Management & Productivity - Best Practices



Time Management & Productivity - Best PracticesVit Horky
Ã˝
Here's my presentation on by proven best practices how to manage your work time effectively and how to improve your productivity. It includes practical tips and how to use tools such as Slack, Google Apps, Hubspot, Google Calendar, Gmail and others.The six step guide to practical project management



The six step guide to practical project managementMindGenius
Ã˝
The six step guide to practical project management
If you think managing projects is too difficult, think again.
We’ve stripped back project management processes to the
basics – to make it quicker and easier, without sacrificing
the vital ingredients for success.
“If you’re looking for some real-world guidance, then The Six Step Guide to Practical Project Management will help.”
Dr Andrew Makar, Tactical Project ManagementBeginners Guide to TikTok for Search - Rachel Pearson - We are Tilt __ Bright...



Beginners Guide to TikTok for Search - Rachel Pearson - We are Tilt __ Bright...RachelPearson36
Ã˝
A presentation for absolute beginners who have never touched TikTok and may be a bit scared of it!Unlocking the Power of ChatGPT and AI in Testing - A Real-World Look, present...



Unlocking the Power of ChatGPT and AI in Testing - A Real-World Look, present...Applitools
Ã˝
During this webinar, Anand Bagmar demonstrates how AI tools such as ChatGPT can be applied to various stages of the software development life cycle (SDLC) using an eCommerce application case study. Find the on-demand recording and more info at https://applitools.info/b59
Key takeaways:
• Learn how to use ChatGPT to add AI power to your testing and test automation
• Understand the limitations of the technology and where human expertise is crucial
• Gain insight into different AI-based tools
• Adopt AI-based tools to stay relevant and optimize work for developers and testers
* ChatGPT and OpenAI belong to OpenAI, L.L.C.structuraatomului
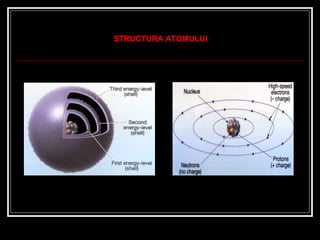
- 1. CAPITOLUL 1. STRUCTURA ÎNVELIŞULUI ELECTRONIC
- 2. Despre ce vom învăţa în acest capitol: Orbital atomic Substrat Mişcare de spin Strat Configuraţie electronică Element reprezentativ Element tranziţional Principiul stabilităţii Principiul lui Pauli Regula lui Hund
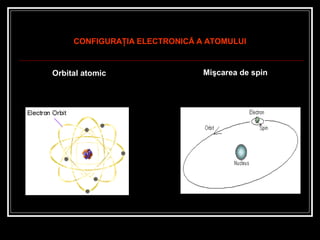
- 4. CONFIGURAŢIA ELECTRONICĂ A ATOMULUI Orbital atomic Mişcarea de spin
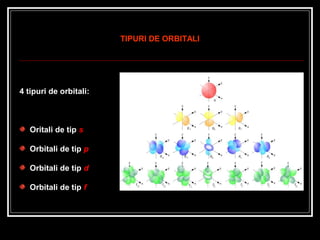
- 5. TIPURI DE ORBITALI 4 tipuri de orbitali: Oritali de tip s Orbitali de tip p Orbitali de tip d Orbitali de tip f
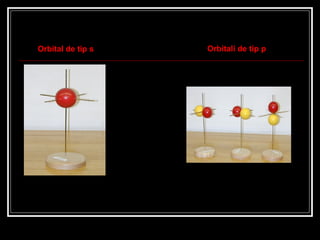
- 6. Orbital de tip s Orbitali de tip p
- 7. Orbitali de tip d Orbitali de tip f
- 8. exerciţiu Notează în tabelul de mai jos numărul de orbitali corespunzători fiecărui substrat: substrat s p d Nr. orbitali creşte energia orbitalilor f
- 10. CONFIGURAŢIA ELECTRONICĂ A ATOMULUI principiul stabilităţii principiul de excluziune al lui Pauli regula lui Hund
- 11. Ordinea ocupării cu electroni a orbitalilor atomici pentru primele 4 straturi: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4 p6 5s2 4d10 5 p6 6s2 4f14 5d10 6 p6 7s2 5f14 6 d10
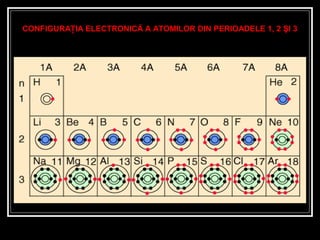
- 12. CONFIGURAŢIA ELECTRONICĂ A ATOMILOR DIN PERIOADELE 1, 2 ŞI 3
- 13. Clasificarea elementelor chimice în blocuri de elemente:
- 14. CONFIGURAŢIA ELECTRONICĂ A ATOMILOR DIN PERIOADA 4 Exerciţiu 1: Notează configuraţia electronică a Sc, Z = 21 1s2 2s2 2p6 3s2 3p6 4s2 3d1 Explică de ce electronul distinctiv se află în orbitalul 3d şi nu în 4p. Explicaţie: substratul 3d are o energie mai joasă decât substratul 4p Elementele de la Sc până la Zn, la care electronul distinctiv se plasează în substratul 3d elemente tranziţionale de tip d
- 15. Exerciţiul 2: Notează configuraţia electronică a Cr, Z = 24 1s2 2s2 2p6 3s2 3p6 4s1 3d5 Observaţie: substratul d semiocupat sau total ocupat cu electroni este mai stabil Exerciţiul 3: Notează configuraţia electronică a Cu, Z = 29 1s2 2s2 2p6 3s2 3p6 4s1 3d10
- 16. RELAŢIA DINTRE STRUCTURA ATOMICĂ A ELEMENTELOR ŞI POZIŢIA LOR ÎN SISTEMUL PERIODIC Structura învelişului electronic al atomului → poziţia elementului în sistemul periodic Numărul grupei Numărul perioadei Blocul de elemente Substrat
- 17. Prof. LUIZA BĂRBUCEANU LICEUL ,, GEORGE CĂLINESCU BUCUREŞTI
