Tugas organik ii
- 1. TUGAS KIMIA ORGANIK II TAUTOMERI AFANDI MUH. MUSA F1C112084
- 2. Tautomeri adalah senyawa-senyawa organik yang dapat melakukan reaksi perubahan yang disebut tautomerisasi, reaksi ini dihasilkan oleh perpindahan atom hidrogen atau proton yang diikuti dengan pergantian ikatan tunggal dengan ikatan ganda di sebelahnya. 1. Pengertian
- 3. Tautomerisasi Suatu senyawa karbonil dengan suatu hidrogen alfa yang bersifat asam, dapat berada dalam dua bentuk yang disebut tautomer. Suatu tautomer keto dan sebuah tautomer enol, tautomerisasi adalah isomer-isomer yang berbeda satu dengan lainnya hanya pada posisi ikatan rangkap dan sebuah atom hidrogen yang berhubungan.
- 4. Karena atom hidrogen berada dalam posisi yang berlainan, kedua bentuk tautomerik ini bukanlah struktur resonansi, melainkan dua struktur berlainan yang berada dalam kesetimbangan (harus diingat bahwa struktur-struktur resonansi berbeda hanya dalam hal posisi elektron).
- 5. 2.Macam-macam Tautomer Tautomerisme prototropik Merujuk pada relokasi sebuah proton.Tautomer prototropik adalah sekelompok keadaan protonasi isomerik dengan rumus empiris dan muatan total yang sama. Tautomerisme annular Sejenis tautomerisme prototropik dimanasebuah proton dapat menduduki dua atau lebih posisi dalam sebuah sistem heterosiklik . Sebagai contoh, 1H- dan 3H- imidazola; 1H-, 2H-, dan 4H-1,2,4- triazola ;1H- dan 2-Hisoindola. Tautomerisme rantai-cincin Terjadi ketika perpindahan proton diikuti oleh perubahan struktur terbuka menjadi cincin, seperti pada bentuk aldehida dan piran glukosa.
- 6. 3. Faktor-Faktor Yang Mempengaruhi Tautomeri Temperatur Pelarut pH
- 7. 4. Bentuk Tautomer Mekanisme umum:
- 8. Reaksi Oksidasi: Tautomeri dapat mempengaruhi kereaktivan suatu senyawa. Suatu pengecualian terhadap sifat keton yang tidak mudah teroksidasi, ialah oksidasi keton yang memiliki sekurang- kurangnya satu hidrogen . Suatu keton yang dapat mengalami tautomeri dapat dioksidasi oleh zat pengoksidasi kuat pada ikatan rangkap karbon-karbon (dari) tautomer enolnya.
- 9. Pendorong elektron – CH2CH3 > – CH3 sehingga pada 1 < 2 akibatnya ikatan C-H pada 1 cenderung lebih sulit diputuskan *) oksidasi keton → asam karboksilat
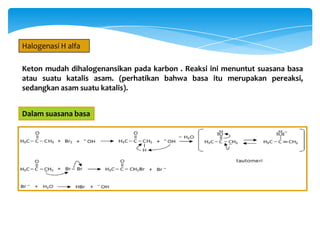
- 10. Keton mudah dihalogenansikan pada karbon . Reaksi ini menuntut suasana basa atau suatu katalis asam. (perhatikan bahwa basa itu merupakan pereaksi, sedangkan asam suatu katalis). Dalam suasana basa Halogenasi H alfa