ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќФќµѕГќЉѕМѕВ
- 1. ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќФќµѕГќЉѕМѕВ ќ†ѕБќ±ќ≥ќЉќ±ѕДќњѕАќњќєќµќѓѕДќ±ќє ќЉќµѕДќ±ќЊѕН ќіѕНќњ ќ±ќЉќµѕДќђќїќїѕЙќљ ќіќЈќї. ќіѕЕќњ ѕГѕДќњќєѕЗќµќѓѕЙќљ ѕАќњѕЕ ќ≠ѕЗќњѕЕќљ ѕДќђѕГќЈ ќљќ± ѕАѕБќњѕГќїќђќ≤ќњѕЕќљ ќЈќїќµќЇѕДѕБѕМќљќєќ±. ќ•ѕАќђѕБѕЗќњѕЕќљ ќіѕНќњ ѕАќµѕБќєѕАѕДѕОѕГќµќєѕВ:ќ•ѕАќђѕБѕЗќњѕЕќљ ќіѕНќњ ѕАќµѕБќєѕАѕДѕОѕГќµќєѕВ: ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќіќµѕГќЉѕМѕВ ќЉќµѕДќ±ќЊѕН ќіѕНќњ ќЃ ѕАќµѕБќєѕГѕГѕМѕДќµѕБѕЙќљ ќ±ѕДѕМќЉѕЙќљ ѕДќњѕЕ ќѓќіќєќњѕЕ ѕГѕДќњќєѕЗќµќѓќњѕЕ (ќЉќЈ ѕАќњќїѕЙќЉќ≠ќљќњѕВ ќњќЉќњќєќњѕАќњќїќєќЇѕМѕВ) ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќіќµѕГќЉѕМѕВ ќЉќµѕДќ±ќЊѕН ќіѕНќњ ќЃ ѕАќµѕБќєѕГѕГѕМѕДќµѕБѕЙќљ ќ±ѕДѕМќЉѕЙќљ ѕДќњѕЕ ќѓќіќєќњѕЕ ѕГѕДќњќєѕЗќµќѓќњѕЕ (ќЉќЈ ѕАќњќїѕЙќЉќ≠ќљќњѕВ ќњќЉќњќєќњѕАќњќїќєќЇѕМѕВ) ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќіќµѕГќЉѕМѕВ ќЉќµѕДќ±ќЊѕН ќіѕНќњ ќЃ ѕАќµѕБќєѕГѕГѕМѕДќµѕБѕЙќљ ќ±ѕДѕМќЉѕЙќљ ќіќєќ±ѕЖќњѕБќµѕДќєќЇѕОќљ ѕГѕДќњќєѕЗќµќѓѕЙќљ (ѕАќњќїѕЙќЉќ≠ќљќњѕВ ќњќЉќњќєќњѕАќњќїќєќЇѕМѕВ) ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќіќµѕГќЉѕМѕВ ќЉќµѕДќ±ќЊѕН ќіѕНќњ ќЃ ѕАќµѕБќєѕГѕГѕМѕДќµѕБѕЙќљ ќ±ѕДѕМќЉѕЙќљ ќіќєќ±ѕЖќњѕБќµѕДќєќЇѕОќљ ѕГѕДќњќєѕЗќµќѓѕЙќљ (ѕАќњќїѕЙќЉќ≠ќљќњѕВ ќњќЉќњќєќњѕАќњќїќєќЇѕМѕВ) ѕА.ѕЗ ѕЕќіѕБќњќ≥ѕМќљќњ (H) ќЉќµ ѕЕќіѕБќњќ≥ѕМќљќњ (H)вЖТ H2 ѕЗќїѕОѕБќєќњ (Cl) ќЉќµ ѕЗќїѕОѕБќєќњ (Cl)вЖТ Cl2 ќњќЊѕЕќ≥ѕМќљќњ (O)ќЉќµ ќњќЊѕЕќ≥ѕМќљќњ (O) вЖТ O2 ќЃ ќЯ3 ќђќґѕЙѕДќњ (ќЭ) ќЉќµ ќђќґѕЙѕДќњ (N) вЖТ N ѕА.ѕЗ ѕЕќіѕБќњќ≥ѕМќљќњ (H) ќЉќµ ѕЕќіѕБќњќ≥ѕМќљќњ (H)вЖТ H2 ѕЗќїѕОѕБќєќњ (Cl) ќЉќµ ѕЗќїѕОѕБќєќњ (Cl)вЖТ Cl2 ќњќЊѕЕќ≥ѕМќљќњ (O)ќЉќµ ќњќЊѕЕќ≥ѕМќљќњ (O) вЖТ O2 ќЃ ќЯ3 ќђќґѕЙѕДќњ (ќЭ) ќЉќµ ќђќґѕЙѕДќњ (N) вЖТ N2 ѕА.ѕЗ ѕЕќіѕБќњќ≥ѕМќљќњ (H) ќЉќµ ѕЗќїѕОѕБќєќњ (Cl)вЖТ HCl ѕЕќіѕБќњќ≥ѕМќљќњ (H) ќЉќµ ќњќЊѕЕќ≥ѕМќљќњ (ќЯ)вЖТ H2O ѕЕќіѕБќњќ≥ѕМќљќњ (H) ќЉќµ ќђќґѕЙѕДќњ (N) вЖТ NH3 ѕЖѕЙѕГѕЖѕМѕБќњѕВ (P)ќЉќµ ѕЗќїѕОѕБќєќњ (Cl) вЖТ PCl3 ѕА.ѕЗ ѕЕќіѕБќњќ≥ѕМќљќњ (H) ќЉќµ ѕЗќїѕОѕБќєќњ (Cl)вЖТ HCl ѕЕќіѕБќњќ≥ѕМќљќњ (H) ќЉќµ ќњќЊѕЕќ≥ѕМќљќњ (ќЯ)вЖТ H2O ѕЕќіѕБќњќ≥ѕМќљќњ (H) ќЉќµ ќђќґѕЙѕДќњ (N) вЖТ NH3 ѕЖѕЙѕГѕЖѕМѕБќњѕВ (P)ќЉќµ ѕЗќїѕОѕБќєќњ (Cl) вЖТ PCl3
- 2. ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќФќµѕГќЉѕМѕВ ќЯ ќњќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќіќµѕГќЉѕМѕВ ѕГѕЕќЉќ≤ќ±ќѓќљќµќє ќЉќµ ќ±ќЉќњќєќ≤ќ±ќѓќ± ѕГѕЕќљќµќєѕГѕЖќњѕБќђ ѕДѕЙќљ ќЉќњќљќЃѕБѕЙќљ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљ ѕДѕЙќљ ѕГѕДќњќєѕЗќµќѓѕЙќљ. ќ†.ѕЗ. вА¶ѕАѕЙѕВ ќµќљѕОќљќµѕДќ±ќє ќ≠ќљќ± ѕЗќїѕОѕБќєќњ (Cl) ќЉќµ ќ≠ќљќ± ќђќїќїќњ ѕЗќїѕОѕБќєќњ (Cl) ќИѕГѕДѕЙ ќ≠ќљќ± ќђѕДќњќЉќњ 17Cl ѕАќњѕЕ ќ≠ѕЗќµќє ќЈќїќµќЇѕДѕБќњќљќєќ±ќЇќЃ ќіѕМќЉќЈѕГќЈ ќЪ(2) L (8) ќЬ (7) ќЇќ±ќє ѕГѕНќЉќ≤ќњќїѕМ Lewis: ќ§ќњ ќѓќіќєќњ ѕМќЉѕЙѕВ ќЄќ± ќЃќЄќµќїќµ ќЇќ±ќє ѕДќњ ќђќїќїќњ ќђѕДќњќЉќњ Cl ќСѕЕѕДѕМ ѕАќњѕЕ ќЄќ± ќЃќЄќµќїќµ ќµќѓќљќ±ќє ќљќ± ќ≠ѕЗќµќє ќ±ќЇѕМќЉќЈ ќ≠ќљќ± ќЈќїќµќЇѕДѕБѕМќљќєќњ. ќЫѕНѕГќЈ: ќЧ ќ±ќЉќњќєќ≤ќ±ќѓќ± ѕГѕЕќљќµќєѕГѕЖќњѕБќђ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљ ќіќЈќї. ѕДќ± ќЈќїќµќЇѕДѕБѕМќљќєќ± ѕАќњѕЕ ќµќѓќљќ±ќє ќЉѕМќљќ± ѕДќњѕЕѕВ ќµќљѕОќљќњќљѕДќ±ќє ќЇќђќљќњќљѕДќ±ѕВ ќ≠ќљќ± ќљќ≠ќњ ќґќµѕЕќ≥ќђѕБќє ѕАќњѕЕ ќ±ќљќЃќЇќµќє ќЇќ±ќє ѕГѕДќ± ќіѕНќњ ќђѕДќњќЉќ±
- 3. ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќФќµѕГќЉѕМѕВ ќФќЈќїќ±ќіќЃ: ќ§ќ± ќіѕНќњ ќђѕДќњќЉќ± ѕДќњѕЕ ѕЗќїѕЙѕБќѓќњѕЕ ќЉќњќєѕБќђќґќњќљѕДќ±ќє ѕДќњ ќЇќњќєќљѕМ ќґќµѕНќ≥ќњѕВ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљ. ќЯ ќњќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќіќµѕГќЉѕМѕВ ѕГѕЕќЉќ≤ќњќїќѓќґќµѕДќ±ќє ќЇќ±ќє ќЉќµ ќЉќєќ± ќ≥ѕБќ±ќЉќЉќЃ ѕАќњѕЕ ќµќѓќљќ±ќє ѕГќ±ќљ ќљќ± ќµќљѕОќљќµќє ѕДќ± ќіѕНќњ ќЇќњќєќљќђ ќЈќїќµќЇѕДѕБѕМќљќєќ± вА¶ќЇќ±ќє ќ≥ѕБќђѕЖќµѕДќ±ќєвА¶ Cl2 вЖТ
- 4. ќУќєќ± ѕАѕБќњѕГѕАќ±ќЄќЃѕГѕДќµ ѕДќЈќљ ќ≠ќљѕЙѕГќЈ 1H ќЇќ±ќє 1ќЧ ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќФќµѕГќЉѕМѕВ H2 вА¶ќЇќ±ќє ќ≥ѕБќђѕЖќњѕЕќЉќµ:
- 5. ќУќєќ± ѕАѕБќњѕГѕАќ±ќЄќЃѕГѕДќµ ѕДќЈќљ ќ≠ќљѕЙѕГќЈ 1H ќЇќ±ќє 17Cl ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќФќµѕГќЉѕМѕВ HClвА¶ќЇќ±ќє ќ≥ѕБќђѕЖќњѕЕќЉќµ:
- 6. ќУќєќ± ѕАѕБќњѕГѕАќ±ќЄќЃѕГѕДќµ ѕДќЈќљ ќ≠ќљѕЙѕГќЈ 1H ќЇќ±ќє 7N ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќФќµѕГќЉѕМѕВ NH3 вА¶ќЇќ±ќє ќ≥ѕБќђѕЖќњѕЕќЉќµ:
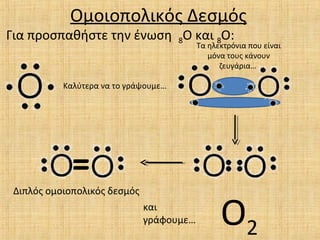
- 7. ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќФќµѕГќЉѕМѕВ ќУќєќ± ѕАѕБќњѕГѕАќ±ќЄќЃѕГѕДќµ ѕДќЈќљ ќ≠ќљѕЙѕГќЈ 8O ќЇќ±ќє 8O: ќЪќ±ќїѕНѕДќµѕБќ± ќљќ± ѕДќњ ќ≥ѕБќђѕИќњѕЕќЉќµвА¶ ќФќєѕАќїѕМѕВ ќњќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќіќµѕГќЉѕМѕВ ќЇќ±ќє ќ≥ѕБќђѕЖќњѕЕќЉќµвА¶ ќЯ2 ќ§ќ± ќЈќїќµќЇѕДѕБѕМќљќєќ± ѕАќњѕЕ ќµќѓќљќ±ќє ќЉѕМќљќ± ѕДќњѕЕѕВ ќЇќђќљќњѕЕќљ ќґќµѕЕќ≥ќђѕБќєќ±вА¶
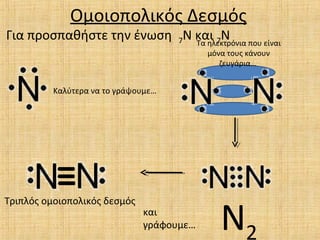
- 8. ќЯќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќФќµѕГќЉѕМѕВ ќУќєќ± ѕАѕБќњѕГѕАќ±ќЄќЃѕГѕДќµ ѕДќЈќљ ќ≠ќљѕЙѕГќЈ 7ќЭ ќЇќ±ќє 7ќЭ ќЪќ±ќїѕНѕДќµѕБќ± ќљќ± ѕДќњ ќ≥ѕБќђѕИќњѕЕќЉќµвА¶ ќ§ѕБќєѕАќїѕМѕВ ќњќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќіќµѕГќЉѕМѕВ ќЇќ±ќє ќ≥ѕБќђѕЖќњѕЕќЉќµвА¶ ќЭ2 ќ§ќ± ќЈќїќµќЇѕДѕБѕМќљќєќ± ѕАќњѕЕ ќµќѓќљќ±ќє ќЉѕМќљќ± ѕДќњѕЕѕВ ќЇќђќљќњѕЕќљ ќґќµѕЕќ≥ќђѕБќєќ±вА¶
- 9. ѕДќњ ќЇќњќєќљѕМ ќЃ ќЇќњќєќљќђ ќґќµѕНќ≥ќЈ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљ ќ≠ќїќЇќњќљѕДќ±ќє ќ±ѕАѕМ ќѓќіќєќњѕЕѕВ ѕАѕЕѕБќЃќљќµѕВ ќ£ѕЕќљќњѕИќѓќґќњќљѕДќ±ѕВ: ќМѕДќ±ќљ ѕГѕЗќЈќЉќ±ѕДќѓќґќњќљѕДќ±ќє ќњќЉќњќєќњѕАќњќїќєќЇќњќѓ ќіќµѕГќЉќњќѓ, ѕДќ± ќђѕДќњќЉќ± ќЉќњќєѕБќђќґќњќљѕДќ±ќє ќЇќњќєќљќђ ќґќµѕНќ≥ќЈ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљвА¶ ќМѕДќ±ќљ ѕГѕЗќЈќЉќ±ѕДќѓќґќњќљѕДќ±ќє ќњќЉќњќєќњѕАќњќїќєќЇќњќѓ ќіќµѕГќЉќњќѓ, ѕДќ± ќђѕДќњќЉќ± ќЉќњќєѕБќђќґќњќљѕДќ±ќє ќЇќњќєќљќђ ќґќµѕНќ≥ќЈ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљвА¶ ќ±ќїќїќђ ѕЕѕАќђѕБѕЗќµќє ќЉќєќ± ќіќєќ±ѕЖќњѕБќђвА¶ ќ±ќїќїќђ ѕЕѕАќђѕБѕЗќµќє ќЉќєќ± ќіќєќ±ѕЖќњѕБќђвА¶ ѕДќњ ќЇќњќєќљѕМ ќЃ ќЇќњќєќљќђ ќґќµѕНќ≥ќЈ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљ ќ≠ќїќЇќњќљѕДќ±ќє ќ±ѕАѕМ ќіќєќ±ѕЖќњѕБќµѕДќєќЇќњѕНѕВ ѕАѕЕѕБќЃќљќµѕВ
- 10. ќФќЈќїќ±ќіќЃ: ќ§ќњ ќЇќњќєќљѕМ ќґќµѕНќ≥ќњѕВ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљ ќ≠ќїќЇќµѕДќ±ќє ќ±ѕАѕМ ќ≠ќљќ±ќљ ѕАѕЕѕБќЃќљќ± ѕЗќїѕЙѕБќѓќњѕЕ ѕАќњѕЕ ќ≠ѕЗќµќє 17 ѕАѕБѕЙѕДѕМќљќєќ± ќЇќ±ќє ќ≠ќљќ±ќљ ѕАѕЕѕБќЃќљќ± ќЧ ѕАќњѕЕ ќ≠ѕЗќµќє 1 ѕАѕБѕЙѕДѕМќљќєќњ. ќ§ќњ ќЇќњќєќљѕМ ќґќµѕНќ≥ќњѕВ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљ ќ≠ќїќЇќµѕДќ±ќє ќ±ѕАѕМ ќіѕНќњ ѕАѕЕѕБќЃќљќµѕВ ѕЗќїѕЙѕБќѓќњѕЕ ѕАќњѕЕ ќњ ќЇќ±ќЄќ≠ќљќ±ѕВ ќ≠ѕЗќµќє 17 ѕАѕБѕЙѕДѕМќљќєќ± ќСѕЕѕДѕМ ќ≠ѕЗќµќє ѕЙѕВ ѕГѕЕќљќ≠ѕАќµќєќ± ѕДќњ ќЇќњќєќљѕМ ќґќµѕНќ≥ќњѕВ ќљќ± ќ≤ѕБќѓѕГќЇќµѕДќ±ќє ѕГќµ ќЉќµќ≥ќ±ќїѕНѕДќµѕБќњ ѕАќњѕГќњѕГѕДѕМ ѕГѕДќЈ ќЉќµѕБќєќђ ѕДќњѕЕ ѕЗќїѕЙѕБќѓќњѕЕ (ќ±ѕЖќњѕН ѕДќњ ќ≠ќїќЇќµќє ѕАќµѕБќєѕГѕГѕМѕДќµѕБќњ). ќИѕДѕГќє ѕДќњ ѕЗќїѕОѕБќєќњ ќ≠ѕЗќµќє ќ≠ќљќ± ¬Ђќµќїќ±ѕЖѕБѕМѕВ¬ї ќ±ѕБќљќЈѕДќєќЇѕМ ѕЖќњѕБѕДќѓќњ (ѕАќњѕЕ ѕДќњ ѕГѕЕќЉќ≤ќњќїќѓќґќњѕЕќЉќµ ќЉќµ ќі- ), ќµќљѕО ѕДќњ ѕЕќіѕБќњќ≥ѕМќљќњ ќ≠ѕЗќµќє ќ≠ќљќ± ¬Ђќµќїќ±ѕЖѕБѕМѕВ¬ї ќЄќµѕДќєќЇѕМ ѕЖќњѕБѕДќѓќњ (ѕАќњѕЕ ѕДќњ ѕГѕЕќЉќ≤ќњќїќѓќґќњѕЕќЉќµ ќЉќµ ќі+ ) ќУќєќ± ѕДќњќљ ѕАќ±ѕБќ±ѕАќђќљѕЙ ќїѕМќ≥ќњ ќ≠ѕЗќњѕЕќЉќµ ќЉќѓќ± ѕАѕМќїѕЙѕГќЈ ѕДќњѕЕ ќњќЉќњќєќњѕАќњќїќєќЇќњѕН ќіќµѕГќЉќњѕН ќЇќ±ќє ќ≥ќєвАЩ ќ±ѕЕѕДѕМ ѕДќњќљ ќіќµѕГќЉѕМ ѕДќњќљ ѕЗќ±ѕБќ±ќЇѕДќЈѕБќѓќґќњѕЕќЉќµ ѕЙѕВ ѕАќњќїѕЙќЉќ≠ќљќњ ќњќЉќњќєќњѕАќњќїќєќЇѕМ ќіќµѕГќЉѕМ. ќі+ ќі-
- 11. ќ†ќњќїѕЙќЉќ≠ќљќњѕВ ќњќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќіќµѕГќЉѕМѕВ ќ±ѕЖќњѕН ѕДќ± ќЇќњќєќљќђ ќґќµѕНќ≥ќЈ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљ ќ≠ќїќЇќњќљѕДќ±ќє ќ±ѕАѕМ ќіќєќ±ѕЖќњѕБќµѕДќєќЇќђ ќђѕДќњќЉќ± ќЬќЈ ѕАќњќїѕЙќЉќ≠ќљќњѕВ ќњќЉќњќєќњѕАќњќїќєќЇѕМѕВ ќіќµѕГќЉѕМѕВ ќ±ѕЖќњѕН ѕДќ± ќЇќњќєќљќђ ќґќµѕНќ≥ќЈ ќЈќїќµќЇѕДѕБќњќљќѓѕЙќљ ќ≠ќїќЇќњќљѕДќ±ќє ќ±ѕАѕМ ќіќєќ±ѕЖќњѕБќµѕДќєќЇќђ ќђѕДќњќЉќ±
































![[ќ¶ѕЕѕГќєќЇќЃ ќУ¬і ќУѕЕќЉќљќ±ѕГќѓќњѕЕ] ќ¶ѕЕќїќїќђќіќєќњ ќ≥ќєќ± ѕДќњ ќЧќїќµќЇѕДѕБќєќЇѕМ ќ°ќµѕНќЉќ±](https://cdn.slidesharecdn.com/ss_thumbnails/02-161214022842-thumbnail.jpg?width=560&fit=bounds)


























































