4 ΣΥΜΠΟΣΙΟ ΚΛΙΝΙΚΗΣ ΟΓΚΟΛΟΓΙΑΣ: Καρκίνος μαστού & εγκυμοσύνη.
- 1. ΑΝΑΣΤΑΣΙΑ ΜΠΟΘΟΥ Μαία, Msc Διπλωματούχος Μαστολογίας Πανεπιστημίου Montpellier 1,Γαλλίας Μέλος της Ελληνο-Γαλλικής Μονάδας Μαστού ¨ΡΕΑ¨ & Δρ. ΣΤΕΦΑΝΟΣ ΖΕΡΒΟΥΔΗΣ Χειρούργος Μαστολόγος Αναπ. Καθηγητής Πανεπιστ. Montpellier-Nimes Πρόεδρος του MANOSMED: Μεσογειακό Πανεπιστήμιο Μαστολογίας ΜΑΙΕΥΤΗΡΙΟ ΡΕΑ, ΑΘΗΝΑ
- 3. ΟΡΙΣΜΟΣ- ΣΥΧΝΟΤΗΤΑ Είναι ο κα��κίνος που διαγιγνώσκεται κατά την κύηση ή κατά τη διάρκεια του πρώτου χρόνου μετά τον τοκετό. Συχνότητα: 0.2 – 3.8 %: 1/ 3000 κυήσεις. >3% των καρκίνων του μαστού διαγιγνώσκονται στη διάρκεια της κύησης μεταξύ 23 και 47 χρονών (μέσος όρος: 33 έτη). Αύξηση της συχνότητας, καθώς όλο και περισσότερες γυναίκες τεκνοποιούν σε μεγάλη ηλικία. Pavlidis N , Pentheroudakis G. Cancer Treat Rev. 2005;31:439-47. Ring AE, et al, Ann Oncol. 2005;16:1855-60 Mignot L., 2002;
- 4. ΕΠΙΔΗΜΙΟΛΟΓΙΑ Πρόωρος τοκετός: μεγαλύτερος κίνδυνος ανάπτυξης Ca μαστού; IUGR και Προεκλαμψία: μικρότερος κίνδυνος; Η αυτόματη αποβολή ή διακοπή κύησης δεν αυξάνει τον κίνδυνο για ανάπτυξη Ca μαστού; Προστατευτική δράση της προγεστερόνης; “The short term & long term effect on breast cancer risk: a prospective study of 802.457 parous Norwegian women”, Albrektsen G. et als, Br.J. Cancer 1995,72.
- 6. ΔΙΑΓΝΩΣΗ Στο παρελθόν: καθυστερημένη διάγνωση – προχωρημένος όγκος, κάκιστη πρόγνωση, απροθυμία επιθετικών χειρισμών κατά την κύηση. Σήμερα: έγκαιρη διάγνωση – απαραίτητη η ψηλάφηση των μαστών κατά τις επισκέψεις. Το πιο συχνό κλινικό εύρημα: ψηλαφητή μάζα ή μονοπορικό έκκριμα θηλής.
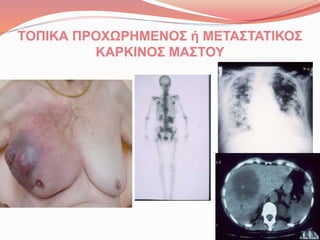
- 7. ΤΟΠΙΚΑ ΠΡΟΧΩΡΗΜΕΝΟΣ ή ΜΕΤΑΣΤΑΤΙΚΟΣ ΚΑΡΚΙΝΟΣ ΜΑΣΤΟΥ
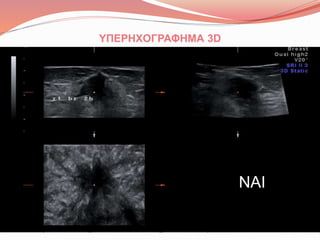
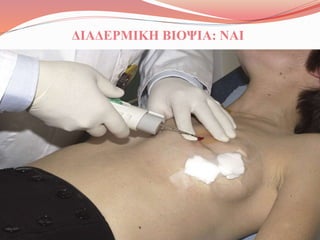
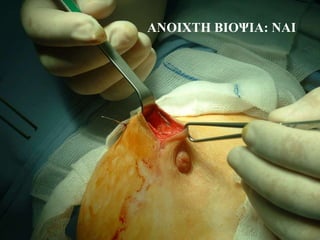
- 8. ΔΙΑΓΝΩΣΤΙΚΕΣ ΜΕΘΟΔΟΙ • Μαστογραφία • Υπερηχογραφία • MRI Δύσκολη: πρόβλημα σκιαγραφικού Gadolinium • FNA Απαιτείται έμπειρος κυτταρολόγος • Core biopsy • Ανοιχτή βιοψία. Αναφερόμενη ευαισθησία 63-78%. Ψευδώς θετικά: 25%. Συχνά δύσκολη-ακτινοσκιερός μαστός • Δεν υπάρχει κίνδυνος για το έμβρυο< 50 mrads. Ασφαλής μέθοδος Η καλύτερη προσέγγιση Απαραίτητη, συμπληρωματική της κλινικής εξέτασης, καλή ειδικότητα
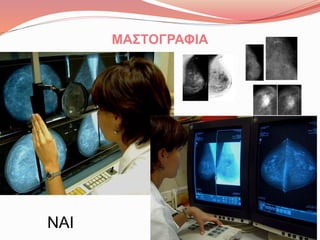
- 10. ΜΑΣΤΟΓΡΑΦΙΑ ΝΑΙ
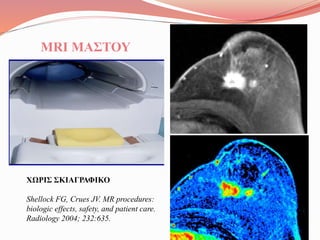
- 11. ΧΩΡΙΣ ΣΚΙΑΓΡΑΦΙΚΟ Shellock FG, Crues JV. MR procedures: biologic effects, safety, and patient care. Radiology 2004; 232:635. MRI ΜΑΣΤΟΥ
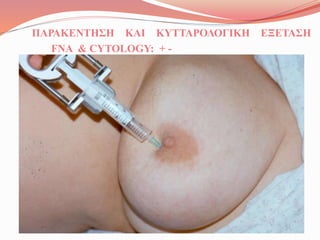
- 12. ΠΑΡΑΚΕΝΤΗΣΗ ΚΑΙ ΚΥΤΤΑΡΟΛΟΓΙΚΗ ΕΞΕΤΑΣΗ FNA & CYTOLOGY: + -
- 15. ΠΑΘΟΛΟΓΟΑΝΑΤΟΜΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ Διηθητικό πορογενές καρκίνωμα:75-90%: χαμηλής διαφοροποίησης (Grade 3), μεγάλης διαμέτρου με αρνητικούς υποδοχείς.` Φλεγμονώδης κα��κίνος: 4-5 %. Μεγαλύτερη προσβολή μασχαλιαίων λεμφαδένων & λεμφαγγειακή διήθηση. Έκφραση του HER2 σε ποσοστό 16-58%. Middleton LP et al, Cancer. 2003;98:1055-60. Bonnier P et al, Int J Cancer. 1997;72:720-7. Ring AE et al, J Clin Oncol. 2005;23:4192-7. Elledge RM et al, Cancer. 1993;71:2499-506.
- 16. ΣΤΑΔΙΟΠΟΙΗΣΗ • Ηπατικός έλεγχος: Αιματολογικές εξετάσεις-Υπερηχογραφία: ΝΑΙ • Ακτινογραφία θώρακος, CT θώρακος: ΝΑΙ, με προστασία της κοιλίας • Αξονική Τομογραφία (CT) Άνω-Κάτω Κοιλίας: Να αποφεύγεται. • Μαγνητική Τομογραφία (MRI): +- NAI • Σπινθηρογράφημα: ΟΧΙ Bone scanning in pregnant patients with breast carcinoma. Baker J, Ali A, Groch MW, Fordham E, Economou SG Clin Nucl Med. 1987;12:519.
- 17. ΘΕΡΑΠΕΙΑ • Ίδια κριτήρια, όπως και εκτός κύησης: το συντομότερο το καλύτερο. The daily increased risk for developing axillary metastasis for an untreated breast carcinoma in pregnant women is 0.057% (1,8% per month !!) Nettleton J et al, Obstet Gynecol. 1996;87:414-8. • Χειρουργική αντιμετώπιση: NAI. • Χημειοθεραπεία: NAI…ΑΛΛΑ. • Ακτινοθεραπεία & Ορμονοθεραπεία: ΟΧΙ, μόνο μετά τη γέννηση. Η θεραπεία εξαρτάται από το στάδιο της νόσου και την εβδομάδα της κύησης.
- 18. ΧΕΙΡΟΥΡΓΙΚΗ ΠΡΟΣΕΓΓΙΣΗ Η ριζική τροποποιημένη μαστεκτομή και η χειρουργική επέμβαση διατήρησης του μαστού με αφαίρεση των μασχαλιαίων λεμφαδένων θεωρούνται οι μέθοδοι επιλογής στη θεραπεία της τοπικής νόσου. Τα ποσοστά επιβίωσης των δύο προσεγγίσεων είναι παρόμοια. Loibl et al, Cancer 2006; Kuerer et al, Surgery 2002 Annane K, Bellocq JP, Brettes JP, Mathelin C. Infiltrative breast cancer during pregnancy and conservative surgery. Fetal Diagn Ther 2005; 20:442
- 19. ΧΗΜΕΙΟΘΕΡΑΠΕΙΑ • Προεγχειρητική ΧΜΘ σε προχωρημένα στάδια. • Όχι στο 1ο τρίμηνο, ναι στο 2ο και 3ο τρίμηνο. • Σύνηθες σχήμα: FEC, FAC. Όχι μεθοτρεξάτη. • Η τελευταία ΧΜΘ θα γίνει 6 εβδομάδες πριν τη ΚΤ. • Χημειοθεραπεία: Αποβάλλεται από το γάλα. • TAXOL, TAXOTERE – λίγες μελέτες • Τα αντιεμετικά επιτρέπονται. !
- 20. ΧΗΜΕΙΟΘΕΡΑΠΕΙΑ •1ο ΤΡΙΜΗΝΟ: Δεν συνιστάται λόγω κινδύνου αποβολής ( > 17%) , τερατογένεσης και συγγενών ανωμαλιών. •2ο & 3ο ΤΡΙΜΗΝΟ: Μικρός κίνδυνος (< 1.5%) Espie M, Cuvier C. Drug Saf. 1998;18:135-42. Doll DC et al, Semin Oncol. 1989;16Germann N, Goffinet F, Goldwasser F. Anthracyclines during pregnancy: embryo-fetal outcome in 160 patients. Ann Oncol 2004; 15:146. :337-46.
- 21. ΑΚΤΙΝΟΘΕΡΑΠΕΙΑ •Η Ακτινοθεραπεία μπορεί να περιλαμβάνει το στήθος, το θωρακικό τοίχωμα και τους λεμφαδένες. •Η έκθεση του εμβρύου σε ιονίζουσα ακτινοβολία στη μήτρα δεν θεωρείται ασφαλής θεραπευτική επιλογή και θα πρέπει να πραγματοποιείται μετά την χημειοθεραπεία και τουλάχιστον 6 μήνες μετά την πρωταρχική θεραπεία •Υπάρχουν τέσσερις κατηγορίες των συνεπειών της ακτινοβολίας στο έμβρυο: απώλεια κύησης (αποβολή ή θνησιγένεια), δυσπλασία, διαταραχές της ανάπτυξης και μεταλλαξιογόνες και καρκινογόνες επιδράσεις. •Μερικές μελέτες είναι καθησυχαστικές σε ό,τι αφορά την έκθεση του εμβρύου: 0,04 - 0,2 gray (50 gray για τη μητέρα) δεν είναι επιβλαβής, χρησιμοποιώντας την ασπίδα μολύβδου. [Fenig et al, Cancer Treat Rev 2001] Gemignani ML, Petrek JA, Borgen PI. Breast cancer and pregnancy. Surg Clin North Am 1999; 79:1157.
- 22. ΟΡΜΟΝΟΘΕΡΑΠΕΙΑ Έχει αναφερθεί ότι η ταμοξιφαίνη έχει τερατογόνο δράση και μπορεί να οδηγήσει σε σοβαρές ανωμαλίες στο έμβρυο. Woo, Arch Surg 2003 Αρκετές μελέτες αναφέρουν έως και 20% ανωμαλίες του εμβρύου: κρανιοπροσωπικές δυσπλασίες και διφορούμενα γεννητικά όργανα. Ως εκ τούτου, συνιστάται η ορμονική θεραπεία να καθυστερήσει μέχρι τη γέννηση.
- 23. ΟΡΜΟΝΟΘΕΡΑΠΕΙΑ Αναστολείς αρωματάσης: Anastrozole, Letrozole, Exemestane – δεν έχουν ένδειξη. Διφωσφωνικά – δεν έχουν ένδειξη στη διάρκεια της κύησης (μόνο σε μεταστατική νόσο).
- 24. ΣΤΟΧΕΥΜΕΝΕΣ ΘΕΡΑΠΕΙΕΣ Trastuzumab (Herceptin®) • Στην κύηση πιο συχνά HER2 +++ • Το φάρμακο διαπερνά τον πλακουντιακό φραγμό • Εμβρυικοί ιστοί εκφράζουν HER2 • Κίνδυνος Ολιγοαμνίου Mir, Ann Oncol 2007 Αντενδείκνυνται στην εγκυμοσύνη Άλλες στοχευμένες θεραπείες: Lapatimib -no datas Αντενδεικνύονται
- 25. ΣΤΑΔΙΟ Ι & ΙΙ 1ο τρίμηνο: α) τροποποιημένη ριζική μαστεκτομή αν Ν (-) τότε συνέχιση κύησης. αν Ν (+) τότε ΧΜΘ. β) ογκεκτομή & λεμφαδενεκτομή. γ) για τη μασχάλη} βιοψία φρουρού λεμφαδένα – τώρα προτείνεται περισσότερο αντί λεμφαδενεκτομή Gentillini: Eur.J.Nucl.Mol. Imag. 2010 2ο & 3ο τρίμηνο: α) μαστεκτομή. β) ογκεκτομή & λεμφαδενεκτομή +- χημειοθεραπεία + ακτινοθεραπεία μετά τον τοκετό.
- 26. ΣΤΑΔΙΟ ΙII & ΙV 1ο τρίμηνο: Διακοπή κύησης & θεραπεία. 2ο & 3ο τρίμηνο: ``Η διακοπή της κύησης δεν βελτιώνει την πρόγνωση``. Αν το έμβρυο είναι βιώσιμο; Τότε ΚΤ & Θεραπεία. Αν δεν είναι βιώσιμο: διακοπή της κύησης & Θεραπεία. Royal College of Obstetrics and Gynaecology, Guideline No 12, revised 2009
- 27. • Όταν ενδείκνυται ΧΜΘ στο 1ο τρίμηνο. • Σε ταχεία εξελισσόμενη νόσο. • Όταν το επιθυμεί η γυναίκα. ΕΝΔΕΙΞΕΙΣ ΔΙΑΚΟΠΗΣ ΚΥΗΣΗΣ
- 28. ΑΠΟΓΑΛΑΚΤΙΣΜΟΣ Συνιστάται λογού εμβρύου αλλά δεν βελτιώνει την πρόγνωση. Ενδείξεις: • Χημειοθεραπεία 1ου τριμήνου. • Ακτινοθεραπεία.
- 29. ΠΡΟΓΝΩΣΗ • Η Πρόγνωση εξαρτάται από την καθυστέρηση στη διάγνωση & στη θεραπεία. • Τα ίδια αποτελέσματα όσον αφορά την επιβίωση και το διάστημα ελεύθερο νόσου εντός ή εκτός κύησης. • Αλλά, γενικά έχει κακή πρόγνωση λογού σταδίου, επιθετικότητας και νεανικής ηλικίας, ανεξάρτητα με την κύηση. • ΧΜΘ στην κύηση; Παρακολούθηση παιδιών – καλά αποτελέσματα. • Διασπορά στο έμβρυο; - Όχι.
- 30. ΚΥΗΣΗ ΜΕΤΑΑΠΟ ΚΑΡΚΙΝΟ ΜΑΣΤΟΥ Η γονιμότητα μετά τη θεραπεία του καρκίνου του μαστού επηρεάζεται σίγουρα, ιδιαίτερα σε γυναίκες μεγαλύτερης ηλικίας (>30 χρόνια), αφού η χημειοθεραπεία μπορεί να οδηγήσει σε πρόωρη ωοθηκική ανεπάρκεια. Πρέπει πάντα να γίνεται κάτω από παρακολούθηση του καρκίνου του μαστού. Παλαιότερα, η κλασική σύσταση ήταν 5 χρόνια. Η τρέχουσα ιατρική συμβουλή για τις προεμμηνοπαυσιακές γυναίκες με καρκίνο του μαστού είναι να περιμένουν δύο χρόνια μετά τη θεραπεία πριν επιχειρήσουν σύλληψη. Στο Στάδιο IV, συνιστάται στις ασθενείς να αποφύγουν την εγκυμοσύνη. Ωστόσο, η αναμονή >6 μήνες μετά την ολοκλήρωση της θεραπείας δεν βελτιώνει την πρόγνωση των ασθενών με εντοπισμένη νόσο. Ives A et al, BMJ. 2007?334: 194-196
- 31. ΣΥΜΠΕΡΑΣΜΑΤΑ • Χρειάζεται ομάδα πολλαπλών ειδικοτήτων. • Έγκαιρη διάγνωση: Η καθυστέρηση στη διάγνωση χειροτερεύει την πρόγνωση. • Αυξημένη επαγρύπνηση μαιευτήρων που παρακολουθούν τις έγκυες γυναίκες – Ψηλάφηση κατά τις επισκέψεις. Υπέρηχο μαστών. • Κυτταρολογική εξέταση ή καλύτερα Μικροβιοψία • Προτιμητέα 1η θεραπεία: Ριζική Τροποποιημένη Μαστεκτομή ή συντηρητική χειρουργική και βιοψία φρουρού λεμφαδένα
- 32. ΣΥΜΠΕΡΑΣΜΑΤΑ • Συντηρητική θεραπεία: εφικτή, αλλά ακτινοθεραπεία μετά τον τοκετό . • Δεν συνίσταται ακτινοθεραπεία κατά την κύηση. • Χημειοθεραπεία 2ο και 3ο τρίμηνο με ελάχιστες επιπλοκές: CAF, CEF, TEC. • Η διακοπή κύησης δεν βελτιώνει την πρόγνωση και την επιβίωση. • Πρακτικά, δεν υπάρχει διαφορά στην επιβίωση όσον αφορά καρκίνο του μαστού κατά την κύηση με καρκίνο εκτός κύησης.












![ΑΚΤΙΝΟΘΕΡΑΠΕΙΑ
•Η Ακτινοθεραπεία μπορεί να περιλαμβάνει το στήθος, το θωρακικό τοίχωμα
και τους λεμφαδένες.
•Η έκθεση του εμβρύου σε ιονίζουσα ακτινοβολία στη μήτρα δεν θεωρείται
ασφαλής θεραπευτική επιλογή και θα πρέπει να πραγματοποιείται μετά την
χημειοθεραπεία και τουλάχιστον 6 μήνες μετά την πρωταρχική θεραπεία
•Υπάρχουν τέσσερις κατηγορίες των συνεπειών της ακτινοβολίας στο έμβρυο:
απώλεια κύησης (αποβολή ή θνησιγένεια), δυσπλασία, διαταραχές της
ανάπτυξης και μεταλλαξιογόνες και καρκινογόνες επιδράσεις.
•Μερικές μελέτες είναι καθησυχαστικές σε ό,τι αφορά την έκθεση του
εμβρύου: 0,04 - 0,2 gray (50 gray για τη μητέρα) δεν είναι επιβλαβής,
χρησιμοποιώντας την ασπίδα μολύβδου.
[Fenig et al, Cancer Treat Rev 2001]
Gemignani ML, Petrek JA, Borgen PI. Breast cancer and pregnancy. Surg Clin North Am
1999; 79:1157.](https://image.slidesharecdn.com/random-160530081509/85/4-21-320.jpg)











