Alkana alkena-alkuna
- 1. ALKANA 1
- 2. Alkana adalah hidrokarbon yang rantai C nya hanya terdiri dari ikatan kovalen tunggal saja. sering disebut sebagai hidrokarbon jenuh, karena jumlah atom Hidrogen dalam tiap-tiap molekulnya maksimal. Memahami tata nama Alkana sangat vital, karena menjadi dasar penamaan senyawa- senyawa karbon lainnya.
- 3. Sifat-sifat umum 1. Hidrokarbon jenuh (tidak ada ikatan atom C rangkap sehingga jumlah atom H nya maksimal) 2. Disebut golongan parafin karena affinitas kecil (sedikit gaya gabung) 3. Sukar bereaksi 4. Bentuk Alkana dengan rantai C1 – C4 pada suhu kamar adalah gas, C4 – C17 pada suhu adalah cair dan > C18 pada suhu kamar adalah padat 5. Titik didih makin tinggi bila unsur C nya bertambah…dan bila jumlah atom C sama maka yang bercabang mempunyai titik didih yang lebih rendah 6. Sifat kelarutan : mudah larut dalam pelarut non polar 7. Massa jenisnya naik seiring dengan penambahan jumlah unsur C 8. Merupakan sumber utama gas alam dan petrolium (minyak bumi)
- 4. Deret homolog alkana Deret homolog adalah suatu golongan/kelompok senyawa karbon dengan rumus umum yang sama, mempunyai sifat yang mirip dan antar suku-suku berturutannya mempunyai beda CH2 atau dengan kata lain merupakan rantai terbuka tanpa cabang atau dengan cabang yang nomor cabangnya sama. Sifat-sifat deret homolog alkana : o Mempunyai sifat kimia yang mirip o Mempunyai rumus umum yang sama o Perbedaan Mr antara 2 suku berturutannya sebesar 14 o Makin panjang rantai karbon, makin tinggi titik didihnya
- 6. Sifat Fisika Alkana Alkana yang memiliki berat molekul rendah yaitu metana, etana, propana dan butana pada suhu kamar dan tekanan atmosfer berwujud gas, alkana yang memiliki 5-17 atom karbon berwujud cair dan selebihnya berwujud padat. Alkana merupakan senyawa nonpolar sehingga sukar larut dalam air tetapi cenderung larut pada pelarut-pelarut yang nonpolar seperti eter. Jika alkana ditambahkan pada air alkana akan berada pada lapisan atas, hal ini disebabkan adanya perbedaan massa jenis antara air dan alkana. Sebagian besar alkana memiliki massa jenis lebih kecil dari massa jenis air. Karena alkana merupakan senyawa nonpolar sehingga alkana yang berwujud cair pada suhu kamar merupakan pelarut yang baik untuk senyawa-senyawa kovalen. Untuk alkana-alkana yang berantai lurus titik leleh dan titik didih makin tinggi seiring bertambahnya massa molekul molekul. Pada molekul-molekul alkana terjadi gaya van der Wals. Oleh karena itu alkana memiliki titik leleh dan titik didih yang lebih rendah dibanding senyawa semipolar atau senyawa polar dengan berat molekul yang hampir sama.
- 7. Sifat Kimia Alkana Alkana merupakan senyawa nonpolar yang tidak bereaksi dengan sebagian besar pereaksi. Hal ini disebabkan alkana memiliki ikatan sigma yang kuat antar atom karbon. Pada kondisi tertentu alkana dapat bereaksi dengan oksigen dan unsur-unsur halogen. Apabila jumlah oksigen tersedia cukup memadai alkana akan teroksidasi sempurna menjadi karbon dioksida dan uap air serta pelepasan sejumlah energi panas. Apabila jumlah oksigen yang tersedia tidak mencukupi, hasil reaksi yang diperoleh berupa karbon monooksida dan uap air. Alkana dapat bereaksi dengan halogen dikatalisis oleh panas atau sinar ultraviolet. Dari reaksi tersebut terjadi pergantian 1 atom H dari alkana terkait. Namun apabila halogen yang tersedia cukup memadai atau berlebih, maka terjadi pergantian lebih dari satu atom bahkan semua atom H digantikan oleh halogen. Berdasarkan penelitian laju pergantian atom H sebagai berikut H3 > H2 > H1. Reaksi pergantian atom dalam suatu senyawa disebut reaksi substitusi.
- 8. Kegunaan alkana, sebagai : • Bahan bakar • Pelarut • Sumber hidrogen • Pelumas • Bahan baku untuk senyawa organik lain • Bahan baku industri
- 9. ALKENA 9
- 10. merupakan senyawa hidrokarbon tak jenuh yang memiliki 1 ikatan rangkap 2 (-C=C-)
- 11. 1. Hidrokarbon tak jenuh ikatan rangkap dua 2. Alkena disebut juga olefin (pembentuk minyak) 3. Sifat fisiologis lebih aktif (sbg obat tidur –> 2-metil-2- butena) 4. Sifat sama dengan Alkana, tapi lebih reaktif 5. Sifat-sifat : gas tak berwarna, dapat dibakar, bau yang khas, eksplosif dalam udara (pada konsentrasi 3 – 34 %) 6. Terdapat dalam gas batu bara biasa pada proses “cracking” Sifat-sifat umum Alkena
- 12. Sifat-sifat fisika Alkena Alkena merupakan senyawa nonpolar sehingga tidak larut dalam air dan memiliki massa jenis lebih kecil dari air. Alkena dapat larut dalam alkena lain, pelarut-pelarut nonpolar dan etanol. Pada temperatur kamar alkena yang memiliki dua, tiga dan empat atom karbon berwujud gas. Sedangkan Alkena dengan dengan berat molekul lebih tinggi dapat berupa cair dan padatan pada suhu kamar.
- 13. Sifat-sifat kimia Alkena Ikatan rangkap yang dimiliki alkena merupakan ciri khas dari alkena yang disebut gugus fungsi. Reaksi terjadi pada alkena dapat terjadi pada ikatan rangkap dapat pula terjadi diluar ikatan rangkap. Reaksi yang terjadi pada ikatan rangkap disebut reaksi adisi yang ditandai dengan putusnya ikatan rangkap (ikatan π) membentuk ikatan tunggal (ikatan α) dengan atom atau gugus tertentu. Selain sifat-sifat tersebut dapat mengalami reaksi polimerisasi dan alkena juga dapat bereaksi dengan oksigen membentuk korbondioksida dan uap air apabila jumlah oksigen melimpah, apabila jumlah oksigen tidak mencukupi maka terbentuk karbonmonooksida dan uap air.
- 14. Kegunaan Alkena sebagai : 1. Dapat digunakan sebagai obat bius (dicampur dengan O2) 2. Untuk memasakkan buah-buahan 3. Bahan baku industri plastik, karet sintetik, dan alkohol.
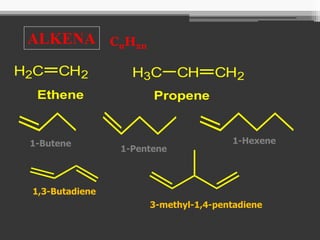
- 16. ALKENA CnH2n CH2H2C H3C CH CH2 Ethene Propene 1-Butene 1-Pentene 1-Hexene 1,3-Butadiene 3-methyl-1,4-pentadiene
- 17. C(6) - 1s2 , 2s2 , 2px 1 , 2py 1 , 2pz 0 C(6) - 1s2 , 2s1 , 2px 1 , 2py 1 , 2pz 1 Hybridization 3 sp2 Three s-bonds p-bondC C H H HH s-bonds – One C-C, two C-H bonds per carbon atom p-bond
- 19. cis- trans- H R R H R R H H H H3C CH3 H CH3 H3C H H cis-2-butene trans-2-butene Geometric isomers have different chemical & physical properties
- 20. TATA NAMA • Rantai utama adalah rantai atom karbon terpanjang yang mempunyai ikatan rangkap. • Nama rantai utama sama dengan alkana, akhiran - ana pada alkana diganti dengan - ena untuk alkena dan - una untuk alkuna. • Penomoran rantai utama dicari agar atom C yang mengandung ikatan rangkap bernomor kecil. • Penamaan dan penomoran gugus cabang sama dengan alkana
- 21. CH3 CH3 CH CH3CHCH CH CH3 C CH CH3 a. b. CH3 CH CH2 CH2 C C CH3CH CH CH CH3 CH CH3 CH c. ( CH3 )2 d.
- 22. E-Z Nomenclature • Gunakan aturan Cahn-Ingold-Prelog untuk menentukan urutan prioritas gugus-gugus yang terikat pada atom C ikatan rangkap. • Jika gugus-gugus yang berprioritas lebih tinggi berada pada sisi yang sama, diberi nama Z (zusammen). • Jika gugus-gugus yang berprioritas lebih tinggi berada pada sisi yang berlawanan, diberi nama E (entgegen).
- 23. Example, E-Z C C H3C H Cl CH2 C C H H CH CH3 Cl1 2 1 2 2Z 2 1 1 2 5E 3,7-dichloro-(2Z, 5E)-2,5-octadiene 3,7-dichloro-(2Z, 5E)-octa-2,5-diene
- 24. Cl Br HF Cl > F Br > H (Z)-2-Bromo-1-chloro-1-fluoroethene Cl H BrF Cl > F Br > H (E)-2-Bromo-1-chloro-1-fluoroethene CH3 H CH3 F F > CH3 CH3 > H (Z)-2-fluorobutene
- 25. Ikatan p adalah area dengan kerapatan electron tinggi, sehingga dapat menyerang molekul yang kekurangan elektron, yang disebut electrophiles, E+ E+ C C + A B CA C B C C H X CH C X X X CX C X CH C OSO3H H OSO3H CH C OH H OH H+ Alkyl Halides Alkyl hydrogen Sulfate Alcohols Dihaloalkanes
- 26. C C H H C H C H Pt or Pd - catalyst solvent, pressure C C H H 2 X CH H CH H Pt - catalyst solvent, pressure Example Pt ethanol, 1 atm cyclohexene cyclohexane Hydrogenation (“Reduction”)
- 27. H2C CH2 KMnO4, - OH, H2O OHOH H2C CH2 + MnO2 OXIDATION OF ALKENES 1,2-Ethanediol Reduction = Gain of electrons Gain of Hydrogen Loss of Oxygen Oxidation = Loss of electrons Loss of Hydrogen Gain of Oxygen An oxidizing agent gets reduced A reducing agent gets oxidized
- 28. C C H H H H H C C H H H C C H H H CH3 H C C CH3 H H C C H H H Cl C C F F F F C C H H C C H H H H C C H H ClH C C F F FF n Polyethylene n Polypropylene propylene ethylene vinyl chloride n n n n Poly(vinylchloride), PVC n n n n TeflonTetrafluoroethene Styrene Polystyrene Polymers are large molecules containing many identical repeating units (100-1000000) Polymerisation reaction is a repetition reaction which combines many small molecules of monomer (alkene) to form a polymer
- 30. merupakan senyawa hidrokarbon tak jenuh yang memiliki 1 ikatan rangkap 3 (–C≡C–). Sifat-nya sama dengan Alkena namun lebih reaktif. Rumus umumnya CnH2n-2 Tata namanya juga sama dengan Alkena, namun akhiran -ena diganti –una
- 32. Sifat Fisika Alkuna merupakan senyawa hidrokarbon tak jenuh yang memiliki 1 ikatan rangkap 3 (– C≡C–). Sifat-nya sama dengan Alkena namun lebih reaktif. 1. Alkuna-alkuna suku rendah pada suhu kamar berwujud gas, sedangkan yang mengandung lima atau lebih atom karbon berwujud gas. 2. Memiliki massa jenis lebih kecil dari air. 3. Tidak larut dalam air tetapi larut dalam pelarut-pelarut organik yang non polar seperti eter, benzena, dan karbon tetraklorida. 4. Titik didih alkuna makin tinggi seiring bertambahnya jumlah atom karbon, tetapi makin rendah apabila terdapat rantai samping atau makin banyak percabangan. Titik didih alkuna sedikit lebih tinggi dari alkana dan alkuna yang berat molekulnya hampir sama.
- 33. Sifat Kimia Alkuna Adanya ikatan rangkap tiga yang dimiliki alkuna memungkinkan terjadinya reaksi adisi, polimerisasi, substitusi dan pembakaran.
- 34. Kegunaan Alkuna 1. etuna (asetilena = C2H2) digunakan untuk mengelas besi dan baja. 2. untuk penerangan 3. Sintesis senyawa lain.
- 35. REAKSI ALKUNA ď‚— Reduksi (reksi dengan H2) ď‚— Adisi (Reaksi dengan X2 dan HX) ď‚— Hidrasi (Reaksi dengan H2O)
- 36. REAKSI REDUKSI CH3 CH3 CH3 CH3 CC HH C C H H CH3C CH3C Pt + Pd/BaSO4 cis-2-butena +2H2 CH3 CH2 CH2 CH3
- 37. REAKSI ADISI CHHC HCl C C H HH Cl CHHC 2HCl CH3 CHCl2 + vinil klorida + 1,1-dikloroetana
- 38. REAKSI HIDRASI CH3 CH3C CH CH3H2O C C H O H C O CH3 + Struk. enol keton H