Laporan tlc
- 1. LAPORAN PRAKTIKUM INSTRUMENTASI KIMIA ACARA : Thin Layer Chromatography(TLC) Disusun Oleh : Nama : Zulhajji Lubis NIM : 011200319 Prodi : Teknokimia Nuklir Semester : III Kelompok :D Teman Kerja : Puji Astuti Asisten : Maria Christina Prihatiningsih SEKOLAH TINGGI TEKNOLOGI NUKLIR BADAN TENAGA NUKLIR NASIONAL YOGYAKARTA 2013
- 2. A. TUJUAN a. Mengenal salah satu pemisahan zat dengan kromatografi. b. Mengidentifikasi klorofil dalam hijau daun bayam dengan kromatografi kertas dan kromatografi lapisan tipis. c. Mengidentifikasi komponen penyusun tinta dengan menggunakan kromatografi kertas dan kromatografi lapisan tipis. B. DASAR TEORI Kromatografi adalah suatu teknik pemisahan molekul berdasarkan perbedaan pola pergerakan antara fase gerak dan fase diam untuk memisahkan komponen (berupa molekul) yang berada pada larutan. Molekul yang terlarut dalam fase gerak, akan melewati kolom yang merupakan fase diam. Molekul yang memiliki ikatan yang kuat dengan kolom akan cenderung bergerak lebih lambat dibanding molekul yang berikatan lemah. Dengan ini, berbagai macam tipe molekul dapat dipisahkan berdasarkan pergerakan pada kolom. Salah satu jenis kromatografi adalah TLC atau kromatografi lapis tipis. Kromatografi lapis tipis merupakan salah satu analisis kualitatif dari suatu sampel yang ingin dideteksi dengan memisahkan komponen-komponen sampel berdasarkan perbedaan kepolaran. Kromatografi lapis tipis (KLT) adalah salah satu metode pemisahan komponen menggunakan fasa diam berupa plat dengan lapisan bahan adsorben inert. KLT merupakan salah satu jenis kromatografi analitik. KLT sering digunakan untuk identifikasi awal, karena banyak keuntungan menggunakan KLT, di antaranya adalah sederhana dan murah. KLT termasuk dalam kategori kromatografi planar, selain kromatografi kertas. Kromatografi lapis tipis menggunakan plat tipis yang dilapisi dengan adsorben seperti silika gel, aluminium oksida (alumina) maupun selulosa. Adsorben tersebut berperan sebagai fasa diam. Fasa gerak yang digunakan dalam KLT sering disebut dengan eluen. Pemilihan eluen didasarkan pada polaritas senyawa dan biasanya merupakan campuran beberapa cairan yang berbeda polaritas, sehingga didapatkan perbandingan tertentu. Eluen KLT dipilih dengan cara trial and error.Kepolaran eluen sangat berpengaruh terhadap Rf (faktor retensi) yang diperoleh.KLT sangat berguna untuk mengetahui jumlah komponen dalam sampel. Peralatan yang digunakan untuk KLT adalah chamber (wadah untuk proses KLT) , pinset, plat KLT, dan eluen. Inilah langkah-langkah memakai KLT: 1. Potong plat sesuai ukuran. Biasanya, untuk satu spot menggunakan plat selebar 1 cm. Berarti jika menguji 3 sampel (3 spot) berarti menggunakan plat selebar 3 cm. 2. Buat garis dasar (base line) di bagian bawah, sekitar 0,5 cm dari ujung bawah plat, dan garis akhir di bagian atas. 3. Menggunakan pipa kapiler, totolkan sampel cairan yang telah disiapkan sejajar, tepat di atas base line. Jika sampel padat, larutkan pada pelarut tertentu. Keringkan totolan. 4. Dengan pipet yang berbeda, masukkan masing-masing eluen ke dalam chamber dan campurkan. 5. Tempatkan plat pada chamber berisi eluen. Base line jangan sampai tercelup oleh ulen. Tutuplah chamber.
- 3. 6. Tunggu eluen mengelusi sampel sampai mencapai garis akhir, di sana pemisahan akan terlihat. 7. Setelah mencapai garis akhir, angkat plat dengan pinset, keringkan dan ukur jarak spot. Jika spot tidak kelihatan, amati pada lampu UV. Jika masih tak terlihat, semprot dengan pewarna tertentu seperti kalium kromat atau ninhidrin. Kromatografi digunakan untuk memisahkan campuran dari substansinya menjadi komponen-komponennya. Seluruh bentuk kromatografi bekerja berdasarkan prinsip yang sama. Seluruh bentuk kromatografi memiliki fase diam (berupa padatan atau cairan yang didukung pada padatan) dan fase gerak (cairan atau gas). Fase gerak mengalir melalui fase diam dan membawa komponen-komponen dari campuran bersama-sama. Komponen-komponen yang berbeda akan bergerak pada laju yang berbeda pula. Kromatografi lapis tipis digunakan untuk memisahkan komponenkomponen atas dasar perbedaan adsorpsi atau partisi oleh pase diam dibawah gerakan pelarut pengembang. Pada dasarnya KLT sangat mirip dengan kromatografi kertas , terutama pada cara pelaksanaannya. Perbedaan nyatanya terlihat pada fase diamnya atau media pemisahnya, yakni digunakan lapisan tipis adsorben sebagai pengganti kertas. Bahan adsorben sebagai fasa diam dapat digunakan silika gel, alumina dan serbuk selulosa. Partikel selika gel mengandung gugus hidroksil pada permukaannya yang akan membentuk ikatan hidrogen dengan molekul polar air. Fase diam untuk kromatografi lapis tipis seringkali juga mengandung substansi yang mana dapat berpendar flour dalam sinar ultra violet. Fase gerak merupakan pelarut atau campuran pelarut yang sesuai. Pada identifikasi noda atau penampakan noda, jika noda sudah bewarna dapat langsung diperiksa dan ditentukan harga Rf. Rf merupakan nilai dari Jarak relative pada pelarut. Harga Rf dihitung sebagai jarak yang ditempuh oleh komponen dibagi dengan jarak tempuh oleh eluen ( fase gerak ) untuk setiap senyawa berlaku rumus sebagai berikut: Faktor retensi (Rf) adalah jarak yang ditempuh oleh komponen dibagi dengan jarak yang ditempuh oleh eluen. Rumus faktor retensi adalah: Nilai Rf sangat karakterisitik untuk senyawa tertentu pada eluen tertentu. Hal tersebut dapat digunakan untuk mengidentifikasi adanya perbedaan senyawa dalam sampel. Senyawa yang mempunyai Rf lebih besar berarti mempunyai kepolaran yang rendah, begitu juga sebaliknya. Hal tersebut dikarenakan fasa diam bersifat polar. Senyawa yang lebih polar akan tertahan kuat pada fasa diam, sehingga menghasilkan nilai Rf yang rendah.
- 4. C. ALAT DAN BAHAN 1) Alat 1) Gelas ukur 250 mL 2) Penumbuk porselin 3) Corong pemisah 4) Corang gelas 5) pipet ukur 2) Bahan 1) Bayam 2) metanol 3) aseton 4) dietileter 5) Mr. Muscle 6) Tinta komputer 7) TLC 8) Kertas kromatografi D. LANGKAH KERJA 1) Ditumbuk bayam dengan menggunakan penumbuk porselin sampai halus. 2) Disaring dengan menggunakan penyaring (kertas saring) untuk mengambil klorofil dari bayam (air bayam). 3) Dimasukan hasil saringan kedalam corong pemisah dan ditambahkan dietil eter secukupnya (sampai dietil eter membasahi hasil saringan air bayam). 4) Dikocok samapi tercampur secara merata dan keluarkan gas buangan hasil reaksi tersebut secara perlahan. 5) Didiamkan hasil ekstraksi di dalam corong pemisah samapi terbentuk perbedaan fase ekstraksi. 6) Dikleuarkan hasil ekstraksi dari corong pemisah ke wadah kaca arloji. 7) Dipipet dengan menggunakan pendose dan di teteskan pada kromatografi kertas dan pada kromatografi lapisan tipis. Jangan samapi berlebihan atau (over load). Ditunggu hingga kering. 8) Dipipet tinta komputer yang disediakan dan diteteskan pada kertas dan pada kromatografi lapisan tipis. Jangan samapi berlebihan atau (over load). Ditunggu hingga kering. 9) Disiapkan pelarut yaitu aseton, metanol dan Mr. Muschle di dalam gelas ukur 250 mL secukupnya ┬▒ 5 mL.
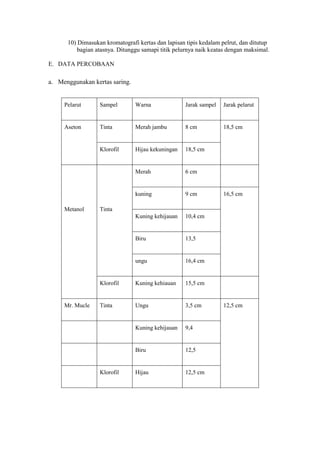
- 5. 10) Dimasukan kromatografi kertas dan lapisan tipis kedalam pelrut, dan ditutup bagian atasnya. Ditunggu samapi titik pelurnya naik keatas dengan maksimal. E. DATA PERCOBAAN a. Menggunakan kertas saring. Pelarut Sampel Warna Jarak sampel Jarak pelarut Aseton Tinta Merah jambu 8 cm 18,5 cm Klorofil Hijau kekuningan 18,5 cm Merah 6 cm kuning 9 cm Kuning kehijauan 10,4 cm Biru 13,5 ungu 16,4 cm Klorofil Kuning kehiauan 15,5 cm Tinta Ungu 3,5 cm Kuning kehijauan 9,4 Biru 12,5 Hijau 12,5 cm Metanol Mr. Mucle 16,5 cm Tinta Klorofil 12,5 cm
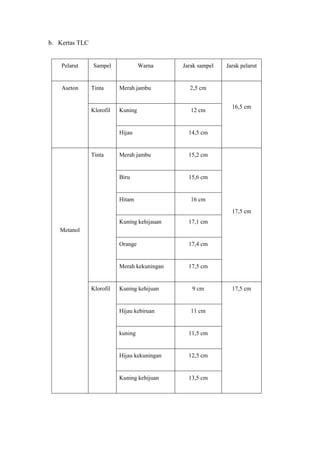
- 6. b. Kertas TLC Pelarut Aseton Sampel Warna Jarak sampel Tinta Merah jambu 2,5 cm Klorofil Kuning 12 cm Jarak pelarut Hijau 14,5 cm Merah jambu 15,2 cm Biru Tinta 16,5 cm 15,6 cm Hitam 16 cm 17,5 cm Kuning kehijauan 17,1 cm Orange 17,4 cm Merah kekuningan 17,5 cm Metanol Klorofil Kuning kehijuan 9 cm Hijau kebiruan 11 cm kuning 11,5 cm Hijau kekuningan 12,5 cm Kuning kehijuan 13,5 cm 17,5 cm
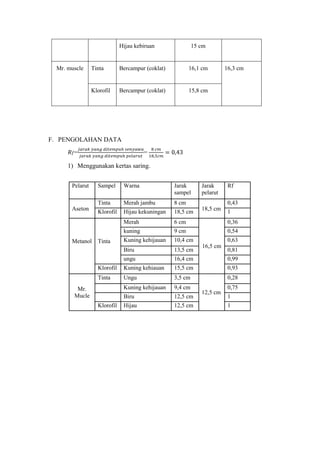
- 7. Hijau kebiruan Mr. muscle 15 cm Tinta Bercampur (coklat) 16,1 cm Klorofil Bercampur (coklat) 16,3 cm 15,8 cm F. PENGOLAHAN DATA = = 1) Menggunakan kertas saring. Pelarut Warna Jarak sampel Tinta Aseton Sampel Merah jambu 8 cm Rf 0,43 18,5 cm 18,5 cm 6 cm 0,36 kuning Tinta Hijau kekuningan Merah Metanol Klorofil Jarak pelarut 1 9 cm 0,54 Kuning kehijauan 10,4 cm 0,63 16,5 cm Biru 13,5 cm ungu 16,4 cm 0,99 Klorofil Kuning kehiauan 15,5 cm 0,93 Tinta Ungu 3,5 cm 0,28 Kuning kehijauan 9,4 cm Biru 12,5 cm Hijau 12,5 cm Mr. Mucle Klorofil 12,5 cm 0,81 0,75 1 1
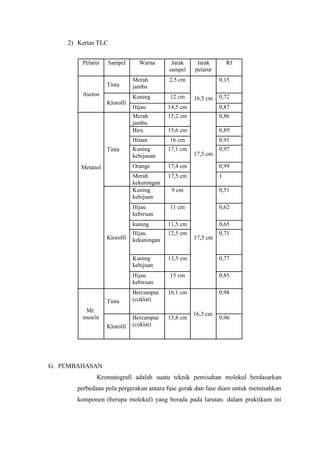
- 8. 2) Kertas TLC Pelarut Sampel Warna Jarak sampel Aseton Klorofil Merah jambu 2,5 cm Kuning Tinta 12 cm Jarak pelarut Rf 0,15 16,5 cm 0,72 Hijau 14,5 cm 0,87 Merah jambu Biru 15,2 cm 0,86 15,6 cm 0,89 Hitam 16 cm 0,91 17,1 cm 17,4 cm 0,99 Merah kekuningan Kuning kehijuan Metanol Kuning kehijauan Orange Tinta 17,5 cm 1 17,5 cm 0,97 9 cm 0,51 11 cm 0,62 kuning 11,5 cm 0,65 Hijau kekuningan 12,5 cm Kuning kehijuan 13,5 cm 0,77 Hijau kebiruan 15 cm 0,85 16,1 cm 0,98 Tinta Bercampur (coklat) 15,8 cm Klorofil Bercampur (coklat) Hijau kebiruan Klorofil Mr. muscle 17,5 cm 16,3 cm 0,71 0,96 G. PEMBAHASAN Kromatografi adalah suatu teknik pemisahan molekul berdasarkan perbedaan pola pergerakan antara fase gerak dan fase diam untuk memisahkan komponen (berupa molekul) yang berada pada larutan. dalam praktikum ini
- 9. digunakan teknik kromatografi lapis tipis dan kromatografi jenis kertas. pada teknik ini gunakan tiga larutan yaitu aseton metanol dan Mr. Muscle. Pada percobaan pertama adalah teknik kromatografi menggunakan kertas saring. Sampel yang digunakan adalah klorofil dan campuran warna tinta printer yang diteteskan pada kertas saring dan dicelupkan masing masing pada larutan aseton, metanol dan Mr Muscle. Pada saat digunakan pelarut aseton, warna klorofil berubah dari warna hijau kemudian menjadi hijau kekuningan dengan waktu retensi sedangkan tinta dari warna hitam menjadi merah jambu dengan waktu retensi 0,43. Sedangkan pada saat digunakan pelarut etanol, warna tinta dapat terpisah menjadi beberapa warna begitu juga saat digunakan pelarut Mr Muscle warna tinta terpisah menjadi beberapa warna, sedangkan warna klorofil menjadi hijau kekuningan dengan waktu retensi sesuai dengan tabel perhitugan waktu retensi di atas. Dari data tersebut dapat diketahui bahwa jarak yang terbentuk tergantung dari kelarutan sampel terhadap pelarutnya. Jika sampel tersebut juga merupakan larutan yang polar maka akan larut sangat baik dalam pelarut etanol yang merupakan pelarut polar. Jika sampel bukan merupakan larutan yang polar maka pelarut akan sulit untuk melarutkan sampel dan menarik pelarut sampai pada ┬Š bagian kertas semaksimal mungkin. Semakin besar jarak sampel yang didapatkan maka nilai Rf akan semakin besar pula. Sesuai dengan teori dari bahwa Rf = Jarak sampel dari titik awal / jarak pelarut dari titik awal, menunjukkan bahwa nilai Rf sebanding dengan jarak sampel. Percobaan kedua adalah kromatografi lapis tipis. Pada teknik ini juga digunakan tiga pelarut yaitu aseton metanol dan Mr Muscle dengan sample klorofil dan tinta. dengan perhitungan juga dapat ditentukan waktu retensi sampel. Dari data perhitungan waktu retensi dapat diketahui bahwa pelarut metanol lebih efektif jika digunakan untuk teknik kromatografi. Jika dibandingkan dengan kromatografi lapis, pemisahan warna pada kromatografi kertas lebih lebih mudah dilihat. dengan demikian kromatografi kertas mempunyai kemampuan lebih baik dalam pemisahan warna.
- 10. H. KESIMPULAN 1. Warna yang ditimbulkan oleh setiap pelarut dengan menggunakan kromatografi kertas maupun dengan menggunakan kromatografi lapisan tipis berbeda tergantung dengan pelarut yang digunakan. 2. Kromatografi adalah teknik untuk memisahkan campuran menjadi komponennya dengan bantuan perbedaan sifat fisik masing-masing komponen. 3. Waktu retensi dapat dihitung dengan membandingkan jarak yang ditempuh senyawa dengan jarak yang ditempuh pelarut. 4. Kromatografi kertas lebih baik digunakan dalam teknik pmisahan warna jika dibandingkan dengan kromatografi lapis tipis dan pelarut yang paling bagus adalah metanol I. DAFTAR PUSTAKA http://id.wikipedia.org/wiki/Kromatografi_lapis_tipis diakses 7 Desember 2013 pukul 18.19 WIB http://www.ilmukimia.org/2013/05/kromatografi-lapis-tipis-klt.html diakses 7 Desember 2013 pukul 18.19 WIB http://erlindaadonara.blogspot.com/2013/09/kromatografi-lapis-tipis.html diakses 7 Desember 2013 pukul 18.19 WIB Asisten Maria Christina Yogyakarta, 7 Desember 2013 Praktikan Zulhajji Lubis