PramoninД— sieros rЕ«gЕЎties gamyba
- 1. PramoninД— sieros rЕ«gЕЎties gamyba
- 2. Tikslai Atskleisti chemijos mokslo ryЕЎДЇ su ЕЎiuolaikine chemijos pramone. ApibrД—Еѕti cheminД—s technologijos sД…vokД… bei cheminД—s technologijos procesus. IЕЎplД—sti besidominДЌiЕі chemija mokiniЕі akiratДЇ, labiau ДЇprasminti chemijos pamokose ДЇgytas Еѕinias.
- 3. Uždaviniai Kartu su mokiniais nueiti sieros rūgšties gamybos kelią nuo žaliavos iki galutinio produkto. Savarankiškai nustatyti cheminių reakcijų seką technologiniame procese ir pavaizduoti jas, naudojant IT. Virtualiai nukeliauti į Kėdainių „LIFOSĄ“ ir išspręsti konkrečias mokytojų pateiktas užduotis. Naudojantis IT surinkti informaciją apie sieros rūgšties naudojimo sritis.
- 4. Istorija Alchemikai gamina sieros rЕ«gЕЎtДЇ jau X amЕѕiuje iЕЎ geleЕѕies (III) sulfato. JД… plaДЌiai naudoja vaistininkai, aukso bei sidabro gaminiЕі meistrai. Sieros rЕ«gЕЎties pramonД— iЕЎsivysto XVII amЕѕiuje.
- 5. Jau XVII a. pramonД— naudoja sieros rЕ«gЕЎtДЇ: tekstilД—s gamybai, metalЕі gamybai, naftos perdirbimui, muilo virimui, stiklo pramonei
- 6. Chemijos pramonД—s ir technologinio proceso sД…voka Chemijos pramonД— gamina chemines medЕѕiagas. Technologinis procesas в•ђ gamyboje vykstanДЌios cheminД—s reakcijos + parametrai. Parametrai - tai slД—gis, temperatЕ«ra, koncentracijos ir katalizatoriai.
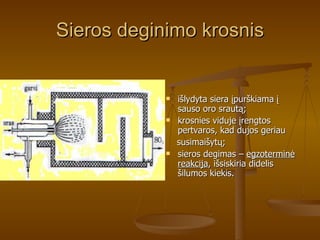
- 8. Sieros deginimo krosnis išlydyta siera įpurškiama į sauso oro srautą; krosnies viduje įrengtos pertvaros, kad dujos geriau susimaišytų; sieros degimas – egzoterminė reakcija , išsiskiria didelis šilumos kiekis.
- 9. Kontaktinė SO 2 oksidacija SO 2 dujos teka išoriniu šilumokaičiu Tarp katalizatoriaus sluoksnių sumontuoti vidiniai šilumokaičiai temperatūros palaikymui SO 2 dujos oksiduojasi, pereidamos visus katalizatoriaus sluoksnius Šis procesas – grįžtamasis, egzoterminis ir katalitinis.
- 10. KontaktinД—s masД—s katalizatorius V 2 O 5 В· 12SiO 2 В· 0,5Al 2 O 3 В· 2K 2 O В· 3BaO В· 2KCl Jo veiklioji dalis - V 2 O 5 Katalizatorius greitina SO 2 oksidacijД….
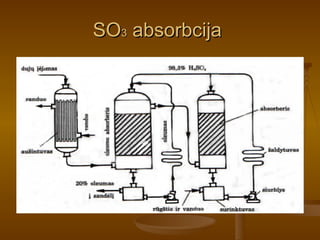
- 11. SO 3 absorbcija
- 12. SO 3 absorbcija Prieš absorbcijos bokštus SO 3 dujos aušinamos; Absorbcijos bokštų paprastai būna du. Bokštai užpildomi įkrova, kuri didina SO 3 ir oleumo sąlytį. Oleumas – tai pastovios sudėties junginys, susidarantis SO 3 tirpstant sieros rūgštyje.
- 13. Sieros rЕ«gЕЎtis pagaminta ! Keliaukime ДЇ uЕѕduotis
- 14. Pirmoji uЕѕduotis Prisiminkite ir paЕѕymД—kite kuo daugiau chemijos pramonД—s ДЇmoniЕі Lietuvoje .
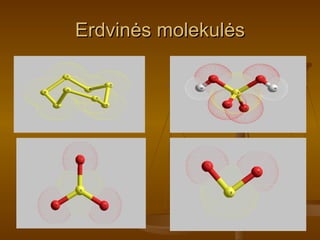
- 15. Antroji uЕѕduotis Remdamiesi erdvinД—mis struktЕ«rinД—mis molekulД—mis, uЕѕraЕЎykite ЕЎiЕі cheminiЕі medЕѕiagЕі molekulines formules ir suraЕЎykite jas nuoseklaus technologinio proceso seka.
- 17. TreДЌioji uЕѕduotis S+... -> SO 2 SO 2 +... ->SO 3 Baikite raЕЎyti ЕЎias reakcijЕі lygtis. IЕЎlyginkite jas. PaЕѕymД—kite oksidatoriЕі ir reduktoriЕі.
- 18. Ketvirtoji uЕѕduotis Katalizatorius V 2 O 5 В· 12SiO 2 В· 0,5Al 2 O 3 В· 2K 2 O В· 3BaO В· 2KCl Kam jis reikalingas? Nurodykite jo sudedamЕіjЕі daliЕі masiЕі santykius. ApskaiДЌiuokite V 2 O 5 masД—s dalДЇ kontaktiniame katalizatoriuje.
- 19. Penktoji uЕѕduotis SO 3 + ... ->H 2 SO 4 Д®raЕЎykite praleistД… junginДЇ ДЇ reakcijos lygtДЇ. ApibЕ«dinkite SO 3 prigimtДЇ. Kas susidaro, tirpstant tokiems oksidams vandenyje?
- 20. KЕ«rybinД— uЕѕduotis Sudarykite schemas, paveikslД—lius, diagramas apie H 2 SO 4 panaudojimo sritis. SД—kmД—s darbe !