àžȘàžČàžŁàžàžŁàž°àžàžàžàčàžźàčàž¶ÏžŁàžàžČàžŁàčàžàžàžàčàžàž àžàž”àž àčàžàžàč
- 2. àžȘàžČàžŁàžàžŁàž°àžàžàžàčàžàž„àčàžàž ïŹàčàžàž„àčàžàž(Alkanes) àžĄàž”àžȘàžàžŁàžàž±àž§àčàž CnH2n+2 àžč àč ïŹàžàž±àžàčàžàč àžàžȘàžČàžŁàžàžŁàž°àžàžàžàčàžźàčàž¶ÏžŁàžàžČàžŁàčàžàžàžàžàžŁàž°àčàž àžàžàžŽàžĄàžàž±àž§(Saturated àč hydrocarbon) ïŹàžàž±àžàžàž°àžŁàž°àž«àž§àčàžČàžàžàžČàžŁàčàžàžàžàžàž°àžàžàžĄàčàžàčàžĄàčàž„àžàžžàž„àčàžàč àžàžàž±àžàžàž°àčàžàž”àžąàž§ àč àžàž±àžàž«àžĄàž àč ïŹàžĄàž”àžàžàčàžàžŁàžàžȘàžŁàčàžČàžàžàž”àčàžàč àžàčàžàčàčàžàžŽàž(àčàžàčàžàžŁàžàčàž„àž°àčàžàčàžàž) àčàž„àž°àčàžàčàžàžŽàž àž±àč àč àžŽàč ïŹàčàžàžŁàžàžȘàžŁàčàžČàžàžàž”àčàžàč àžàčàžàčàžàžŽàžàčàžŁàž”àžąàžàž§àčàžČàčàžàčàžàž„àčàžàž„àčàžàž(Cycloalkane) àžĄàž” àč àžȘàžčàžàžŁàžàž±àž§àčàž CnH2n àč
- 3. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àčàžàž Alkanes(CnH2n+2) àč ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž°àžàžžàžàčàžàž·àžàžàžàžàžàčàžàž„àčàžàžàčàžàžàžŁàžàžàžČàžàžàžàžŽàž àžȘàžčàžàžŁàčàžĄàčàž„àžàžžàž„ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§(ï°C) àžàžžàžàčàžàž·àžàž(ï°C) CH4 -182.5 -161.5 C2H6 -182.8 -88.6 C3H8 -187.7 -42.1 C4H10 -138.3 -0.5 C5H12 -129.7 36.1 àč àž àčàžàžĄàžčàž„àžàžČàž : àčàžàžĄàž” àčàž„àčàžĄàč àžȘàžàžČàžàž±àžàžȘàžàčàžȘàžŁàžŽàžĄàžàžČàžŁàžȘàžàžàž§àžŽàžàžąàžČàžšàžČàžȘàžàžŁàčàčàž„àž°àčàžàžàčàžàčàž„àžąàž”
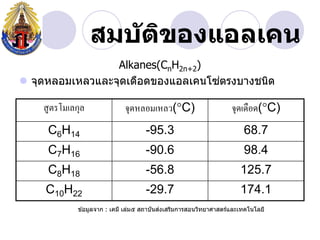
- 4. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àčàžàž Alkanes(CnH2n+2) àč ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž°àžàžžàžàčàžàž·àžàžàžàžàžàčàžàž„àčàžàžàčàžàžàžŁàžàžàžČàžàžàžàžŽàž àžȘàžčàžàžŁàčàžĄàčàž„àžàžžàž„ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§(ï°C) àžàžžàžàčàžàž·àžàž(ï°C) C6H14 -95.3 68.7 C7H16 -90.6 98.4 C8H18 -56.8 125.7 C10H22 -29.7 174.1 àč àž àčàžàžĄàžčàž„àžàžČàž : àčàžàžĄàž” àčàž„àčàžĄàč àžȘàžàžČàžàž±àžàžȘàžàčàžȘàžŁàžŽàžĄàžàžČàžŁàžȘàžàžàž§àžŽàžàžąàžČàžšàžČàžȘàžàžŁàčàčàž„àž°àčàžàžàčàžàčàž„àžąàž”
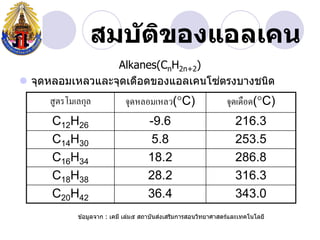
- 5. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àčàžàž Alkanes(CnH2n+2) àč ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž°àžàžžàžàčàžàž·àžàžàžàžàžàčàžàž„àčàžàžàčàžàžàžŁàžàžàžČàžàžàžàžŽàž àžȘàžčàžàžŁàčàžĄàčàž„àžàžžàž„ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§(ï°C) àžàžžàžàčàžàž·àžàž(ï°C) C12H26 -9.6 216.3 C14H30 5.8 253.5 C16H34 18.2 286.8 C18H38 28.2 316.3 C20H42 36.4 343.0 àč àž àčàžàžĄàžčàž„àžàžČàž : àčàžàžĄàž” àčàž„àčàžĄàč àžȘàžàžČàžàž±àžàžȘàžàčàžȘàžŁàžŽàžĄàžàžČàžŁàžȘàžàžàž§àžŽàžàžąàžČàžšàžČàžȘàžàžŁàčàčàž„àž°àčàžàžàčàžàčàž„àžąàž”
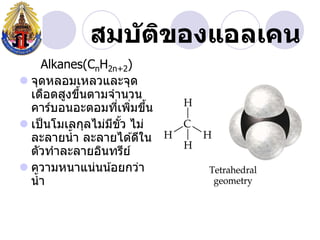
- 6. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àčàžàž Alkanes(CnH2n+2) ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž°àžàžžàž àčàžàž·àžàžàžȘàžčàžàžàž¶àžàžàžČàžĄàžàžČàžàž§àž àč àžàžČàžŁàčàžàžàžàžàž°àžàžàžĄàžàž”àčàžàžŽàžĄàžàž¶àž àč àč àč ïŹ àčàžàč àžàčàžĄàčàž„àžàžžàž„àčàžĄàčàžĄàžàž§ àčàžĄàč àž” àž±àč àž„àž°àž„àžČàžąàžàč àžČ àž„àž°àž„àžČàžąàčàž àčàžàž”àčàž àžàž±àž§àžàžČàž„àž°àž„àžČàžąàžàžŽàžàžàžŁàž”àžą àč ïŹ àžàž§àžČàžĄàž«àžàžČàčàžàčàžàž àčàžàžąàžàž§àčàžČ àžàč àžČ
- 7. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àčàžàž Alkanes(CnH2n+2) àžȘàžčàžàžŁ àžàžžàž àžàžžàžàčàžàž·àžàž ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž°àžàžžàžàčàžàž·àžàž àčàžàžŁàžàžȘàžŁàčàžČàž àž«àž„àžàžĄàčàž«àž„àž§ (ï°C) àžàžàžàčàžàž„àčàžàžàčàžàžàžŁàžàčàž„àž°àčàžàč àč (ï°C) àžàžŽàžàžàžČàžàžàžàžŽàž àč -129.7 36.1 àžàžČàžàžàč àžàžĄàžčàž„ àžàž±àžàčàžŁàž”àžąàžàžȘàžŁàžžàžàžàž§àžČàžĄàžȘàž±àžĄàžàž±àžàžàč -156.6 27.9 àžàžąàč àžČàžàčàžŁ -166.0 9.5 àž àčàžàžĄàžčàž„àžàžČàž : àčàžàžĄàž”àžàžàžàžŁàž”àžąàčàžàž·àžàžàž àčàž àžĄ.àžŁàžČàžĄàžàžČàčàž«àž àžŽ àč àč
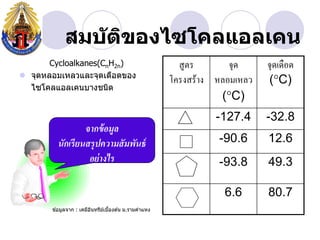
- 8. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàčàžàž„àčàžàž„àčàžàž Cycloalkanes(CnH2n) àžȘàžčàžàžŁ àžàžžàž àžàžžàžàčàžàž·àžàž ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž°àžàžžàžàčàžàž·àžàžàžàžàž àčàžàžŁàžàžȘàžŁàčàžČàž àž«àž„àžàžĄàčàž«àž„àž§ (ï°C) àčàžàčàžàž„àčàžàž„àčàžàžàžàžČàžàžàžàžŽàž (ï°C) -127.4 -32.8 àžàžČàžàžàč àžàžĄàžčàž„ àžàž±àžàčàžŁàž” àžąàžàžȘàžŁàžžàžàžàž§àžČàžĄàžȘàž±àžĄàžàž±àžàžàč -90.6 12.6 àžàžąàčàžČàžàčàžŁ -93.8 49.3 6.6 80.7 àž àčàžàžĄàžčàž„àžàžČàž : àčàžàžĄàž”àžàžàžàžŁàž”àžąàčàžàž·àžàžàž àčàž àžĄ.àžŁàžČàžĄàžàžČàčàž«àž àžŽ àč àč
- 9. àžàžàžŽàžàžŁàžąàžČàčàžàžĄàž”àŸșàžàžàčàžàž„àčàžàž àžŽ àžŽ ïŹàžàžàžŽàžàžŁàžąàžČàžàžČàžŁàčàžàžČàčàž«àžĄ àč(Combustion) àžŽ àžŽ CH4 + 2O2 CO2 + 2H2O 2C6H14+ 19O2 12CO2 + 14H2O + 9O2 6CO2 + 6H2O
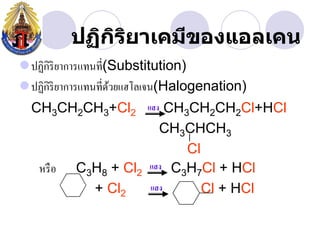
- 10. àžàžàžŽàžàžŁàžąàžČàčàžàžĄàž”àŸșàžàžàčàžàž„àčàžàž àžŽ àžŽ ïŹàžàžàžŽàžàžŽàžŁàžŽàžąàžČàžàžČàžŁàčàžàžàžàž”àč(Substitution) ïŹàžàžàžŽàžàžŽàžŁàžŽàžąàžČàžàžČàžŁàčàžàžàžàž”àčàžàž§àžąàčàžźàčàž„àčàžàž(Halogenation) àč CH3CH2CH3+Cl2 àčàžȘàž CH3CH2CH2Cl+HCl CH3CHCH3 Cl àž«àžŁàž· àž C3H8 + Cl2 àčàžȘàž C3H7Cl + HCl + Cl2 àčàžȘàž Cl + HCl
- 11. àžàžàžŽàžàžŁàžąàžČàčàžàžĄàž”àŸșàžàžàčàžàž„àčàžàž àžŽ àžŽ ïŹàžàžàžŽàžàžŁàžąàžČàčàžàžàžàž”àž àčàž§àžąàž«àžĄàžčàčàžàčàžàžŁ(Nitration) àžŽ àžŽ àč àč CH4 + HNO3 400-500ï°C CH3-NO2 + H2O àžàž§àžČàžĄàž àž±àžàžȘàžčàž
- 12. àžȘàžČàžŁàžàžŁàž°àžàžàžàčàžàž„àžàž”àž ïŹàčàžàž„àžàž”àž(Alkenes) àžĄàž”àžȘàžčàžàžŁàžàž±àž§àčàž CnH2n àč ïŹàžàž±àžàčàžàč àžàžȘàžČàžŁàžàžŁàž°àžàžàžàčàžźàčàž¶ÏžŁàžàžČàžŁàčàžàžàžàžàžŁàž°àčàž àžàčàžĄàčàžàžŽàčàžĄàžàž±àž§ (Unsaturated hydrocarbon) ïŹàžàž±àžàžàž°àžŁàž°àž«àž§àčàžČàžàžàžČàžŁàčàžàžàžàžàž°àžàžàžĄàčàžàčàžĄàčàž„àžàžžàž„àžĄàž”àžàžàžàž°àžàžčàč(C=C) àčàž„àž°àčàžàč àž àž± àž«àžĄàžčàčàžàž±àžàžàčàžàžàžàčàžàž„àžàž”àž ïŹàžĄàž”àžàč àžàčàžàžŁàžàžȘàžŁàčàžČàžàžàž”àčàčàžàč àžàčàžàčàčàžàžŽ àž(àčàžàčàžàžŁàžàčàž„àž°àčàžàčàžàžŽàčàž) àčàž„àž°àčàžàčàžàžŽàž àž± ïŹàčàžàžŁàžàžȘàžŁàčàžČàžàžàž”àčàčàžàč àžàčàžàčàžàžŽàžàčàžŁàž” àžąàžàž§àčàžČàčàžàčàžàž„àčàžàž„àžàž”àž(Cycloalkene) àžĄàž” àžȘàžčàžàžŁàžàž±àž§àčàž CnH2n-2 àč
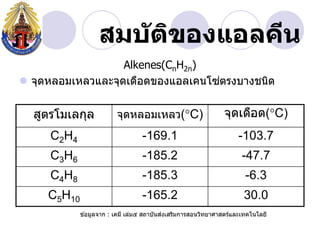
- 13. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àžàž”àž Alkenes(CnH2n) àč ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž°àžàžžàžàčàžàž·àžàžàžàžàžàčàžàž„àčàžàžàčàžàžàžŁàžàžàžČàžàžàžàžŽàž àžȘàžčàžàžŁàčàžĄàčàž„àžàžžàž„ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§(ï°C) àžàžžàžàčàžàž·àžàž(ï°C) C2H4 -169.1 -103.7 C3H6 -185.2 -47.7 C4H8 -185.3 -6.3 C5H10 -165.2 30.0 àč àž àčàžàžĄàžčàž„àžàžČàž : àčàžàžĄàž” àčàž„àčàžĄàč àžȘàžàžČàžàž±àžàžȘàžàčàžȘàžŁàžŽàžĄàžàžČàžŁàžȘàžàžàž§àžŽàžàžąàžČàžšàžČàžȘàžàžŁàčàčàž„àž°àčàžàžàčàžàčàž„àžąàž”
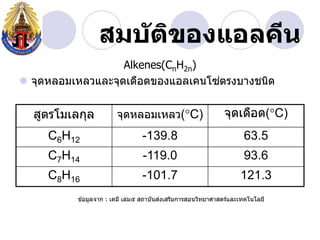
- 14. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àžàž”àž Alkenes(CnH2n) àč ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž°àžàžžàžàčàžàž·àžàžàžàžàžàčàžàž„àčàžàžàčàžàžàžŁàžàžàžČàžàžàžàžŽàž àžȘàžčàžàžŁàčàžĄàčàž„àžàžžàž„ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§(ï°C) àžàžžàžàčàžàž·àžàž(ï°C) C6H12 -139.8 63.5 C7H14 -119.0 93.6 C8H16 -101.7 121.3 àč àž àčàžàžĄàžčàž„àžàžČàž : àčàžàžĄàž” àčàž„àčàžĄàč àžȘàžàžČàžàž±àžàžȘàžàčàžȘàžŁàžŽàžĄàžàžČàžŁàžȘàžàžàž§àžŽàžàžąàžČàžšàžČàžȘàžàžŁàčàčàž„àž°àčàžàžàčàžàčàž„àžąàž”
- 15. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àžàž”àž Alkanes(CnH2n) ïŹ àčàžàž§àčàž àčàžĄàžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž° àžàžžàžàčàžàž·àžàžàžȘàžčàžàžàž¶àžàžàžČàžĄàžàžČàžàž§àž àč àžàžČàžŁàčàžàžàžàžàž°àžàžàžĄàžàž”àčàžàžŽàžĄàžàž¶àž àč àč àč ïŹ àčàžàč àžàčàžĄàčàž„àžàžžàž„àčàžĄàčàžĄàžàž§ àčàžĄàč àž” àž±àč àž„àž°àž„àžČàžąàžàč àžČ ïŹ àžàž§àžČàžĄàž«àžàžČàčàžàčàžàž àčàžàžąàžàž§àčàžČàžàč àžČ
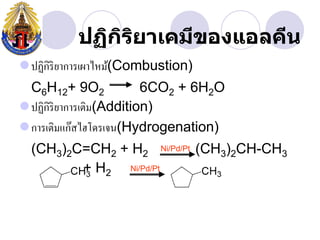
- 16. àžàžàžŽàžàžŁàžąàžČàčàžàžĄàž”àŸșàžàžàčàžàž„àžàž”àž àžŽ àžŽ ïŹàžàžàžŽàžàžŽàžŁàžŽàžąàžČàžàžČàžŁàčàžàžČàčàž«àžĄàč(Combustion) C6H12+ 9O2 6CO2 + 6H2O ïŹàžàžàžŽàžàžŽàžŁàžŽàžąàžČàžàžČàžŁàčàžàžŽàžĄ(Addition) ïŹàžàžČàžŁàčàžàžŽàžĄàčàžàčàžȘàčàžźàčàžàžŁàčàžàž(Hydrogenation) (CH3)2C=CH2 + H2 Ni/Pd/Pt (CH3)2CH-CH3 + H2 Ni/Pd/Pt
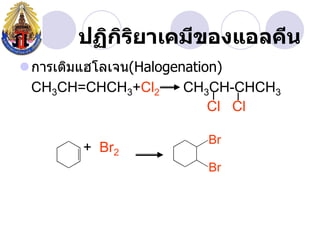
- 17. àžàžàžŽàžàžŁàžąàžČàčàžàžĄàž”àŸșàžàžàčàžàž„àžàž”àž àžŽ àžŽ ïŹàžàžČàžŁàčàžàžŽàžĄàčàžźàčàž„àčàžàž(Halogenation) CH3CH=CHCH3+Cl2 CH3CH-CHCH3 Cl Cl Br + Br2 Br
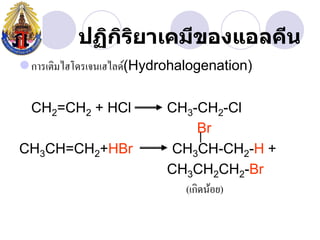
- 18. àžàžàžŽàžàžŁàžąàžČàčàžàžĄàž”àŸșàžàžàčàžàž„àžàž”àž àžŽ àžŽ ïŹàžàžČàžŁàčàžàžŽàžĄàčàžźàčàžàžŁàčàžàžàčàžźàčàž„àžàč(Hydrohalogenation) CH2=CH2 + HCl CH3-CH2-Cl Br CH3CH=CH2+HBr CH3CH-CH2-H + CH3CH2CH2-Br (àčàžàžŽàžàžàčàžàžą)
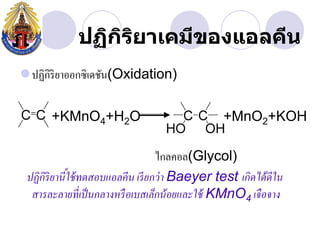
- 19. àžàžàžŽàžàžŁàžąàžČàčàžàžĄàž”àŸșàžàžàčàžàž„àžàž”àž àžŽ àžŽ ïŹàžàžČàžŁàčàžàžŽàžĄàžàč àžČ(Hydration) CH2=CH2 + H2O H2SO4 CH 3CH2OH OH CH3CH=CH2 + H2O H2SO4 CH3CHCH3 + CH3CH2CH2OH (àčàžàžŽàžàžàčàžàžą)
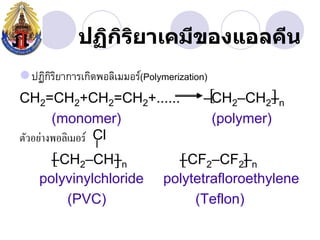
- 20. àžàžàžŽàžàžŁàžąàžČàčàžàžĄàž”àŸșàžàžàčàžàž„àžàž”àž àžŽ àžŽ ïŹàžàžàžŽàžàžŽàžŁàžŽàžąàžČàžàžàžàžàžŽàčàžàžàž±àž(Oxidation) +KMnO4+H2O +MnO2+KOH àčàžàž„àžàžàž„(Glycol) àžàžàžŽàžàžŽàžŁàžŽàžąàžČàžàž”àčàžàč àžàžàžȘàžàžàčàžàž„àžàž”àž àčàžŁàž” àžąàžàž§àč àžČ Baeyer test àčàžàžŽàžàčàžàč àžàž”àčàž àč àžȘàžČàžŁàž„àž°àž„àžČàžąàžàž”àčàčàžàč àžàžàž„àžČàžàž«àžŁàž· àžàčàžàžȘàčàž„àčàžàžàč àžàžąàčàž„àž°àčàžàč KMnO4 àčàžàž·àžàžàžČàž
- 21. àžàžàžŽàžàžŁàžąàžČàčàžàžĄàž”àŸșàžàžàčàžàž„àžàž”àž àžŽ àžŽ ïŹàžàžàžŽàžàžŁàžąàžČàžàžČàžŁàčàžàžŽàžàžàžàž„àžŽàčàžĄàžĄàžàžŁàč(Polymerization) àžŽàžŽ CH2=CH2+CH2=CH2+...... ï âCH2âCH2ânï (monomer) (polymer) àžàž±àž§àžàžąàčàžČàžàžàžàž„àžŽàčàžĄàžàžŁàč Cl ï âCH2âCHân ï âCF2âCF2ï n ï â polyvinylchloride polytetrafloroethylene (PVC) (Teflon)
- 22. àžȘàžČàžŁàžàžŁàž°àžàžàžàčàžàž„àčàžàžàč ïŹàčàžàž„àčàžàžàč(Alkynes) àžĄàž”àžȘàžčàžàžŁàžàž±àž§àčàž CnH2n-2 àč ïŹàžàž±àžàčàžàč àžàžȘàžČàžŁàžàžŁàž°àžàžàžàčàžźàčàž¶ÏžŁàžàžČàžŁàčàžàžàžàžàžŁàž°àčàž àžàčàžĄàčàžàžŽàčàžĄàžàž±àž§ (Unsaturated hydrocarbon) ïŹàžàž±àžàžàž°àžŁàž°àž«àž§àčàžČàžàžàžČàžŁàčàžàžàžàžàž°àžàžàžĄàčàžàčàžĄàčàž„àžàžžàž„àžĄàž”àžàžàžàž°àžȘàžČàžĄ( àž± ) àčàž„àž°àčàžàč àžàž«àžĄàžčàčàžàž±àžàžàčàžàžàžàčàžàž„àčàžàžàč ïŹàžĄàž”àžàč àžàčàžàžŁàžàžȘàžŁàčàžČàžàžàž”àčàčàžàč àžàčàžàčàčàžàžŽ àž(àčàžàčàžàžŁàžàčàž„àž°àčàžàčàžàžŽàčàž) àčàž„àž°àčàžàčàžàžŽàž àž± ïŹàčàžàžŁàžàžȘàžŁàčàžČàžàžàž”àčàčàžàč àžàčàžàčàžàžŽàžàčàžŁàž” àžąàžàž§àčàžČàčàžàčàžàž„àčàžàž„àčàžàžàč(Cycloalkyne)
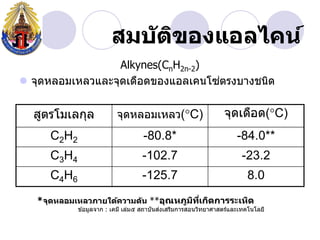
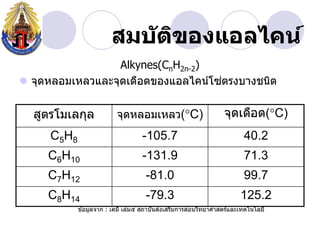
- 23. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àčàžàžàč Alkynes(CnH2n-2) àč ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž°àžàžžàžàčàžàž·àžàžàžàžàžàčàžàž„àčàžàžàčàžàžàžŁàžàžàžČàžàžàžàžŽàž àžȘàžčàžàžŁàčàžĄàčàž„àžàžžàž„ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§(ï°C) àžàžžàžàčàžàž·àžàž(ï°C) C2H2 -80.8* -84.0** C3H4 -102.7 -23.2 C4H6 -125.7 8.0 *àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àž àžČàžąàčàžàčàžàž§àžČàžĄàž àž±àž **àžàžžàžàž«àž àžčàžĄàžàčàžàžŽàžàžàžČàžŁàžŁàž°àčàž«àžŽàž àžŽ àž”àč àč àž àčàžàžĄàžčàž„àžàžČàž : àčàžàžĄàž” àčàž„àčàžĄàč àžȘàžàžČàžàž±àžàžȘàžàčàžȘàžŁàžŽàžĄàžàžČàžŁàžȘàžàžàž§àžŽàžàžąàžČàžšàžČàžȘàžàžŁàčàčàž„àž°àčàžàžàčàžàčàž„àžąàž”
- 24. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àčàžàžàč Alkynes(CnH2n-2) àč ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž°àžàžžàžàčàžàž·àžàžàžàžàžàčàžàž„àčàžàžàčàčàžàžàžŁàžàžàžČàžàžàžàžŽàž àžȘàžčàžàžŁàčàžĄàčàž„àžàžžàž„ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§(ï°C) àžàžžàžàčàžàž·àžàž(ï°C) C5H8 -105.7 40.2 C6H10 -131.9 71.3 C7H12 -81.0 99.7 C8H14 -79.3 125.2 àč àž àčàžàžĄàžčàž„àžàžČàž : àčàžàžĄàž” àčàž„àčàžĄàč àžȘàžàžČàžàž±àžàžȘàžàčàžȘàžŁàžŽàžĄàžàžČàžŁàžȘàžàžàž§àžŽàžàžąàžČàžšàžČàžȘàžàžŁàčàčàž„àž°àčàžàžàčàžàčàž„àžąàž”
- 25. àžȘàžĄàž àž±àžàžŽàžàžàžàčàžàž„àčàžàžàč Alkynes(CnH2n-2) ïŹ àčàžàž§àčàž àčàžĄàžàžžàžàž«àž„àžàžĄàčàž«àž„àž§àčàž„àž° àžàžžàžàčàžàž·àžàžàžȘàžčàžàžàž¶àžàžàžČàžĄàžàžČàžàž§àž àč àžàžČàžŁàčàžàžàžàžàž°àžàžàžĄàžàž”àčàžàžŽàžĄàžàž¶àž àč àč àč ïŹ àčàžàč àžàčàžĄàčàž„àžàžžàž„àčàžĄàčàžĄàžàž§ àčàžĄàč àž” àž±àč àž„àž°àž„àžČàžąàžàč àžČ ïŹ àžàž§àžČàžĄàž«àžàžČàčàžàčàžàž àčàžàžąàžàž§àčàžČàžàč àžČ
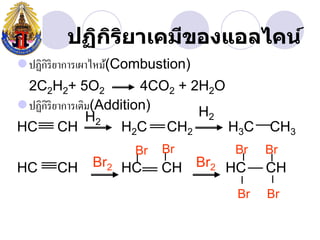
- 26. àžàžàžŽàžàžŁàžąàžČàčàžàžĄàž”àŸșàžàžàčàžàž„àčàžàžàč àžŽ àžŽ ïŹàžàžàžŽàžàžŽàžŁàžŽàžąàžČàžàžČàžŁàčàžàžČàčàž«àžĄàč(Combustion) 2C2H2+ 5O2 4CO2 + 2H2O ïŹàžàžàžŽàžàžŽàžŁàžŽàžąàžČàžàžČàžŁàčàžàžŽàžĄ(Addition) H2 H2 HC CH H2C CH2 H 3C CH3 Br Br Br Br HC CH Br2 HC CH Br2 HC CH Br Br
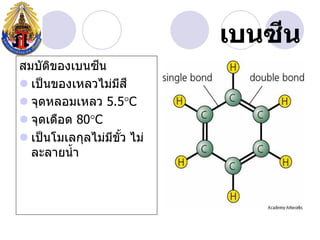
- 27. àž” àčàžàžàžàž àžȘàžĄàžàž±àžàžàžàžàčàžàžàžàž àžŽ àž” ïŹ àčàžàč àžàžàžàžàčàž«àž„àž§àčàžĄàčàžĄàžȘ àž” àž” ïŹ àžàžžàžàž«àž„àžàžĄàčàž«àž„àž§ 5.5ï°C ïŹ àžàžžàžàčàžàž·àžàž 80ï°C ïŹ àčàžàč àžàčàžĄàčàž„àžàžžàž„àčàžĄàčàžĄàžàž§ àčàžĄàč àž” àž±àč àž„àž°àž„àžČàžąàžàč àžČ
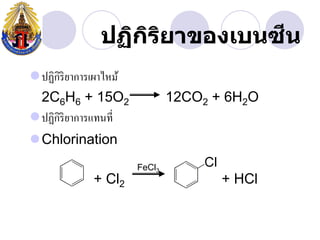
- 28. àž” àžàžàžŽàžàžŁàžąàžČàžàžàžàčàžàžàžàž àžŽ àžŽ ïŹàžàžàžŽàžàžŽàžŁàžŽàžąàžČàžàžČàžŁàčàžàžČàčàž«àžĄàč 2C6H6 + 15O2 12CO2 + 6H2O ïŹàžàžàžŽàžàžŽàžŁàžŽàžąàžČàžàžČàžŁàčàžàžàžàž”àč ïŹChlorination FeCl3 + Cl2 + HCl
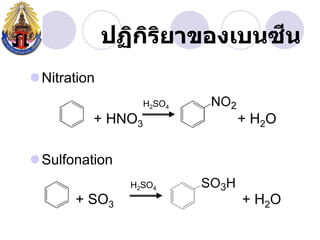
- 29. àž” àžàžàžŽàžàžŁàžąàžČàžàžàžàčàžàžàžàž àžŽ àžŽ ïŹNitration H2SO4 + HNO3 + H2 O ïŹSulfonation H2SO4 + SO3 + H2O
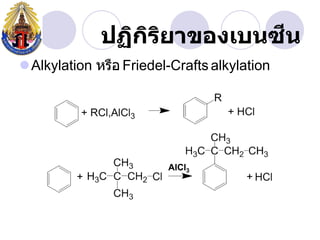
- 30. àž” àžàžàžŽàžàžŁàžąàžČàžàžàžàčàžàžàžàž àžŽ àžŽ ïŹAlkylation àž«àžŁàž·àž Friedel-Crafts alkylation AlCl3
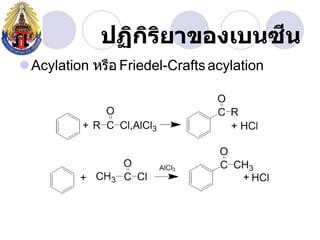
- 31. àž” àžàžàžŽàžàžŁàžąàžČàžàžàžàčàžàžàžàž àžŽ àžŽ ïŹAcylation àž«àžŁàž·àž Friedel-Crafts acylation