1 of 6
Downloaded 19 times





Recommended
Laporan praktikum hidrolisis garam kelas XI kimia



Laporan praktikum hidrolisis garam kelas XI kimiaEmirSyarif
Ėý
Berikut ini merupakan laporan atau makalah praktikum hidrolisis garam, yang bis aLaporan percobaan kimia elektrolisis



Laporan percobaan kimia elektrolisisWaQhyoe Arryee
Ėý
Laporan ini mendeskripsikan tiga percobaan elektrolisis menggunakan larutan Na2SO4, KI, dan CuSO4 dengan elektrode yang berbeda. Hasilnya menunjukkan terjadinya reaksi redoks di anoda dan katoda, dengan pelepasan gas hidrogen di katoda dan gas oksigen atau iodin di anoda.Soal2 laju reaksi kesetimbangan



Soal2 laju reaksi kesetimbanganDian Fery Irawan
Ėý
Dokumen tersebut membahas tentang laju reaksi dan kesetimbangan kimia. Terdapat beberapa soal dan jawaban mengenai konsep-konsep tersebut.Laporan Praktikum Kimia_Larutan Penyangga



Laporan Praktikum Kimia_Larutan PenyanggaFeren Jr
Ėý
Dokumen tersebut membahas tentang sifat larutan penyangga dan cara kerjanya dalam mempertahankan pH ketika ditambahkan asam, basa, atau pengencer. Larutan penyangga terdiri atas campuran asam/basa lemah dan garamnya. Ketika ditambahkan asam atau basa, akan terjadi reaksi netralisasi sehingga pH tetap. Larutan penyangga ujiannya adalah campuran asam asetat dan garamnya serta campuran amonia dan garPercobaan Elektrolisis



Percobaan Elektrolisisrinandani
Ėý
Elektrolisis larutan Na2SO4 dan KI. Terjadi reaksi redoks di katoda dan anoda. Pada katoda terbentuk H2 dan OH- melalui reduksi H2O. Pada anoda terbentuk O2, H+, dan I2 melalui oksidasi H2O dan I-. Hasilnya dibuktikan dengan indikator dan terbentuknya gelembung gas.Ester dan kegunaanya



Ester dan kegunaanyakimia12ipa1213
Ėý
Ester terbagi menjadi tiga golongan berdasarkan susunannya, yaitu sari buah-buahan, lemak atau minyak, dan lilin. Sari buah-buahan adalah ester dari alkohol suku rendah atau tengah, sedangkan lemak dan minyak adalah ester dari gliserol dan asam karboksilat suku tengah atau tinggi. Lilin adalah ester dari alkohol suku tinggi dan asam karboksilat suku tinggi.Praktikum Sel Volta



Praktikum Sel Voltaanggundiantriana
Ėý
Laporan ini membahas tentang praktikum sel volta yang meliputi tujuan, alat dan bahan, cara kerja, hasil pengamatan, analisis data, kesimpulan, dan saran. Praktikum ini bertujuan untuk mengetahui ciri-ciri sel volta dan menghitung beda potensial antara dua logam."Laporan Biologi Enzim Katalase



Laporan Biologi Enzim KatalaseHilya Auliya
Ėý
Laporan praktikum menguji aktivitas enzim katalase pada ekstrak hati ayam. Percobaan menunjukkan enzim katalase mampu menguraikan H2O2 menjadi air dan oksigen, namun aktivitasnya dipengaruhi suhu dan pH. Pemanasan atau penambahan asam/basa dapat merusak enzim dan menghambat aktivitasnya.Aldehid dan keton



Aldehid dan ketonHilya Fithri
Ėý
Dokumen tersebut memberikan informasi tentang aldehid dan keton. Aldehid dan keton merupakan senyawa yang mengandung gugus karbonil C=O dan digunakan sebagai bahan baku industri serta memiliki berbagai reaksi kimia. Aldehid lebih reaktif daripada keton karena memiliki atom hidrogen pada gugus karbonil.ALKIL HALIDA



ALKIL HALIDAJunando Gan Pandiangan
Ėý
Dokumen tersebut membahas tentang alkil halida dan reaksi substitusi nukleofiliknya. Terdapat pembahasan mengenai jenis-jenis alkil halida, mekanisme SN1 dan SN2, serta reaksi eliminasi E1 dan E2 pada alkil halida.Laporan Hasil Praktikum Menentukan Perubahan Entalpi Reaksi



Laporan Hasil Praktikum Menentukan Perubahan Entalpi ReaksiNadiya Rahmawati
Ėý
Laporan Hasil Praktikum Menentukan Perubahan Entalpi Reaksi | ÂĐ 2014 Nadiya RahmawatiSifat Golongan IA



Sifat Golongan IAElisabeth maranatha
Ėý
Logam alkali adalah unsur golongan satu yang membentuk basa kuat ketika bereaksi dengan air. Sifat fisiknya beraturan dari atas ke bawah periode, sementara sifat kimianya meliputi kecenderungan melepas elektron yang semakin besar dari atas ke bawah. Reaksinya dengan air, hidrogen, oksigen, dan halogen menghasilkan produk yang bersifat ionik dan larut dalam air.Laporan Praktikum Kimia - Titrasi Asam Basa



Laporan Praktikum Kimia - Titrasi Asam BasaMilantika Dyah Puspitasari
Ėý
Laporan Praktikum Kimia mengenai Titrasi Asam Basa
materi ajar kelas 11 IPA
Kelompok 3 - 11 IPA 2 - SMA Negeri 3 Kota Tangerang
TA: #2012/2013Kimia SMA XI IPA : Termokimia - Sistem dan lingkungan 



Kimia SMA XI IPA : Termokimia - Sistem dan lingkungan kevinengel
Ėý
1. Termokimia mempelajari perubahan kalor yang menyertai reaksi kimia dan proses fisika.
2. Hukum kekekalan energi dan hukum termodinamika pertama merupakan bahan kajian utama termokimia.
3. Sistem dan lingkungan merupakan dua hal penting dalam termokimia yang berkaitan dengan perpindahan energi.LAPORAN PRAKTIKUM TITRASI



LAPORAN PRAKTIKUM TITRASIMuhammad Daffa' Wiandaputra Haribowo
Ėý
Laporan praktikum kimia ini membahas tentang titrasi asam-basa untuk menentukan konsentrasi larutan cuka tak diketahui menggunakan larutan NaOH 0,1 M. Percobaan dilakukan dengan menitrasi larutan cuka dengan larutan NaOH sambil diindikasi dengan fenolftalein hingga terjadi perubahan warna, lalu rata-rata hasil titrasi digunakan untuk menghitung konsentrasi larutan cuka.Laporan praktikum fisika Hukum Hooke



Laporan praktikum fisika Hukum HookeYunan Malifah
Ėý
Laporan praktikum fisika mengenai hukum Hooke yang dilakukan oleh kelompok III SMA Negeri 1 Kota Bima pada tahun pelajaran 2014/2015. Praktikum ini bertujuan untuk menyelidiki hubungan antara gaya dengan pertambahan panjang pegas. Hasilnya menunjukkan bahwa gaya yang diberikan pada pegas berbanding lurus dengan pertambahan panjangnya, sehingga mendukung hukum Hooke.Identifikasi senyawa hidrokarbon



Identifikasi senyawa hidrokarbonputrisagut
Ėý
Senyawa organik awalnya didefinisikan sebagai senyawa yang mengandung karbon dan hidrogen karena diasumsikan terdapat dalam makhluk hidup. Namun definisi ini berubah setelah Friedrich Wohler berhasil mensintesis urea secara buatan. Senyawa organik dapat diidentifikasi melalui reaksi pemanasan, pengujian dengan air kapur, dan kertas kobalt. Hidrokarbon dapat dikelompokkan menjadi alifatik, siklik, tak jenuh,Larutan Penyangga dan Hidrolisis Garam



Larutan Penyangga dan Hidrolisis GaramThoyib Antarnusa
Ėý
šÝšÝßĢ mengenai Larutan Penyangga dan Hidrolisis.Laporan Kimia - hidrolisis



Laporan Kimia - hidrolisisDayana Florencia
Ėý
Dokumen tersebut membahas tentang sifat asam atau basa pada berbagai larutan garam. Terdapat empat jenis garam yang terbentuk dari kombinasi asam dan basa kuat atau lemah, yaitu garam netral, asam, basa, atau mengalami hidrolisis total. Dokumen ini melakukan percobaan untuk menentukan sifat pH larutan beberapa garam seperti Na2CO3, NaCl, NH4Cl, CH3COONa, dan Al2(SO4)More Related Content
What's hot (20)
Ester dan kegunaanya



Ester dan kegunaanyakimia12ipa1213
Ėý
Ester terbagi menjadi tiga golongan berdasarkan susunannya, yaitu sari buah-buahan, lemak atau minyak, dan lilin. Sari buah-buahan adalah ester dari alkohol suku rendah atau tengah, sedangkan lemak dan minyak adalah ester dari gliserol dan asam karboksilat suku tengah atau tinggi. Lilin adalah ester dari alkohol suku tinggi dan asam karboksilat suku tinggi.Praktikum Sel Volta



Praktikum Sel Voltaanggundiantriana
Ėý
Laporan ini membahas tentang praktikum sel volta yang meliputi tujuan, alat dan bahan, cara kerja, hasil pengamatan, analisis data, kesimpulan, dan saran. Praktikum ini bertujuan untuk mengetahui ciri-ciri sel volta dan menghitung beda potensial antara dua logam."Laporan Biologi Enzim Katalase



Laporan Biologi Enzim KatalaseHilya Auliya
Ėý
Laporan praktikum menguji aktivitas enzim katalase pada ekstrak hati ayam. Percobaan menunjukkan enzim katalase mampu menguraikan H2O2 menjadi air dan oksigen, namun aktivitasnya dipengaruhi suhu dan pH. Pemanasan atau penambahan asam/basa dapat merusak enzim dan menghambat aktivitasnya.Aldehid dan keton



Aldehid dan ketonHilya Fithri
Ėý
Dokumen tersebut memberikan informasi tentang aldehid dan keton. Aldehid dan keton merupakan senyawa yang mengandung gugus karbonil C=O dan digunakan sebagai bahan baku industri serta memiliki berbagai reaksi kimia. Aldehid lebih reaktif daripada keton karena memiliki atom hidrogen pada gugus karbonil.ALKIL HALIDA



ALKIL HALIDAJunando Gan Pandiangan
Ėý
Dokumen tersebut membahas tentang alkil halida dan reaksi substitusi nukleofiliknya. Terdapat pembahasan mengenai jenis-jenis alkil halida, mekanisme SN1 dan SN2, serta reaksi eliminasi E1 dan E2 pada alkil halida.Laporan Hasil Praktikum Menentukan Perubahan Entalpi Reaksi



Laporan Hasil Praktikum Menentukan Perubahan Entalpi ReaksiNadiya Rahmawati
Ėý
Laporan Hasil Praktikum Menentukan Perubahan Entalpi Reaksi | ÂĐ 2014 Nadiya RahmawatiSifat Golongan IA



Sifat Golongan IAElisabeth maranatha
Ėý
Logam alkali adalah unsur golongan satu yang membentuk basa kuat ketika bereaksi dengan air. Sifat fisiknya beraturan dari atas ke bawah periode, sementara sifat kimianya meliputi kecenderungan melepas elektron yang semakin besar dari atas ke bawah. Reaksinya dengan air, hidrogen, oksigen, dan halogen menghasilkan produk yang bersifat ionik dan larut dalam air.Laporan Praktikum Kimia - Titrasi Asam Basa



Laporan Praktikum Kimia - Titrasi Asam BasaMilantika Dyah Puspitasari
Ėý
Laporan Praktikum Kimia mengenai Titrasi Asam Basa
materi ajar kelas 11 IPA
Kelompok 3 - 11 IPA 2 - SMA Negeri 3 Kota Tangerang
TA: #2012/2013Kimia SMA XI IPA : Termokimia - Sistem dan lingkungan 



Kimia SMA XI IPA : Termokimia - Sistem dan lingkungan kevinengel
Ėý
1. Termokimia mempelajari perubahan kalor yang menyertai reaksi kimia dan proses fisika.
2. Hukum kekekalan energi dan hukum termodinamika pertama merupakan bahan kajian utama termokimia.
3. Sistem dan lingkungan merupakan dua hal penting dalam termokimia yang berkaitan dengan perpindahan energi.LAPORAN PRAKTIKUM TITRASI



LAPORAN PRAKTIKUM TITRASIMuhammad Daffa' Wiandaputra Haribowo
Ėý
Laporan praktikum kimia ini membahas tentang titrasi asam-basa untuk menentukan konsentrasi larutan cuka tak diketahui menggunakan larutan NaOH 0,1 M. Percobaan dilakukan dengan menitrasi larutan cuka dengan larutan NaOH sambil diindikasi dengan fenolftalein hingga terjadi perubahan warna, lalu rata-rata hasil titrasi digunakan untuk menghitung konsentrasi larutan cuka.Laporan praktikum fisika Hukum Hooke



Laporan praktikum fisika Hukum HookeYunan Malifah
Ėý
Laporan praktikum fisika mengenai hukum Hooke yang dilakukan oleh kelompok III SMA Negeri 1 Kota Bima pada tahun pelajaran 2014/2015. Praktikum ini bertujuan untuk menyelidiki hubungan antara gaya dengan pertambahan panjang pegas. Hasilnya menunjukkan bahwa gaya yang diberikan pada pegas berbanding lurus dengan pertambahan panjangnya, sehingga mendukung hukum Hooke.Identifikasi senyawa hidrokarbon



Identifikasi senyawa hidrokarbonputrisagut
Ėý
Senyawa organik awalnya didefinisikan sebagai senyawa yang mengandung karbon dan hidrogen karena diasumsikan terdapat dalam makhluk hidup. Namun definisi ini berubah setelah Friedrich Wohler berhasil mensintesis urea secara buatan. Senyawa organik dapat diidentifikasi melalui reaksi pemanasan, pengujian dengan air kapur, dan kertas kobalt. Hidrokarbon dapat dikelompokkan menjadi alifatik, siklik, tak jenuh,Larutan Penyangga dan Hidrolisis Garam



Larutan Penyangga dan Hidrolisis GaramThoyib Antarnusa
Ėý
šÝšÝßĢ mengenai Larutan Penyangga dan Hidrolisis.Viewers also liked (11)
Laporan Kimia - hidrolisis



Laporan Kimia - hidrolisisDayana Florencia
Ėý
Dokumen tersebut membahas tentang sifat asam atau basa pada berbagai larutan garam. Terdapat empat jenis garam yang terbentuk dari kombinasi asam dan basa kuat atau lemah, yaitu garam netral, asam, basa, atau mengalami hidrolisis total. Dokumen ini melakukan percobaan untuk menentukan sifat pH larutan beberapa garam seperti Na2CO3, NaCl, NH4Cl, CH3COONa, dan Al2(SO4)Bab.3 asam,basa dan garam



Bab.3 asam,basa dan garam" Sigit School" Kutowinangun,Kebumen Jawa Tengah
Ėý
Dokumen tersebut membahas tentang asam, basa, dan garam. Asam dapat melepaskan ion hidrogen (H+) dalam air, basa dapat melepaskan ion hidroksida (OH-), dan garam terbentuk dari reaksi asam dan basa. Dokumen tersebut juga menjelaskan cara mengidentifikasi larutan asam dan basa menggunakan kertas lakmus dan indikator alami seperti bunga mawar merah, serta menjelaskan skala pH untuk mengGangguan Asam Basa



Gangguan Asam Basamcrohman
Ėý
This document summarizes a case study of a child with metabolic acidosis following sepsis and 20% body surface area burns. It applies the Fencl-Stewart approach to analyze the acid-base disturbance. This involves measuring the standard base excess, sodium-chloride effect, albumin effect, and calculating the unmeasured ion effect. In this case, the unmeasured ion effect of -21.5 mEq/L suggests lactic acidosis as the cause. Bicarbonate therapy is not recommended due to risks of worsening tissue hypoxia and intracellular acidosis. The appropriate treatment is to correct hypoalbuminemia, hypernatremia, and the underlying cause of lactic acidosis through improving oxygen delivery andLaporan Praktikum Kimia Hidrolisis



Laporan Praktikum Kimia Hidrolisisvina irodatul afiyah
Ėý
Mengetahui sifat-sifat larutan garam yang terhidrolisis
yang terdiri dari dasar teori yang interaktif mudah dipahami, alar, bahan dan langkah kerja. hasil pengamatan berupa Identifikasi sifat, reaksi, serta pengukuran pH larutan.
pembahasan umum dan khusus Koloid liofil dan liofob kelompok 6. 11 ipa 2



Koloid liofil dan liofob kelompok 6. 11 ipa 2sarah fauzia
Ėý
Koloid liofil dan liofob memiliki perbedaan dalam sifat daya tarik antara partikel terdispersi dan medium pendispersinya. Koloid liofil memiliki daya tarik yang kuat sehingga lebih stabil, sedangkan koloid liofob memiliki daya tarik yang lemah sehingga kurang stabil.Soal2 p h larutan



Soal2 p h larutanDian Fery Irawan
Ėý
Dokumen tersebut berisi soal-soal tentang pH dan larutan penyangga. Beberapa soal membahas tentang penentuan pH dari larutan asam, basa, dan garam tertentu berdasarkan konsentrasi dan tetapan ionisasi atau hasil kali kelarutan. Soal lain membahas tentang reaksi antara asam dan basa untuk membentuk larutan penyangga dan menentukan jumlah zat yang dibutuhkan.Similar to hidrolisis Garam (20)
Materi ajar hidrolisis garam sri handayani siregar



Materi ajar hidrolisis garam sri handayani siregarSiregar Sri Handayani
Ėý
[dokumen]
1. Membahas konsep hidrolisis garam dan jenis-jenis garam berdasarkan asam dan basanya.
2. Menghitung pH larutan garam yang mengalami hidrolisis secara parsial dan total.
3. Memberikan contoh aplikasi konsep hidrolisis dalam kehidupan sehari-hari seperti pelarutan sabun dan penjernihan air.PPT_hidrolisis.ppt



PPT_hidrolisis.pptAgniaNurJihaddiniIma1
Ėý
Dokumen tersebut membahas tentang hidrolisis garam, yaitu penguraian garam oleh air yang menghasilkan asam dan basanya kembali. Terdapat dua jenis hidrolisis, yaitu parsial dan total. Jenis garam yang mengalami hidrolisis dipengaruhi oleh sifat asam dan basa pembentuknya, seperti garam dari asam kuat dan basa lemah hanya mengalami hidrolisis parsial.laporan Asam Basa



laporan Asam BasaPutri Yusril
Ėý
Dokumen tersebut merangkum percobaan untuk menguji sifat asam dan basa dari beberapa senyawa dengan menggunakan indikator lakmus dan indikator alami seperti kunyit dan mahkota bunga. Percobaan menunjukkan perubahan warna indikator untuk menentukan sifat asam atau basa dari senyawa yang diuji.Laporan praktikum - pembuatan asam benzoat



Laporan praktikum - pembuatan asam benzoatFirda Shabrina
Ėý
Laporan praktikum kimia ini memberikan ringkasan singkat tentang sintesis asam benzoat dari oksidasi toluena menggunakan KMnO4. Prosesnya melibatkan reaksi oksidasi toluena menjadi aldehida lalu asam benzoat dalam kondisi basa. Hasil akhir adalah kristal asam benzoat berbentuk panjang tajam berwarna putih seberat 0,171 gram.Laporan praktikum kimia asam basa



Laporan praktikum kimia asam basaQueena N.A.S
Ėý
Laporan ini membahas praktikum pH asam-basa yang meliputi tujuan, alat dan bahan, dasar teori, cara kerja, dan hasil pengamatan. Tujuannya adalah menentukan pH larutan dengan indikator dan menemukan rumus asam kuat, basa kuat, asam lemah, dan basa lemah berdasarkan pengukuran pH. Hasilnya menunjukkan perbedaan pH antara asam dan basa kuat versus lemah serta pengaruh pengenceran terhadap perubLaporan tetap sifat asam dan basa senyawa organik



Laporan tetap sifat asam dan basa senyawa organikMitha Pratiwi
Ėý
Dokumen tersebut membahas tentang sifat asam dan basa senyawa organik melalui serangkaian percobaan. Percobaan pertama menguji pH senyawa untuk mengetahui sifat asam atau basanya, sedangkan percobaan kedua menguji kelarutan senyawa dalam minyak sayur. Hasilnya menunjukkan perbedaan pH dan kelarutan antara senyawa organik.Hidrolisis garam kim2 revisi



Hidrolisis garam kim2 revisiUniversity OxFord
Ėý
Dokumen tersebut membahas tentang konsep hidrolisis garam, jenis-jenis hidrolisis garam yang dapat terjadi, dan tujuan pembelajaran mengenai hidrolisis garam. Tujuan pembelajaran antara lain menjelaskan ciri-ciri garam yang dapat terhidrolisis, menentukan sifat larutan garam terhidrolisis, dan menuliskan reaksi hidrolisis berbagai jenis garam. pH Hidrolisis garam 



pH Hidrolisis garam Irmi Mimiqi
Ėý
Dokumen tersebut membahas tentang hidrolisis garam dan penentuan pH larutan garam. Secara umum dijelaskan bahwa sifat asam atau basa suatu larutan garam ditentukan oleh jenis asam dan basa pembentuk garam tersebut, dan pH dapat dihitung berdasarkan konstanta kesetimbangan asam dan basa.Hidrolisis garam kelas XI



Hidrolisis garam kelas XIIrmi Mimiqi
Ėý
Dokumen tersebut membahas tentang konsep hidrolisis garam dan bagaimana sifat asam atau basa suatu larutan garam ditentukan oleh kekuatan relatif asam dan basa yang membentuk garam tersebut. Garam yang terbentuk dari asam dan basa kuat bersifat netral, sedangkan garam yang terbentuk dari asam lemah dan basa kuat bersifat basa, atau sebaliknya.Hidrolisis garam kelas XI



Hidrolisis garam kelas XIIrmi Mimiqi
Ėý
Dokumen tersebut membahas tentang konsep hidrolisis garam dan bagaimana sifat asam atau basa suatu larutan garam ditentukan oleh kekuatan relatif asam dan basa yang membentuk garam tersebut. Garam yang terbentuk dari asam dan basa kuat bersifat netral, sedangkan garam yang terbentuk dari asam lemah dan basa kuat bersifat basa, atau sebaliknya.5. bahan ajar )



5. bahan ajar )Irmi Mimiqi
Ėý
Dokumen tersebut membahas tentang konsep hidrolisis garam dan bagaimana sifat asam atau basa suatu larutan garam ditentukan oleh kekuatan relatif asam dan basa yang membentuk garam tersebut. Garam yang terbentuk dari asam dan basa kuat bersifat netral, sedangkan garam yang terbentuk dari asam lemah dan basa kuat bersifat basa, atau sebaliknya.Hidrolisis garam kelas XI



Hidrolisis garam kelas XInadripratama
Ėý
Dokumen ini adalah dokumen untuk mempelajari hidrolisis garamAsam Basa



Asam BasaRino Safrizal
Ėý
Dokumen tersebut membahas tentang teori-teori asam basa menurut Arrhenius, Brownsted-Lowry, dan Lewis. Juga dibahas tentang karakteristik asam dan basa, kekuatan asam dan basa, serta konsep pH pada larutan elektrolit.Laporan Percobaan Reaksi Asam Basa (Asam Poliprotik)



Laporan Percobaan Reaksi Asam Basa (Asam Poliprotik)Ahmad Dzikrullah
Ėý
Laporan praktikum kimia dasar II ini membahas reaksi asam basa pada asam poliprotik. Percobaan dilakukan untuk mengenal ion karbonat dan bikarbonat dalam larutan serta menentukan kadarnya. Metode yang digunakan adalah titrasi asidimetri dengan indikator fenolftalein dan metil orange.Materi asam dan_basa_power_point_ppt



Materi asam dan_basa_power_point_pptolanascorepta
Ėý
Dokumen tersebut membahas tentang asam dan basa, termasuk definisi, sifat, teori, pH, dan reaksi asam-basa. Dijelaskan bahwa asam akan menghasilkan ion H+ sedangkan basa akan menghasilkan ion OH- dalam air. Juga dibahas mengenai kekuatan asam dan basa, serta pengaruhnya terhadap pH larutan.More from Putri Yusril (11)
laporan Titrasi Asam Basa 



laporan Titrasi Asam Basa Putri Yusril
Ėý
Laporan ini menjelaskan eksperimen titrasi asam basa untuk menentukan konsentrasi HCl dengan NaOH 0,1 M. Metode titrasi melibatkan penambahan NaOH secara bertahap hingga indikator berubah warna, menunjukkan titik ekuivalen telah tercapai. Rata-rata volume NaOH yang dibutuhkan kemudian digunakan untuk menghitung konsentrasi HCl.laporan memperkirakan PH suatu larutan



laporan memperkirakan PH suatu larutanPutri Yusril
Ėý
Dokumen tersebut merangkum percobaan menentukan pH larutan dengan menggunakan beberapa indikator asam basa seperti lakmus, fenolftalein, metil merah, metil orange dan bromtimol biru. Percobaan dilakukan terhadap beberapa larutan seperti air, larutan A dan B, urine, air jeruk nipis dan air kran, yang menghasilkan perbedaan warna indikator dan perkiraan pH berkisar antara 3-14.pengaruh katalisator terhadap laju reaksi



pengaruh katalisator terhadap laju reaksiPutri Yusril
Ėý
Dokumen tersebut membahas percobaan untuk mengetahui pengaruh katalisator terhadap laju reaksi dekomposisi H2O2. Larutan H2O2 ditambahkan FeCl3 menghasilkan gelembung gas paling banyak karena FeCl3 berperan sebagai katalisator dengan mempercepat laju reaksi. Katalisator bekerja dengan menurunkan energi aktivasi sehingga reaksi dapat berlangsung lebih cepat.Perubahan entalpi reaksi



Perubahan entalpi reaksiPutri Yusril
Ėý
Eksperimen mengukur perubahan entalpi reaksi antara larutan natrium hidroksida dan asam klorida menggunakan kalorimeter. Larutan NaOH dan HCl dicampur, menyebabkan suhu meningkat 4°C. Perhitungan menunjukkan energi yang dipindahkan ke lingkungan adalah 0,84 kJ. Jumlah mol pereaksi sama, yaitu 0,025 mol.Laporan Biologi Difusi dan Osmosis Putri Yusril



Laporan Biologi Difusi dan Osmosis Putri YusrilPutri Yusril
Ėý
Laporan biologi Difusi pada larutan dan osmosis pada kentang dan wortelNo titl1



No titl1Putri Yusril
Ėý
Dokumen ini menceritakan tentang perasaan cinta seseorang yang tidak pernah terbalas. Orang tersebut selalu setia menanti dan berusaha membuat orang yang dicintainya mengerti perasaannya, namun terlalu sulit karena perasaannya tidak pernah dipahami. Akhirnya orang tersebut hanya berharap suatu hari nanti perasaan cintanya dapat dipahami.Recently uploaded (20)
04. Integral Bidang Kompleks (Universitas Pakuan).pdf



04. Integral Bidang Kompleks (Universitas Pakuan).pdfAsepSaepulrohman4
Ėý
Lintasan dalam integral kompleks menentukan jalur pengintegralan di bidang kompleks.
Jenis lintasan meliputi garis lurus, lingkaran, dan kontur tertutup.
Integral kontur tertutup penting dalam Teorema Cauchy dan Teorema ResidÞ.
Hasil integral bisa bergantung pada lintasan, terutama jika terdapat singularitas di dalamnya.Pancasila Simbol Harmonisasi Antar Umat Bergama Di Indonesia - Ulya



Pancasila Simbol Harmonisasi Antar Umat Bergama Di Indonesia - UlyaMAJELIS REMBUG SINAU (MARS) PANCASILA
Ėý
https://marspancasila.blogspot.comIndependent Study Pendidikan Karakter ASWAJA.pdf



Independent Study Pendidikan Karakter ASWAJA.pdfSyarifatul Marwiyah
Ėý
Independent Study Pendidikan Karakter ASWAJA Pascasarjana UAS Kencong JemberPresentasi Rumus-Rumus Bangun Ruang Bola



Presentasi Rumus-Rumus Bangun Ruang BolaIluDeviSania
Ėý
Bola adalah objek geometri dimensi yang serupa dengan objek melingkar dua dimensi, yaitu "lingkaran" adalah batas dari "cakram". Pada umumnya, bola didefinisikan sebagai himpunan titik yang memiliki jarak sama dari pusat
bola ke permukaan bola.04__Distribusi_Probabilitas_Diskrit (Unpak).pdf



04__Distribusi_Probabilitas_Diskrit (Unpak).pdfAsepSaepulrohman4
Ėý
Distribusi probabilitas diskrit menggambarkan variabel acak yang hanya dapat mengambil nilai tertentu, biasanya bilangan bulat, dengan setiap nilai memiliki probabilitas yang terukur. Fungsi distribusi probabilitas (Probability Mass Function, PMF) memberikan probabilitas bahwa variabel acak
ð
X sama dengan nilai tertentu
ðĨ
x, dan memenuhi syarat bahwa jumlah seluruh probabilitas adalah satu. Contoh umum dari distribusi probabilitas diskrit termasuk distribusi binomial, yang menggambarkan jumlah sukses dalam
ð
n percobaan independen; distribusi Poisson, yang menggambarkan jumlah kejadian dalam interval waktu atau ruang tertentu; dan distribusi geometrik, yang menggambarkan jumlah percobaan hingga sukses pertama. Karakteristik penting dari distribusi ini meliputi rata-rata (mean) dan varians, yang masing-masing dapat dihitung menggunakan rumus tertentu. Distribusi probabilitas diskrit memiliki aplikasi luas dalam berbagai bidang, termasuk statistik, ilmu komputer, ekonomi, dan rekayasa, sehingga menjadi alat penting untuk analisis data yang bersifat diskrit.
Kamus Bahasa Indonesia di Lingkungan PGSD .pdf



Kamus Bahasa Indonesia di Lingkungan PGSD .pdfUniversitas Negeri Medan
Ėý
Kamus bahasa Indonesia di Lingkungan PGSD berisi istilah - istilah yang ada atau sering digunakan di lingkungan PGSD ( Pendidikan Guru Sekolah Dasar) dan arti dari istilah - istilah tersebut.Modul 1 - Mengenal Kejahatan Siber pada Anak.pdf



Modul 1 - Mengenal Kejahatan Siber pada Anak.pdfYayasan Pusat Kajian dan Perlindungan Anak
Ėý
Bagaimana mengidentifikasi Kejahatan yang terjadi pada Anak
Ayo Belajar Bersama !!!Model Ian Barbour Dialektika Ilmu dan Agama



Model Ian Barbour Dialektika Ilmu dan AgamaIslamic Studies
Ėý
Bagi Barbour, dialektika ilmu dan agama bukanlah sebuah pertarungan untuk menentukan mana yang lebih benar, melainkan sebuah proses kolaboratif yang dapat memperkaya pemahaman kita terhadap dunia. Bagi banyak orang, pemikiran Barbour membuka kemungkinan bahwa sains dan agama dapat berkembang bersama, dengan keduanya saling memberi wawasan yang lebih dalam tentang realitas yang kita hadapi.
Dengan demikian, model dialektika yang dikembangkan oleh Ian Barbour menawarkan sebuah jalan tengah yang mendalam antara dua dunia yang tampaknya berbeda, namun pada kenyataannya dapat saling melengkapi, membawa pencerahan bagi umat manusia."Penemuan Kembali Revolusi Kita" - Soekarnp



"Penemuan Kembali Revolusi Kita" - SoekarnpMAJELIS REMBUG SINAU (MARS) PANCASILA
Ėý
https://marspancasila.blogspot.comRencana PEMAPARAN Materi Pelatihan_TNA-Negotiating Skill for Procurement.pdf



Rencana PEMAPARAN Materi Pelatihan_TNA-Negotiating Skill for Procurement.pdfKanaidi ken
Ėý
Narasumber/ Pemateri Training: Kanaidi, SE., M.Si., cSAP., CBCM
HP/Wa Kanaidi: 0812 2353 284,
e-mail : kanaidi63@gmail.com
----------------------------------------
bagi Para Karyawan *PT. VIVERE Group (Jakarta)*
yg diselenggarakan *secara Online Meeting* (tgl 18 Maret 2025).Independent Study pengembangan Kurikulum & Model pembelajaran PAI (1).pdf



Independent Study pengembangan Kurikulum & Model pembelajaran PAI (1).pdfSyarifatul Marwiyah
Ėý
Independent Study pengembangan Kurikulum & Model pembelajaran PAI Pascasarjana UAS Kencong JemberModul Ajar Pendidikan Pancasila Kelas 2 Fase A Kurikulum Merdeka



Modul Ajar Pendidikan Pancasila Kelas 2 Fase A Kurikulum MerdekaModul Kelas
Ėý
Modul Ajar Pendidikan Pancasila Kelas 2 Fase A Kurikulum Merdeka [MODULKELAS.COM]"MUHAMMAD HUSNI THAMRIN" - Anhar Gonggong.pdf



"MUHAMMAD HUSNI THAMRIN" - Anhar Gonggong.pdfMAJELIS REMBUG SINAU (MARS) PANCASILA
Ėý
https://marspancasila.blogspot.comPancasila Simbol Harmonisasi Antar Umat Bergama Di Indonesia - Ulya



Pancasila Simbol Harmonisasi Antar Umat Bergama Di Indonesia - UlyaMAJELIS REMBUG SINAU (MARS) PANCASILA
Ėý
hidrolisis Garam
- 1. K I M I A Disusun oleh : Putri Yusril B Kelas : XI IPA 4 SMA NEGERI 1 MAKALE
- 3. KATA PENGANTAR Puji dan syukur kehadirat Tuhan yang Maha Esa, karena atas berkat dan rahmat- Nya penulis dapat menyelesaikan âLaporan Akhir Praktikum Kimiaâ dengan sebaik-baiknya dan tepat waktu. Adapun tujuan dari penulisan laporan ini adalah sebagai bukti hasil dari percobaan- percobaan yang telah dilakukan saat praktikum dan untuk melengkapi tugas dari praktikum kimia. Penulis juga berterima kasih kepada pihak-pihak yang telah membantu dalam proses penyelesaian laporan ini. Penulis menyadari bahwa dalam upaya penyelasaian tugas laporan ini, banyak megalami berbagai kesulitan sehingga tidaklah mengherankan apabila dalam laporan ini masih banyak ditemukan kesalahan-kesalahan di sana sini. Oleh karena itu, kami sebagai penulis banyak mengalami kendala dan kesulitan.Kami menyadari bahwa laporan ini jauh dari kesempurnaan oleh sebab kritik dan saran dari berbagai pihak yang sifatnya membangun, sangat kami harapkan.Semoga laporan ini bermanfaat adanya. Makale, 23 Mei 2013 Penulis, Putri Yusril
- 4. HIDROLISIS GARAM Tujuan Untuk mengetahui sifat larutan garam yang terhidrolisis LANDASAN TEORI Hidrolisis merupakan istilah untuk beraksinya suatu zat dengan air. Pada bagian ini, akan dibahas hidrolisis larutan garam. Larutan garam ada yang bersifat netral, asam ataupun basa.Sifat asam-basa suatu garam bergantung pada kekuatan relatif asam dan basa penyusunnya.Garam yang berasal dari asam kuat dan basa kuat dalam air tidak mengalami hidrolisis dan larutannya bersifat netral, contoh garam jenis ini adalah NaCl, KCl, dan Na2SO4. Dalam air, ion-ion garam tersebut tidak bereaksi satu sama lain. Contoh reaksi ionisasinya: NaCl â Na+ + Cl- H2O â H+ + OH- Larutan tersebut bersifat netral karena konsentrasi ion H+ dan OH- sama. Garam yang berasal dari asam lemah dan basa kuat dalam larutan akan bersifat basa karena mengalami hidrolisis sebagian. Contoh garam ini adalah CH3COONa dan KCN. Dalam air, ion negatif dari garam akan bereaksi dengan ion H+ membentuk asam lemah sehingga kesetimbangan terganggu. Contoh reaksi ionisasinya: KCN â K+ + CN- CN + H2O â HCN + OH Ion H+ bereaksi dengan ion CN- membentuk HCN, sedangkan K+ tidak bereaksi dengan OH- sebeb KOH basa kuat. Karena terjadi kelebihan ion OH- , menjadikan larutan tersebut bersifat basa. Garam yang berasal dari asam kuat dan basa lemah dalam air akan bersifat asam karena mengalami hidrolisis sebagian, contohnya adalah NH4Cl. Dalam air, NH4Cl akan terionisasi dan ion NH4 + yang dihasilkan akan bereaksi dengan air, sedangkan ion Cl- tidak akan bereaksi dengan air sebab berasal dari asam kuat. Reaksi ionisasinya adalah: NH4Cl â NH4 + + Cl- NH4 + + H2O â NH4OH + H+ Kelebihan ion H+ dalam larutan NH4Cl menyebabkan larutan bersifat asam. Garam-garam yang berasal dari asam lemah dan basa lemah, misalnya NH4CN di dalam air akan mengalami hidrolisis total. Reaksi yang terjadi adalah: NH4CN â NH4 + + CN- NH4 + + H2O â NH4OH + H+ CN + H2O â HCN + OH-
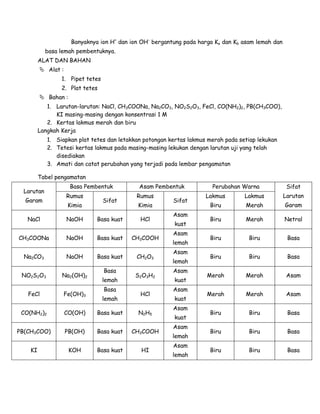
- 5. Banyaknya ion H+ dan ion OH- bergantung pada harga Ka dan Kb asam lemah dan basa lemah pembentuknya. ALAT DAN BAHAN ï Alat : 1. Pipet tetes 2. Plat tetes ï Bahan : 1. Larutan-larutan: NaCl, CH3COONa, Na2CO3, NO2S2O3, FeCl, CO(NH2)2, PB(CH3COO), KI masing-masing dengan konsentrasi 1 M 2. Kertas lakmus merah dan biru Langkah Kerja 1. Siapkan plat tetes dan letakkan potongan kertas lakmus merah pada setiap lekukan 2. Tetesi kertas lakmus pada masing-masing lekukan dengan larutan uji yang telah disediakan 3. Amati dan catat perubahan yang terjadi pada lembar pengamatan Tabel pengamatan Larutan Garam Basa Pembentuk Asam Pembentuk Perubahan Warna Sifat Larutan Garam Rumus Kimia Sifat Rumus Kimia Sifat Lakmus Biru Lakmus Merah NaCl NaOH Basa kuat HCl Asam kust Biru Merah Netral CH3COONa NaOH Basa kuat CH3COOH Asam lemah Biru Biru Basa Na2CO3 NaOH Basa kuat CH2O3 Asam lemah Biru Biru Basa NO2S2O3 Na2(OH)2 Basa lemah S2O3H2 Asam kuat Merah Merah Asam FeCl Fe(OH)3 Basa lemah HCl Asam kuat Merah Merah Asam CO(NH2)2 CO(OH) Basa kuat N2H5 Asam kuat Biru Biru Basa PB(CH3COO) PB(OH) Basa kuat CH3COOH Asam lemah Biru Biru Basa KI KOH Basa kuat HI Asam lemah Biru Biru Basa
- 6. KESIMPULAN Berdasarkan hasil eksperimen yang telah dilakukan larutan yang terhidrolisis adalah CH3COONa, Na2CO3, NO2S2O3, FeCl, CO(NH2)2, PB(CH3COO), KI karena bersifat asam dan basa. Sedangkan larutan yang tidak terhidrolisis adalah latutan NaCl karena bersifat netral. Garam yang terbentuk dari asam lemah dan basa kuat maka garam yang terbentuk bersifat basa.Garam yang terbentuk dari asam kuat dan basa lemah maka garam yang terbentuk bersifat asam.Garam yang terbentuk dari asam lemah dan basa lemah maka garam yang terbentuk bersifat asam atau basa tergantung pada besar atau lebihnya nilai Kb atau Ka. Hubungan antara asam dan basa pembentuk garam dengan sifat larutan garam dalam air adalah sebagai berikut : Contoh : Asam HCl + NaOH basa akan membentuk ion H+ , Cl- , Na+ , dan OH- . Jadi, jika dicampur akan terbentuk NaCl (garam) + H2O (air) Jika asam ditambahkan dengan basa akan menghasilkan garam dan air. Asam jika dilarutkan dalam air menghasilkan ion sama juga dengan basa.
































