Laju reaksi. ok ppt
- 2. Standar kompetensi Memahami kinetika dan kesetimbangan reaksi kimia serta faktor-faktor yang mempengaruhinya
- 3. Kompetensi Dasar Mendeskripsikan pengertian laju reaksi dengan melakukan percobaan tentang faktor- faktor yang mempengaruhi laju reaksi
- 4. indikator Menghitung konsenrasi larutan (molaritas larutan) Menganalisis faktor-faktor yg mempengaruhi laju reaksi (konsentrasi, luas permukaan, suhu,dan katalis)melalui percobaan. Menafsirkan grafik dari data percobaan tentang factor ŌĆōfaktor yg mempengaruhi laju reaksi
- 5. Molaritas/Konsentrasi (M) Molaritas menyatakan jumlah mol zat yang terlarut dalam satu liter larutan M = mol / liter M = gr X 1000 mr ml
- 6. Latihan Soal 1.Tentukan molaritas 0,2 mol HCl dalam 1 liter larutan! 2.Tentukan molaritas larutan yang dibuat dari 2 gram NaOH yang dilarutkan ke dalam air sampai volumenya menjadi 500 mL!
- 7. Pengenceran mol sebelum pengenceran = mol setelah pengenceran M1 x V1 = M2 x V2 Molaritas Campuran M = M1 x V1 + M2 x V2 + ŌĆ”. V1 + V2 + ŌĆ”.
- 8. Kadar Zat Mpekat = Žü x 10 x %massa Mr Latihan soal Tentukan molaritas dari asam sulfat pekat yang mengandung 96% H2SO4 dan massa jenis 1,8 kg LŌĆō1! (diketahui Ar H = 1, S = 32, dan O = 16)
- 9. Laju Reaksi Cepat Lambatnya reaksi berlangsung Perubahan Konsetrasi pereaksi atau hasil reaksi dalam satuan waktu. A + B ŌåÆ C V = ╬ö[Reaktan] V= ╬ö[Produk] ╬öt ╬öt VA =- ╬ö[A] VB =-╬ö[B] VC =+╬ö[C] ╬öt ╬öt ╬öt
- 10. Grafik Laju Reaksi [ P ] [ R ] [ P ] = konsentrasi produk [ R ] = konsentrasi reaktan
- 11. Contoh Soal Berdasarkan reaksi: 2 N2O5(g) ŌåÆ 4 NO2(g) + O2(g) diketahui bahwa N2O5 berkurang dari 2 mol/liter menjadi 0,5 mol/liter dalam waktu 10 detik. Berapakah laju reaksi berkurangnya N2O5?
- 12. Pembahasan VN2O5 = - ╬ö[N2O5] ╬öt = [2 ŌĆō 0,5] 10 = 0,15 M/detik
- 13. Latihan Soal 1.Ke dalam ruang yang volumenya 2 liter, dimasukkan 4 mol gas HI yang kemudian terurai menjadi gas H2 dan I2. Setelah 5 detik, dalam ruang tersebut terdapat 1 mol gas H2. Tentukan laju reaksi pembentukan gas H2 dan laju reaksi peruraian gas HI! 2.Diketahui reaksi 2 NO(g)+ O2(g)ŌåÆ N2O4(g). Bila mula-mula 2 mol NO bereaksi dengan 2 mol oksigen dalam ruang 2 liter selama 10 detik, tentukan besarnya laju reaksi pembentukan N2O4!
- 14. 3.Empat mol NOCl terurai dalam ruang 5 liter sesuai reaksi: 2 NOCl(g) ŌåÆ 2 NO(g) + Cl2(g) terbentuk 1 mol gas Cl2, tentukan: a. besarnya laju pengurangan NOCl dalam waktu 20 detik b. besarnya laju pembentukan NO dan Cl2 dalam waktu 10 detik
- 15. Standar Kompetensi: Mengidentifikasi faktor-faktor yang mempengaruhi laju reaksi Kompetensi Dasar: Menjelaskan faktor-faktor yang mempengaruhi laju reaksi
- 17. PRAKTIKUM
- 19. Teori Tumbukan Reaksi kimia terjadi karena adanya tumbukan yang efektif antara partikel-partikel zat yang bereaksi. Tumbukan efektif adalah tumbukan yang mempunyai energi yang cukup untuk memutuskan ikatan-ikatan pada zat yang bereaksi (bereaksi)
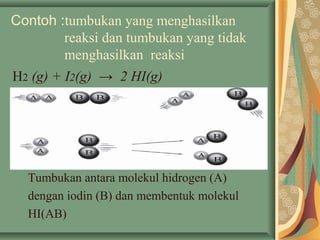
- 20. Contoh :tumbukan yang menghasilkan reaksi dan tumbukan yang tidak menghasilkan reaksi H2 (g) + I2(g) ŌåÆ 2 HI(g) Tumbukan antara molekul hidrogen (A) dengan iodin (B) dan membentuk molekul HI(AB)
- 21. Ilustrasi Mana yang lebih mungkin terjadi tabrakan, di jalan lenggang atau dijalanan padat?
- 22. 1. Konsentrasi Pada umumnya, reaksi berlangsung lebih cepat jika konsentrasi pereaksi diperbesar. Zat yang konsentrasinya besar mengandung jumlah partikel yang lebih banyak, sehingga partikel-partikelnya tersusun lebih rapat dibanding zat yang konsentrasinya rendah, sehingga akan lebih sering bertumbukan dibanding dengan partikel yang susunannya renggang, sehingga kemungkinan terjadinya reaksi makin besar.
- 23. 2. Temperatur Partikel selalu bergerak. Temperatur dinaikkan, energi gerak / energi kinetik partikel bertambah, sehingga tumbukan lebih sering terjadi. Dengan frekuensi tumbukan semakin besar, maka kemungkinan terjadinya tumbukan efektif yang mampu menghasilkan reaksi juga semakin besar. ŌÖźZat-zat yang energi potensialnya kecil, jika bertumbukan akan sukar menghasilkan tumbukan efektif. Suhu ternyata juga memperbesar energi potensial suatu zat, sehingga ketika bertumbukan akan menghasilkan reaksi.
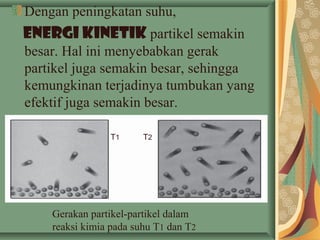
- 24. Dengan peningkatan suhu, energi kinetik partikel semakin besar. Hal ini menyebabkan gerak partikel juga semakin besar, sehingga kemungkinan terjadinya tumbukan yang efektif juga semakin besar. Gerakan partikel-partikel dalam reaksi kimia pada suhu T1 dan T2 T1 T2
- 25. Hubungan Kuntitatif perubahan suhu terhadap laju reaksi: Hubungan ini ditetapkan dari suatu percobaan, misal diperoleh data sebagai berikut: Suhu (o C) Laju reaksi (M/detik) 10 20 30 40 t 0,3 0,6 1,2 2,4 Vt
- 26. Hubungan laju reaksi dengan perubahan suhu dapat dirumuskan : Vt =2n V0 Vt =3n V0 Dengan : n = T2 ŌĆō T1 n = T2 ŌĆō T1 10 20 2 = factor perubahan suhu setiap 10o 3= factor perubahan suhu setiap 20┬║ Vt = Laju pada suhu tertentu V0 = Laju mula-mula T1 = suhu awal T2 = suhu akhir
- 27. Karena laju berbanding terbalik dengan waktu maka rumus diatas juga dapat dinyatakan sebagai berikut: t = 2-n t0 t = 3-n t0 dengan : t = waktu yang diperlukan pada suhu T0 C t0= waktu mula-mula
- 28. Contoh Soal setiap kenaikan 10o C laju reaksi menjadi 2 kali lebih cepat suatu reaksi pada suhu 30o C laju=a ,bila suhu dinaikkan menjadi 100o C maka laju reaksinya adalahŌĆ”.. A.14a B.28a C.32a D.64a E.128a
- 29. Pembahasan n = 100 ŌĆō 30 10 = 7 V100 = 27 . a = 128 a
- 30. Contoh Soal Setiap kenaikan suhu 10┬░C, reaksi akan berlangsung dua kali lebih cepat dari semula. Apabila pada suhu 20┬░C reaksi berlangsung 12 menit, pada suhu 50┬░C reaksi berlangsung selama ... menit A. 0,75 B. 4 C. 1,5 D. 96 E. 2
- 31. Pembahasan t = 2-n t0 n = 50 - 20 10 = 3 t = 2-3 . 12 menit
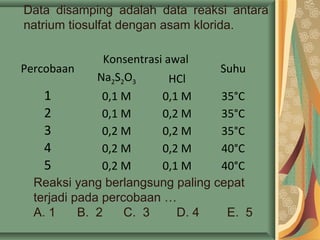
- 32. Percobaan Konsentrasi awal Suhu Na2S2O3 HCl 1 0,1 M 0,1 M 35┬░C 2 0,1 M 0,2 M 35┬░C 3 0,2 M 0,2 M 35┬░C 4 0,2 M 0,2 M 40┬░C 5 0,2 M 0,1 M 40┬░C Reaksi yang berlangsung paling cepat terjadi pada percobaan ŌĆ” A. 1 B. 2 C. 3 D. 4 E. 5 Data disamping adalah data reaksi antara natrium tiosulfat dengan asam klorida.
- 35. Perhatikan bahwa luas permukaan balok utuh lebih kecil dari balok yang dipotong 4
- 37. 3. Luas Permukaan bidang sentuh Pada campuran pereaksi yang heterogen, reaksi hanya terjadi pada bidang batas campuran. Bidang batas campuran inilah yang dimaksud dengan bidang sentuh. Dengan memperbesar luas bidang sentuh, reaksi akan berlangsung lebih cepat.
- 38. 4. Katalis Katalis adalah suatu zat yang berfungsi mempercepat terjadinya reaksi, tetapi pada akhir reaksi dapat diperoleh kembali. Contoh : Ragi, enzim, arang, nikel, platina, nitrogen dioksida dll
- 39. Fungsi katalis Ōś╗ Menurunkan energi aktivasi, sehingga jika ke dalam suatu reaksi ditambahkan katalis, maka reaksi akan lebih mudah terjadi. Hal ini disebabkan karena zat- zat yang bereaksi akan lebih mudah melampaui energi aktivasi. Ōś╗ Memberikan mekanisme reaksi dengan menghsilkan energi aktivasi
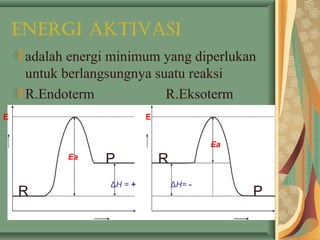
- 40. EnErgi AktivAsi adalah energi minimum yang diperlukan untuk berlangsungnya suatu reaksi R.Endoterm R.Eksoterm Ea Ea R P ΔH = + R P ΔH= - E E
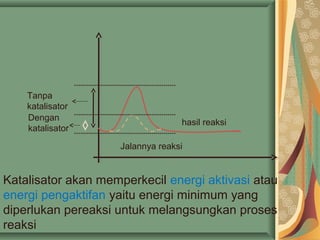
- 41. Tanpa katalisator Dengan katalisator Jalannya reaksi hasil reaksi Katalisator akan memperkecil energi aktivasi atau energi pengaktifan yaitu energi minimum yang diperlukan pereaksi untuk melangsungkan proses reaksi
- 42. Mekanisme Reaksi tanpa Katalis A + B ŌåÆ AB ╬öH = + 100 kJ (lambat) ŌÖź Reaksi dengan Katalis I. A + K ŌåÆ AK ╬öH = + 50 kJ II. AK + B ŌåÆ AB + K ╬öH = + 30 kJ A + B ŌåÆ AB ╬öH = + 80 kJ (cepat)
- 43. Jenis-jenis katalis Katalis Heterogen Katalis Homogen Biokatalis Inhibitor Autokatalis
- 44. Katalis Homogen Katalis yang dapat bercampur secara homogen dengan zat pereaksinya karena mempunyai wujud yang sama ex: 2SO2(g) + O2(g) ŌåÆ 2SO3(g) (lambat) 2SO2(g) + O2(g) ŌåÆ 2SO3(g) (cepat) NO2(g)
- 45. Katalis Heterogen Katalis yang tidak dapat bercampur secara homogen dengan pereaksinya karena wujudnya berbeda C2H4(g) + H2(g) ŌåÆ C2H6(g) (lambat) C2H4(g) + H2(g) ŌåÆ C2H6(g) (cepat) Ni (s)
- 46. Biokatalis Zat yang bertindak sebagai katalis pada proses metabolisme Misalnya: Enzim Ō¢║amilase (menghidrolisis amilum menjadi maltosa) Ō¢║katalase (mengurai H2O2 ŌåÆ O2 + H2O ) Ō¢║lipase (mengurai lipid menjadi gliserol + as.lemak
- 47. Autokatalis Zat hasil reaksi yang bertindak sebagai katalis 2KMnO4(aq) + 5H2C2O4(aq) + 3H2O4(aq) ŌåÆ 2MnSO4(aq) + 10CO2(aq) + K2SO4 + 8H2O katalis
- 48. Inhibitor Zat yang dalam jumlah sangat sedikit dapat mengurangi atau menghambat kerja katalis (racun katalis) Contoh: I2 atau CO bersifat inhibitor pada reaksi: 2H2 + O2 ŌåÆ 2H2O
- 49. Katalis yang digunakan dalam pembuatan asam sulfat adalah ŌĆ” A. nikel B. V2O5 C. Fe D. Zeolit E. Pt
- 50. Katalis yang digunakan dalam pembuatan amonia adalah ŌĆ” A. nikel B. V2O5 C. Fe D. Zeolit E. Pt
- 51. Katalis yang digunakan dalam pembuatan asam nitrat adalah ŌĆ” A. nikel B. V2O5 C. Fe D. Zeolit E. Pt
- 52. Katalis yang digunakan dalam pembuatan mentega adalah ŌĆ” A. nikel B. V2O5 C. Fe D. Zeolit E. Pt
- 53. Katalis yang digunakan dalam pengolahan minyak bumi adalah ŌĆ” A. nikel B. V2O5 C. Fe D. Zeolit E. Pt









![Laju Reaksi
Cepat Lambatnya reaksi berlangsung
Perubahan Konsetrasi pereaksi atau
hasil reaksi dalam satuan waktu.
A + B ŌåÆ C
V = Δ[Reaktan] V= Δ[Produk]
Δt Δt
VA =- Δ[A] VB =-Δ[B] VC =+Δ[C]
Δt Δt Δt](https://image.slidesharecdn.com/laju-reaksi-150215211650-conversion-gate02/85/Laju-reaksi-ok-ppt-9-320.jpg)
![Grafik Laju Reaksi
[ P ]
[ R ]
[ P ] = konsentrasi produk
[ R ] = konsentrasi reaktan](https://image.slidesharecdn.com/laju-reaksi-150215211650-conversion-gate02/85/Laju-reaksi-ok-ppt-10-320.jpg)

![Pembahasan
VN2O5 = - Δ[N2O5]
Δt
= [2 ŌĆō 0,5]
10
= 0,15 M/detik](https://image.slidesharecdn.com/laju-reaksi-150215211650-conversion-gate02/85/Laju-reaksi-ok-ppt-12-320.jpg)